Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

mFe2O3=64%m=0,64mkg ,
mC=1,2%m=0,012m kg
Fe2O3+3C-->3CO+2Fe
mC trong 1 tấn gang=3,6%.1000=36kg
tổng mC=36+0,012 kg
nC=0,001m+3 (kmol)
nFe2O3=0,64m/160=0,004m (kmol)
theo pt và đb=>C dư
-->nCO=nC=3nFe2O3=0,012m
-->nC dư = 3-0,011m(kmol) ->mCdư=36-0,132m
mCO=0,336m
theo đl bảo toàn khối kg ta có:
mthép thu dc=1000+m-0,336m=1000+0,664m
mà lượng thép thu dc chứa 1,2%Cnên ta có
(36-0,132m)/(1000+0,664m)=1,2/100
=>0,139968m=24
=>m=171,46
một loại quặng chứa 82% Fe2O3. Thành phần phần trăm của Fe trong quặng theo khối lượng là bao nhiêu?


Fe+CuSO4--->FeSO4 +Cu
Gọi n\(_{Fe}=1\Rightarrow m_{Fe}=56\left(g\right)\)
m\(_{Cu}=64\left(g\right)\)
Ta có khối lượng Fe tawg 1,2% có nghĩa là
64-56=\(\frac{1,2}{m}\)
=>\(8=\frac{1,2}{m}\)
=>m=\(\frac{12}{8}=1,5\left(g\right)\)

2 A l + 3 C u S O 4 → A l 2 S O 4 3 + 3 C u
x…………3/2.x
F e + C u S O 4 → F e S O 4 + C u
y……..y
Al phản ứng hết với C u S O 4 sau đó Fe mới phản ứng với C u S O 4 . Vì sau phản ứng thu được rắn Y gồm 2 kim loại nên Al đã tan hết và Fe có thể đã phản ứng 1 phần hoặc chưa phản ứng. 2 kim loại trong Y là Fe và Cu.
⇒ n C u = n C u S O 4 = 0,2.1 = 0,2 mol
⇒ m F e dư = m Y - m C u = 15,68 - 0,2.64 = 2,88g
Đặt số mol Al ban đầu là x, số mol Fe phản ứng là y, ta có hệ phương trình:
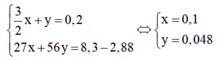
⇒ m A l = 0,1.27 = 2,7g
⇒ % m A l = 2,7/8,3.100 = 32,53%
⇒ Chọn A.

a, 2Al + 3CuSO4 → Al2(SO4)3 + 3Cu
x…………3/2.x
Fe + CuSO4 → FeSO4 + Cu
y……..y
Al phản ứng hết với CuSO4 sau đó Fe mới phản ứng với CuSO4. Vì sau phản ứng thu được rắn Y gồm 2 kim loại nên Al đã tan hết và Fe có thể đã phản ứng 1 phần hoặc chưa phản ứng. 2 kim loại trong Y là Fe và Cu.
⇒ nCu = nCuSO4 = 0,2.1 = 0,2 mol
⇒ mFe dư = mY - mCu = 15,68 - 0,2.64 = 2,88g
Đặt số mol Al ban đầu là x, số mol Fe phản ứng là y, ta có hệ phương trình:
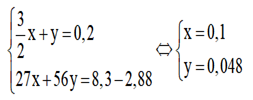
⇒ mAl = 0,1.27 = 2,7g
⇒ %mAl = 2,7/8,3.100 = 32,53%

Xem lại số mol H2 vì theo ĐL bảo toàn nguyên tố thì nH2 =1/2 nHCl mà nH2 ở đây là 0,3 mol và bằng nHCl
\(Mg+2HCl\rightarrow MgCl_2+H_2\)
\(Fe+2HCl\rightarrow FeCl_2+H_2\)
Gọi x,y là số mol Mg, Fe
\(\left\{{}\begin{matrix}24x+56y=5,2\\2x+2y=0,3\end{matrix}\right.\)
=> x=0,1 ; y=0,05
=> \(\%m_{Mg}=\dfrac{0,1.24}{5,2}.100=46,15\%\)
\(\%m_{Fe}=100-46,15=53,85\%\)
\(Mg+2HCl \to MgCl_2+H_2\\ Fe+2HCl \to FeCl_2+H_2\\ n_{Mg}=a(mol)\\\ n_{Fe}=b(mol) m_{hh}=24a+56b=5,2(1)\\ n_{HCl}=2a+2b=0,3(2)\\ (1)(2) a=0,1;b=0,05\\ \%m_{Mg}=\frac{0,1.24}{5,2}.100\%=46,15\%\\ \%m_{Fe}=53,85\%\)

mFe2O3=64%m=0,64mkg ,
mC=1,2%m=0,012m kg
Fe2O3+3C-->3CO+2Fe
mC trong 1 tấn gang=3,6%.1000=36kg
tổng mC=36+0,012 kg
nC=0,001m+3 (kmol)
nFe2O3=0,64m/160=0,004m (kmol)
theo pt và đb=>C dư
-->nCO=nC=3nFe2O3=0,012m
-->nC dư = 3-0,011m(kmol) ->mCdư=36-0,132m
mCO=0,336m
theo đl bảo toàn khối kg ta có:
mthép thu dc=1000+m-0,336m=1000+0,664m
mà lượng thép thu dc chứa 1,2%Cnên ta có
(36-0,132m)/(1000+0,664m)=1,2/100
=>0,139968m=24
=>m=171,46
m đâu ???