Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

n AgCl = \(\dfrac{25,83}{143,5}=0,18\) ( mol )
FeCly + AgNO3 → Fe(NO3)y + AgCl ↓
( mol ) \(\dfrac{0,18}{y}\) ← 0,18
m FeCly = \(\dfrac{0,18}{y}+\left(56+35,5y\right)=9,75\)
\(\Leftrightarrow\dfrac{10,08}{y}+6,39=9,75\)
\(\Leftrightarrow\dfrac{10,08}{y}=3,36\)
\(\Leftrightarrow10,08=3,36y\)
\(\Leftrightarrow\dfrac{10,08}{3,36}=3\)
Cồn thức hóa học của muối sắt là: FeCl3

Hỗn hợp khí B gồm CO và CO2 khi tác dụng với dd chứa 0,025 mol Ca(OH)2 chắc chắc tạo 2 muối
Ta có: \(n_{CaCO_3}=\dfrac{2}{100}=0,02\left(mol\right)\)
PTHH: \(CO_2+Ca\left(OH\right)_2\rightarrow CaCO_3\downarrow+H_2O\)
0,02______0,02______0,02 (mol)
\(2CO_2+Ca\left(OH\right)_2\rightarrow Ca\left(HCO_3\right)_2\)
0,01_____0,005_______0,005 (mol)
\(\Rightarrow n_{CO_2}=0,03\left(mol\right)\) \(\Rightarrow m_{CO_2}=0,03\cdot44=1,32\left(g\right)\)
Bảo toàn nguyên tố: \(n_{CO\left(p/ứ\right)}=n_{CO_2}=0,03\left(mol\right)\) \(\Rightarrow m_{CO}=0,03\cdot28=0,84\left(g\right)\)
Bảo toàn khối lượng: \(m_A=m_{oxit}+m_{CO}-m_{CO_2}=1,12\left(g\right)\)
PTHH: \(2A+2zHCl\rightarrow ACl_z+zH_2\uparrow\) (z là hóa trị của A)
Ta có: \(n_{H_2}=\dfrac{0,448}{22,4}=0,02\left(mol\right)\)
\(\Rightarrow n_A=\dfrac{0,04}{z}\left(mol\right)\) \(\Rightarrow M_A=\dfrac{1,12}{\dfrac{0,04}{z}}=28z\)
Ta thấy với \(z=2\) thì \(M_A=56\) \(\Rightarrow\) Kim loại A là Fe
Gọi công thức oxit cần tìm là FexOy
Bảo toàn Oxi: \(n_{O\left(oxit\right)}=2n_{CO_2}-n_{CO}=0,03\left(mol\right)\)
Xét tỉ lệ \(x:y=0,02:0,03=2:3\)
Vậy công thức oxit là Fe2O3

/ nồng độ dung dịch KAl(SO4)2 bão hòa ở 20 độ C là 5,66%=> 600g dd KAl(SO4)2 chứa 600*5,66%=33,96g KAl(SO4)2 và 600-33,96g=566,04g H2O
độ tan = (33,96*100)/566,04=5,9996
b/ mH2O còn lại = 566,04-200=366,04g
nKAl(SO4)2=33,96/258 (mol)
nH2O=336,04/18(mol)
KAl(SO4)2 + 12H2O --->KAl(SO4)2.12H2O
33,96/258--------336,04/18
=> H2O dư
=>nKAl(SO4)2.12H2O=nKAl(SO4)2=33,96/25...
=>mKAl(SO4)2.12H2O=33,96/258*474=62,39...

Giả sử mol CO2 pứ là: x và y (mol)
CO2 + Ca(OH)2 → CaCO3↓ + H2O
x → x x
2CO2 + Ca(OH)2 → Ca(HCO3)2
y → 0,5y 0,5y
Ca(HCO3)2 + Ba(OH)2 → CaCO3↓ + BaCO3↓ + 2H2O
0,5y → 0,5y 0,5y
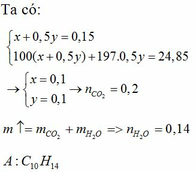
b.
A có CTPT là: C10H14. Vậy nên trong A: số vòng + số pi = 4
A lại không tác dụng với KMnO4 nên liên kết pi chỉ có thể trong vòng → có vòng benzen A tạo 1 monoclo duy nhất nên A chỉ có thể là: CH3–C(CH3)(C6H5)–CH3

Lấy 7,11 gam phèn nung tới khối lượng không đổi thì thu được 3,87 gam phèn khan. => Khối lượng nước ở trong phèn là:
mH2O(.)phèn = 7,11 – 3,87 = 3,24(g)
Số mol nước ở trong phèn: nH2O(.) phèn = 3,24/18 = 0,18 (mol)
Số mol kết tủa BaSO4: nBaSO4 = 6,99/233 = 0,03 (mol)
Ta có: Số mol phèn = ½ số mol của kết tủa
BaSO4 = ½ x 0,03 = 0,015 (mol)
Do đó khối lượng mol của phèn là: M phèn = 7,11/0,015 = 474(g)
Vì số mol của H2O trong phèn là 0,18 và số mol của phèn là 0,015 nên ta có phương trình: 0,015n = 0,18. Giải ra được: n = 12.
Do đó khối lượng của kim loại M trong phèn là:
MM = 474 – 27 - 12x18 – 96x2 = 39 (g) => M là Kali
(thỏa mãn là kim loại thuộc nhóm IA bảng tuần hoàn các NTHH).
Kết luận: Vậy CTPT của phèn là : KAl(SO4)2.12H2O.

pthh: FeCln + nAgNO3 ---. Fe(NO3)n +nAgCl
(56+35.5n) n*143.5
16.25 40.05
Nhân chéo,ta có: 40.05*(56+35.5n)=16.25*143.5n
giải pt trên được n=???
em kiểm tra đề giúp anh nha!!!

a, PT: \(MO+CO\underrightarrow{t^o}M+CO_2\)
Ta có: \(n_{MO}=\dfrac{7,2}{M_M+16}\left(mol\right)\)
\(n_M=\dfrac{5,6}{M_M}\left(mol\right)\)
Theo PT: \(n_{MO}=n_M\) \(\Rightarrow\dfrac{7,2}{M_M+16}=\dfrac{5,6}{M_M}\)
\(\Rightarrow M_M=56\left(g/mol\right)\)
⇒ M là Fe.
Vậy: Oxit kim loại đó là FeO.
b, Theo PT: \(n_{CO_2}=n_M=\dfrac{5,6}{56}=0,1\left(mol\right)\)
PT: \(CO_2+Ca\left(OH\right)_2\rightarrow CaCO_{3\downarrow}+H_2O\)
Theo PT: \(n_{CaCO_3}=n_{CO_2}=0,1\left(mol\right)\)
\(\Rightarrow m_{\downarrow}=m_{CaCO_3}=0,1.100=10\left(g\right)\)
Bạn tham khảo nhé!


bn check lại xem là KAl(SO4)3.nH2O hay KAl(SO4)2.nH2O nhé