Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Vì nguyên tử trung hòa về điện ⇒ PM = EM và PX = EX
- Tổng số hạt trong MX2 là 186 hạt.
⇒ 2PM + NM + 2.(2PX + NX) = 186 (1)
- Trong MX2 số hạt mang điện nhiều hơn số hạt không mang điện là 54 hạt.
⇒ 2PX - 2+ 2.2PX + 2 - NM - 2NX = 54 (2)
- Khối lượng của M2+ lớn hơn khối lượng của X- là 21 amu.
⇒ PM + NM - (PX + NX) = 21 (3)
- Tổng số hạt trong M2+ nhiều hơn X- là 27 hạt.
⇒ (2PM + NM - 2) - (2PX + NX + 1) = 27 (4)
Từ (1), (2), (3) và (4) \(\Rightarrow\left\{{}\begin{matrix}P_M=E_M=26\\N_M=30\\P_X=E_X=17\\N_X=18\end{matrix}\right.\)

Bài toán không đơn thuần chỉ là tìm ra chất mà còn tích hợp cả kiến thức về tính chất hóa học của các chất. Nếu tìm được chất mà không nắm chắc tính chất hóa học của chất đó thì quá trình tìm chất trở nên vô nghĩa. Vì vậy để làm được bài này các bạn cần phải nắm chắc kiến thức về tính chất hóa học của các chất.
Gọi lần lượt là số proton, nơtron của M và X.
Theo giả thiết ta có:
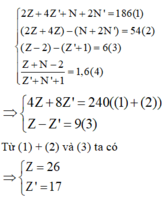
M là Fe và X là Cl.
Vậy hợp chất cần tìm là FeCl2
Xét các đáp án:
A: Đúng: kết tủa là AgCl
B: Sai: Dung dịch muối FeCl2 không làm thay đổi màu quỳ tím
C: Sai: FeCl2 là chất điện li mạnh
D: Sai: FeCl2 vừa thể hiện tính oxi hóa vừa thể hiện tính khử do Fe ở trạng thái oxi hóa trung gian
Đáp án A.

Tổng số các hạt trong phân tử là 140 → 2ZX + NX + 2.( 2ZM + NM ) = 140 (1)
Số hạt mang điện nhiều hơn số hạt không mang điện là 44 hạt → 2ZX+ 2. 2ZM - NX- 2. NM = 44 (2)
Giải hệ (1), (2) → 4ZM+ 2ZX= 92, 2NM+ NX = 48
Số khối của M+ lớn hơn số khối của X2- là 23.→ ZM + NM - ( ZX + NX) = 23 (3)
Tổng số hạt trong M+ nhiều hơn trong X2- là 31 → [2.ZM + NM -1]- [2ZX + NX+2] = 31 (4)
Lấy (4) - (3) → ZM - ZX = 11
Ta có hệ
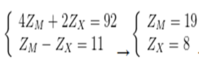
M là K và X là O
Vậy công thức là K2O.
Đáp án A.

Gọi p, e, n là số proton, số electron và số nơtron trong một nguyên tử M; p’, e’, n’ là số proton, số electron và số nơtron trong một nguyên tử X.
Trong nguyên tử số proton = số electron; các hạt mang điện là proton và electron, hạt không mang điện là nơtron.
+ Trong phân tử của M2X2 có tổng số hạt proton, nơtron và electron là 164 nên suy ra:
2(2p + n) + 2(2p’ + n’) = 164 (1)
+ Trong đó số hạt mang điện nhiều hơn hạt không mang điện là 52 nên suy ra:
(4p + 4p’) - 2(n + n’) = 52 (2)
+ Số khối của M lớn hơn số khối của X là 23 đơn vị nên ta có suy ra:
(p + n) - (p’ + n’) = 23 (3)
+ Tổng số hạt electron trong M+ nhiều hơn trong X22- là 7 hạt nên suy ra:
(2p + n - 1) - 2(2p’ + n’) + 2 = 7 (4)
Giải hệ (1), (2), (3), (4) ta được p = 19 ⇒ M là kali; p’ = 8 ⇒ X là oxi.
Công thức phân tử của hợp chất là K2O2.
*Tk

Gọi số hạt proton, electron, notron trong M lần lượt là \(p_M;e_M;n_M\)
số hạt proton, electron, notron trong X lần lượt là \(p_X;e_X;n_X\)
\(\Rightarrow2p_M+n_M+2p_X+n_X=86\left(1\right)\)
Mà số hạt mang điện nhiều hơn số hạt không mang điện là 26
\(\Rightarrow2p_M-n_M+2p_X-n_X=26\left(2\right)\)
Ta có số khối của X lớn hơn số khối của M là 12
\(\Rightarrow p_X+n_X-p_M-n_M=12\left(3\right)\)
Tổng số hạt trong X nhiều hơn trong M là 18
\(\Rightarrow2p_X+n_X-2p_M-n_M=18\left(4\right)\)
Từ (1); (2); (3); (4) ta có:
\(p_M=11;n_M=12;p_X=17;n_X=18\)
Vậy M là Na còn X là Cl
Tổng số hạt trong MX (Phân tử gồm 1 nguyên tử M + 1 nguyên tử X):
2ZM + NM + 2ZX + NX = 86
Trong phân tử MX, số hạt mang điện (2ZM + 2ZX) nhiều hơn số hạt không mang điện (NM + NX):
(2ZM + 2ZX) – (NM + NX) = 26
Số khối của X (ZX + NX) lớn hơn số khối của M (ZM + NM):
(ZX + NX) – (ZM + NM) = 12
Tổng số hạt trong X (2ZX + NX) nhiều hơn tổng số hạt trong M (2ZM + NM):
(2ZX + NX) – (2ZM + NM) = 18
Giải hệ trên được:
ZM = 11
ZX = 17
Vậy M là Na, X là Cl

