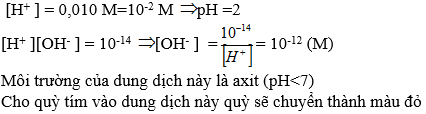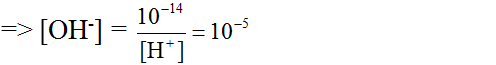Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

[H+] = 0,010M = 10-2M ⇒ pH = -log[H+] = -log(1,0.10-2) = 2
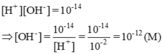
Môi trường của dung dịch này là axit (pH < 7)
Cho quỳ tím vào dung dịch này quỳ sẽ chuyển thành màu đỏ

[H+] = 0,01M = 10-2M => pH = 2
[OH-] = 10-14 / 10-2M =10-12
Dung dịch có pH = 2 < 7 => môi trường axit, quỳ tím có màu đỏ.

[OH-]=1.10^-14/0.01=10^-12 (M) tính Ph=log[H+] từ kết quả của Ph xem nó lớn hơn 7 hay j xong suy ra môi trường ,môi trường axit thì quỳ đỏ môi trường kiềm quy xanh trung tính ko màu

pH = 9,0 ≥ [H+] = 10-9 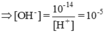
Cho phenolphtalein trong dung dịch này sẽ thấy phenolphtalein chuyển thành màu hồng (khi pH ≥ 8,3 phenolphtalein đổi màu)

pH=9 => CH+=10-9 và COH-=10-5
Đọo pH của dung dịch có môi trường kiêm nên Phenolphtalein có màu hồng (cái này trong sách giáo khoa 11 có)

a)
\([OH^-] = C_{M_{NaOH}} = 0,01M\\ [H^+] = \dfrac{10^{-14}}{[OH^-]} = 10^{-12}M\\ \Rightarrow pH = -log([H^+]) = 12\)
Dung dịch này làm quỳ tím hóa xanh, làm dung dịch phenolphtalein chuyển sang màu đỏ.
b)
\([H^+] = C_{M_{HCl}} = 0,01M\\ \Rightarrow pH = -log([H^+]) = -log(0,01) = 2\)
Dung dịch này làm quỳ tím hóa đỏ, không làm đổi màu dung dịch phenolphtalein.