Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án A
Sơ đồ ta có:

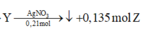
( Z phản ứng với 0,165 mol Br2)
Có
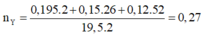
nH2phản ứng = nX- nY = 0,195 mol
+ Chất tham gia phản ứng với AgNO3/NH3 lần lượt là C2H2 dư : amol, C4H4 : b mol và CH≡C-CH2-CH3: c mol
Có 2a + b + c = 0,21
nY=a +b +c + nZ → a+b +c =0,135
+ Bảo toàn liên kết π → 2a + 3b + 2c = ( 0,15.2+ 0,12. 3) - 0,195 - 0,165
+ Giải hệ → a = 0,075; b = 0,03 và c = 0,03
m↓ =0,075. 240 + 0,03. 159 + 0,03, 161 = 27,6 gam.

Đáp án C
Có nX = 0 , 5 × 26 + 0 , 4 × 52 + 0 , 65 × 2 19 , 5 × 2 = 0,9 mol
Có nH2 pư = 0,5 +0,4 + 0,65- 0,9 = 0,65 mol
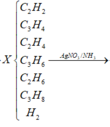
Chất tạo kết tủa với AgNO3/NH3dư gồm
CH≡CH dư : x mol, CH2=CH-C≡CH : y mol và CH≡C-CH2-CH3 : z mol
Ta có hệ →

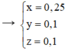
→ m = 0,25×(26 + 107.2) + 0,1×(52 + 107) + 0,1×(54 + 107) = 92 gam.

Khi cho hỗn hợp gồm ![]() và
và ![]() , H2 có chứa bột Ni nung nóng một thời gian thì các phản ứng có thể xảy ra:
, H2 có chứa bột Ni nung nóng một thời gian thì các phản ứng có thể xảy ra:
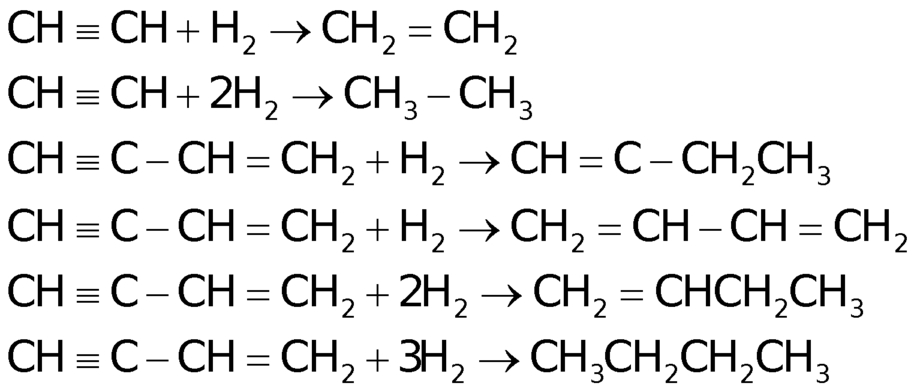
Có nhiều phản ứng có thể xảy ra tương ứng với nhiều sản phẩm. Do đó chúng ta cần biện luận dựa vào giả thiết đề bài để tìm ra thành phần của hỗn hợp khí X. Đây là một bài tập khá phức tạp, nếu chưa xác định được ngay hướng làm thì ta sẽ phân tích lần lượt các giả thiết:
Đầu tiên, áp dụng định luật bảo toàn khối lượng ta có:
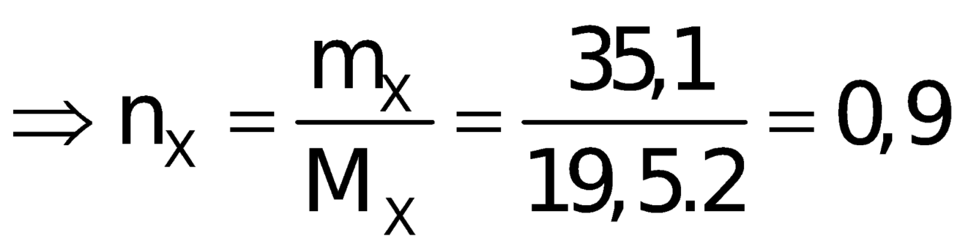
![]()
=> nH2 phản ứng= n khí giảm= n khí bđ - nX
![]()
Mà nH2 ban đầu=0,65
Nên H2 đã phản ứng hết và trong X chỉ gồm các hidrocacbon.
Vì X có phản ứng tạo kết tủa với dung dịch AgNO3/ NH3 nên trong X có chứa các hidrocacbon có liên kết ba đầu mạch, các hidrocacbon này có thể là ![]() và
và ![]() .
.
Mặt khác MX = 19,5.2 = 39
Khi cho X qua dung dịch AgNO3/ NH3 có thoát ra khí Y với nY = 0,45.
Mà ![]() nên n liên kết(Y)=nBr2=0,45
nên n liên kết(Y)=nBr2=0,45
Lại có n hidrocacbon phản ứng với AgNO3/NH3=nX-nY=0,45
Mà n AgNO3 phản ứng =0,7> 0,45 nên trong X chắc chắn chứa C2H2.
Trong X, gọi
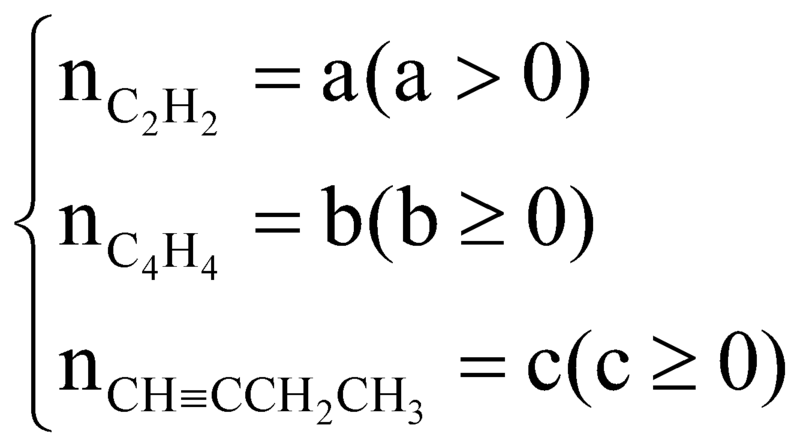
Ta có:
C2H2 -> Ag2C2
C2H4 -> AgC ≡ CCH=CH2
CH=CCH2CH3-> AgC ≡ CCH2ch3
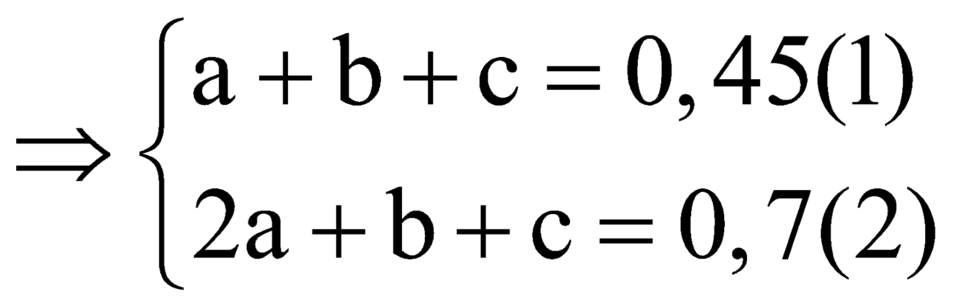
![]()
Từ (1), (2) và (3) có
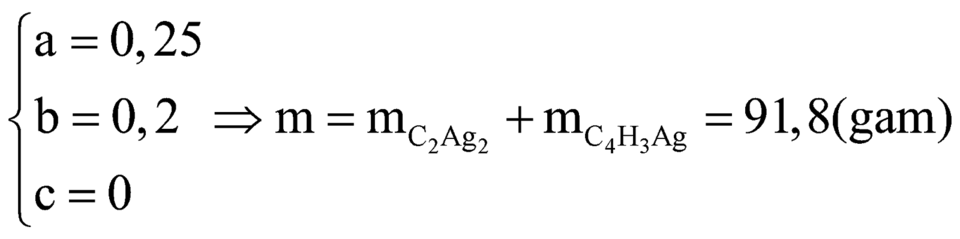

Chọn đáp án D.
Đặt số mol của
![]()
trong X lần lượt là x, y, z.
![]()
![]()
Bảo toàn khối lượng có:
![]()
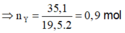
⇒ n H 2 p h ả n ứ n g = 0,5 + 0,4 + 0,65 - 0,9 = 0,65 mol
Áp dụng bảo toàn liên kết π có:
![]()
Từ (1), (2), (3) suy ra
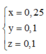
![]()
![]()
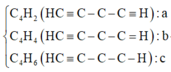
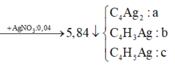
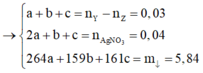
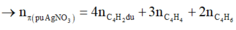
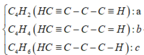
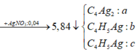
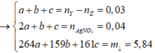
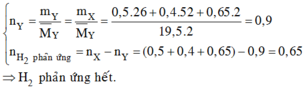
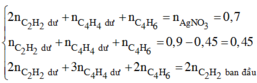
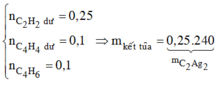
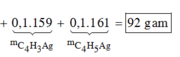
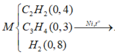
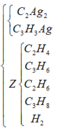
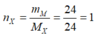
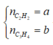
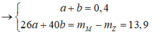
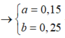
Đáp án C
n khí giảm = nH2 pư = 0,195 mol => H2 phản ứng hết
Kết tủa gồm