
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


CuO + H2 -> Cu + H2O
0.01 0.01
FexOy + yH2 -> xFe + yH2O
Fe + 2HCl -> FeCl2 + H2
\(\)0.02 0.02 \(\)
Cu + HCl -> (không phản ứng)
nH2 = 0.02mol => mFe = 1.12g
=> mCu = 1.76 - 1.12 = 0.64g => nCu = 0.01mol
=> mCuO = 0.8g => mFexOy = 2.4 - 0.8 = 1.6g
Ta có: 56x + 16y -> 56x
1.6g -> 1.12g
=> \(1.6\times56x=1.12\times\left(56x+16y\right)\)
=> \(26.88x=17.92y\Leftrightarrow\dfrac{x}{y}=\dfrac{2}{3}\)
=> Fe2O3

Bài 8 :
200ml = 0,2l
\(n_{HCl}=0,2.1=0,2\left(mol\right)\)
Pt : \(R+2HCl\rightarrow RCl_2+H_2|\)
1 2 1 1
0,1 0,2 0,1
a) \(n_{H2}=\dfrac{0,2.1}{2}=0,1\left(mol\right)\)
\(V_{H2\left(dktc\right)}=0,1.22,4=2,24\left(l\right)\)
b) \(n_R=\dfrac{0,2.1}{2}=0,1\left(mol\right)\)
⇒ \(M_R=\dfrac{2,4}{0,1}=24\) (g/mol)
Vậy kim loại R là magie
Chúc bạn học tốt

a) - Dùng quỳ tím:
+ Hóa đỏ -> dd H2SO4
+ Hóa xanh -> dd NaOH
+ Không đổi màu -> dd NaCl
b) - Dùng quỳ tím:
+ Hóa xanh -> dd Ca(OH)2
+ Hóa đỏ -> dd H2SO4, dd HCl
- Dùng dd BaCl2:
+ Có kết tủa trắng BaSO4 -> dd H2SO4
+ Không có kt trắng -> dd HCl
PTHH: H2SO4 + BaCl2 -> BaSO4 (kt trắng) + 2 HCl

Ta có: \(n_{SO_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
a. PTHH:
Na2SO3 + H2SO4 ---> Na2SO4 + SO2 + H2O (1)
K2SO3 + H2SO4 ---> K2SO4 + SO2 + H2O (2)
Theo PT(1,2): \(n_{H_2SO_4}=n_{SO_2}=0,3\left(mol\right)\)
=> \(m_{H_2SO_4}=0,3.98=29,4\left(g\right)\)
b. Gọi x, y lần lượt là số mol của Na2SO3 và K2SO3
Theo PT(1,2):
=> x + y = 0,3
Theo đề, ta có: 126x + 158y = 44,2
=> x = 0,1, y = 0,2
Theo PT(1): \(n_{Na_2SO_4}=n_{Na_2SO_3}=0,1\left(mol\right)\)
=> \(m_{Na_2SO_4}=0,1.142=14,2\left(g\right)\)
Theo PT(2): \(n_{K_2SO_4}=n_{K_2SO_3}=0,2\left(mol\right)\)
=> \(m_{K_2SO_4}=0,2.164=34,8\left(g\right)\)
=> \(m_{sau.phản.ứng}=34,8+14,2=49\left(g\right)\)
Ta có: \(C_{\%_{H_2SO_4}}=\dfrac{0,3.98}{m_{dd_{H_2SO_4}}}.100\%=20\%\)
=> \(m_{dd_{H_2SO_4}}=147\left(g\right)\)
Ta có: \(m_{dd_{sau.phản.ứng}}=147+44,2=191,2\left(g\right)\)
=> \(C_{\%_{dd_{sau.phản.úng}}}=\dfrac{49}{191,2}.100\%=25,63\%\)
c. Đổi 500ml = 0,5 lít
=> \(n_{Ba\left(OH\right)_2}=1.0,5=0,5\left(mol\right)\)
Ta có: \(T=\dfrac{n_{SO_2}}{n_{Ba\left(OH\right)_2}}=\dfrac{0,3}{0,5}=0,6< 1\)
Vậy PTHH là: \(SO_2+Ba\left(OH\right)_2--->BaSO_3+H_2O\) (Ba(OH)2 dư.)
Theo PT: \(n_{BaSO_3}=n_{SO_2}=0,3\left(mol\right)\)
=> \(m_{BaSO_3}=0,3.217=65,1\left(g\right)\)
\(n_{SO_2}=\dfrac{6,72}{22,4}=0,3mol\)
\(Na_2SO_3+H_2SO_4\rightarrow Na_2SO_4+H_2O+SO_2\)
\(x\) \(x\)
\(K_2SO_3+H_2SO_4\rightarrow K_2SO_3+H_2O+SO_2\)
\(y\) \(y\)
Ta có: \(\left\{{}\begin{matrix}126x+158y=44,2\\x+y=0,3\end{matrix}\right.\) \(\Rightarrow\left\{{}\begin{matrix}x=0,1\\y=0,2\end{matrix}\right.\)
a)\(\Rightarrow\Sigma n_{H_2SO_4}=0,1+0,2=0,3mol\)
\(\Rightarrow m_{H_2SO_4}=0,3\cdot98=29,4\left(g\right)\)
\(\Rightarrow m_{ddH_2SO_4}=\dfrac{29,4}{20}\cdot100=147\left(g\right)\)
b)

Câu 1
1)
$(1) 4FeS_2 + 11O_2 \xrightarrow{t^o} 2Fe_2O_3 + 8SO_2$
$(2) 2SO_2 + O_2 \xrightarrow{t^o,V_2O_5} 2SO_3$
$(3) SO_3 + H_2O \to H_2SO_4$
$(4)6FeSO_4 + 3Cl_2 \to 2Fe_2(SO_4)_3 + 2FeCl_3$
$(5) Fe_2(SO_4)_3 + 3BaCl_2 \to 3BaSO_4 + 2FeCl_3$
$(6) FeCl_3 + 3KOH \to Fe(OH)_3 + 3KCl$
$(7) 2Fe(OH)_3 \xrightarrow{t^o} Fe_2O_3 + 3H_2O$
2)
Trích mẫu thử
Cho dung dịch phenolphtalein vào
- mẫu thử hóa hồng là NaOH
Cho ba mẫu thử còn lai tác dụng lần lượt với nhau
- mẫu thử tạo kết tủa trắng là $H_2SO_4,Ba(NO_3)_2$
$Ba(NO_3)_2 + H_2SO_4 \to BaSO_4 + 2HNO_3$
- mẫu thử không hiện tượng là HCl
Cô cạn hai mẫu thử còn :
- mẫu thử thu được chất rắn khan là $Ba(NO_3)_2$
- mẫu thử không thu được chất rắn là $H_2SO_4$






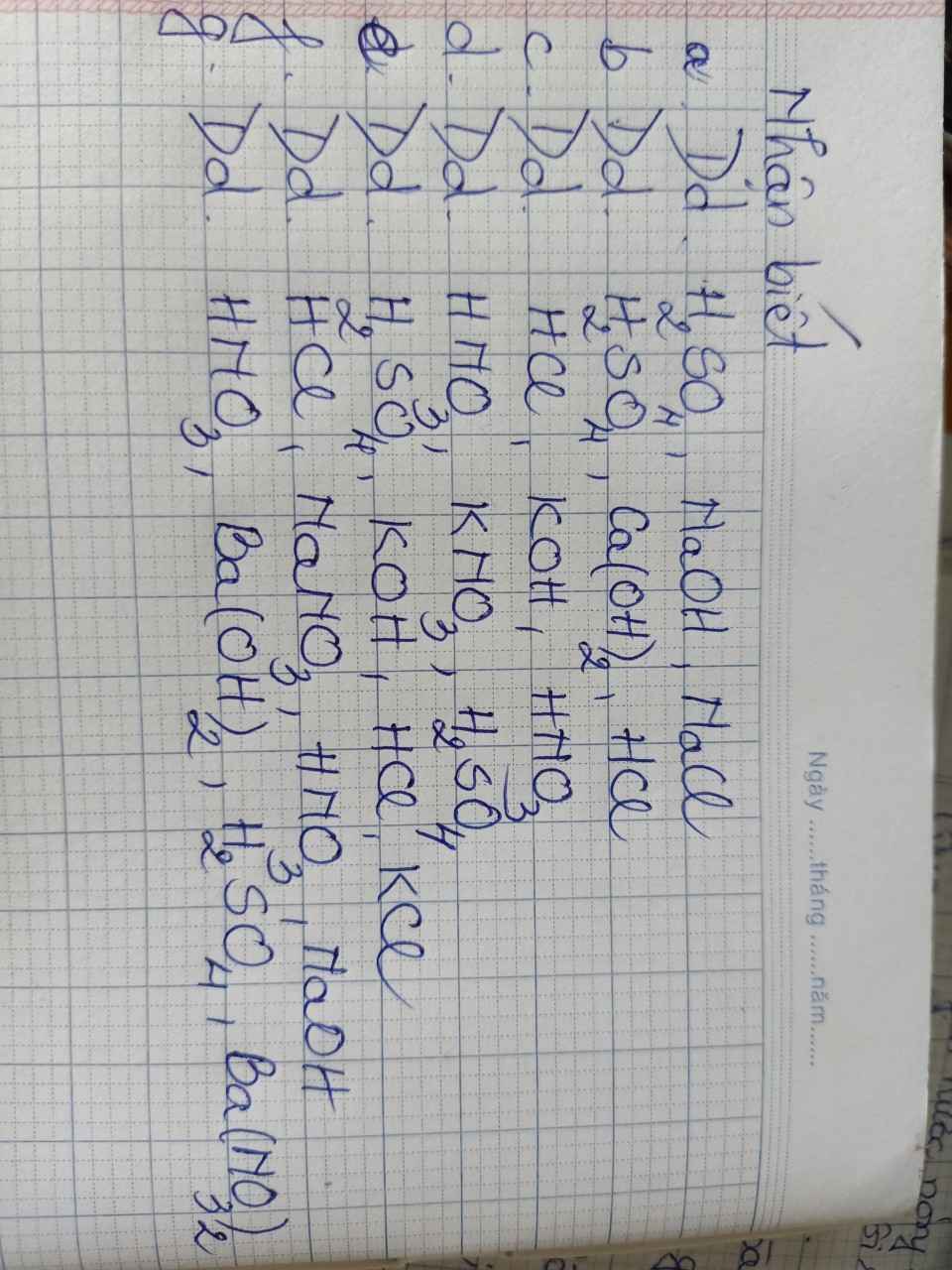
 giúp với ạa
giúp với ạa


