
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


X: Fe3O4
Y: FeCl2
Z: FeCl3
T: Fe(OH)2
U: Fe(OH)3
A: NaCl (hoặc H2O)
B: H2O (hoặc NaCl)
D: H2 (hoặc Cl2)
E: Cl2 (hoặc H2)
F: NaOH
G: HCl
PTHH:
a) NaCl + H2O -dpmn----> 1/2 H2 + 1/2 Cl2 + NaOH
H2 + Cl2 -to-> 2 HCl
HCl + NaOH -> NaCl + H2O
b) 3 Fe +2 O2 -to->Fe3O4
Fe3O4 + 8 HCl -> FeCl2 +2 FeCl3 + H2O
FeCl2 + 2 NaOH -> Fe(OH)2 + 2 NaCl
FeCl3 +3 NaOH -> Fe(OH)3 + 3NaCl
Chúc em học tốt!


$2Fe + 6H_2SO_4 \to Fe_2(SO_4)_3 + 3SO_2 + 6H_2O(1)$
$Fe_2(SO_4)_3 + Fe\ to 3FeSO_4(2)$
Gọi $n_{Fe_2(SO_4)_3} = a(mol) ; n_{FeSO_4} = b(mol)$
Ta có : $400a + 152b = 62,8(1)$
$n_{SO_2} = 0,15(mol)$
$n_{Fe_2(SO_4)_3(1)} = \dfrac{1}{3}n_{SO_2} = 0,05(mol)$
$n_{Fe_2(SO_4)_3(2)} = \dfrac{1}{3}n_{FeSO_4} = \dfrac{b}{3}$
Suy ra:
$0,05 - \dfrac{b}{3} = a(2)$
Từ (1)(2) suy ra $a = \dfrac{45}{112} ; b = -1,055<0$
=> Sai đề


12.
Na2CO3+H2SO4->Na2SO4+H2O+CO2
............. 0,5 ............. ......... 0,5
CO2+2KOH->K2CO3+H2O
x 2x x
CO2+KOH->KHCO3
y y y
mKOH=98.40/100=39,2g
nKOH=39,2/56=0,7mol
Có:
2x+y=0,7
138x+100y=57,6
=>x=0,2mol; y=0,3mol
mK2CO3=138.0,2=27,6g
mKHCO3=57,6-27,6=30g
b.
nCO2=x+y=0,2+0,3=0,5mol
CMddH2SO4=0,5/0,2=2,5M
8. Hoàn thành sơ đồ chuyển hóa sau:
Mg \(\underrightarrow{\left(1\right)}\) MgO \(\underrightarrow{\left(2\right)}\) MgCl2 \(\underrightarrow{\left(3\right)}\) Mg(OH)2 \(\underrightarrow{\left(4\right)}\) MgO \(\underrightarrow{\left(5\right)}\) MgSO4 \(\underrightarrow{\left(6\right)}\) MgCO3 \(\underrightarrow{\left(7\right)}\) MgO
\(\left(1\right)2Mg+O_2\underrightarrow{t^o}2MgO\)
\(\left(2\right)MgO+2HCl\rightarrow MgCl_2+H_2O\)
\(\left(3\right)MgCl_2+2NaOH\rightarrow Mg\left(OH\right)_2\downarrow+2NaCl\)
\(\left(4\right)Mg\left(OH\right)_2\underrightarrow{t^o}MgO+H_2O\)
\(\left(5\right)MgO+H_2SO_4\rightarrow MgSO_4+H_2O\)
\(\left(6\right)MgSO_4+Na_2CO_3\rightarrow MgCO_3+Na_2SO_4\)
\(\left(7\right)MgCO_3\underrightarrow{t^o}MgO+CO_2\uparrow\)

1. a) Tên gọi của axit:
HNO3: axit nitric
HCl: axit clohidric
H2CO3: axit cacbonic
H2S: axit sunfuhidric
H2SO4: axit sunfuric
H2SO3: axit sunfurơ
Axit mạnh: HCl, HNO3, H2SO4...
Axit yếu: H2S, H2CO3...

Câu 9: Theo đề : Vd d HCl=200ml=0,2 (lít)
=> nHCl=CM.V=3,5.0,2=0,7(mol)
Gọi a,b lần lượt là số mol của CuO và Fe2O3
PT1: CuO +2HCl -> CuCl2 +H2O
cứ : 1............2............1..........1 (moL)
Vậy : a -> 2a -> a (mol)
PT2: Fe2O3 + 6HCl -> 2FeCl3 + 3H2O
cứ-: 1..............6.............2 (moL)
vậy : b -> 6b -> 2b (mol)
Từ PT và đề ,ta có:
2a + 6b=0,7
80a + 160b=20
Giải hệ PT ,ta được : a=0,05(mol) , b=0,1 (mol)
=> mCuO=n.M=0,05.80=4(gam)
=> mFe2O3=n.M=0,1.160=16(gam)
Vậy chọn câu A
Câu 10 : ( cũng tương tự)
Vd d HCl=100ml=0,1 lít=> nHCl=CM.V=3.0,1=0,3 (mol)
Gọi x,y lần lượt là số mol của CuO và ZnO
PT1: CuO + 2HCl -> CuCl2 + H2O
cứ- : 1...........2.............1.............1 (mol)
Vậy: x -> 2x -> x (mol)
PT2: ZnO + 2HCl -> ZnCl2 +H2O
Cứ- : 1.............2...........1.............1 (mol)
Vậy : y -> 2y -> y (mol)
Từ PT và đề , ta có:
2x +2y=0,3
80x+ 81y=12,1
Giải PT, ta cũng có: x=0,05 , y=0,1
=> mCuO=n.M=0,05.80=4 (gam)
=>mZnO=n.M=0,1.81=8,1 (gam)
=> %CuO=\(\dfrac{m_{CuO}.100\%}{m_{hh}}=\dfrac{4.100}{12,1}\approx33,06\left(\%\right)\)
%ZnO=\(100\%-\%CuO=100-33,06=66,94\left(\%\right)\)





 Giúp hộ mình nha !!!
Giúp hộ mình nha !!!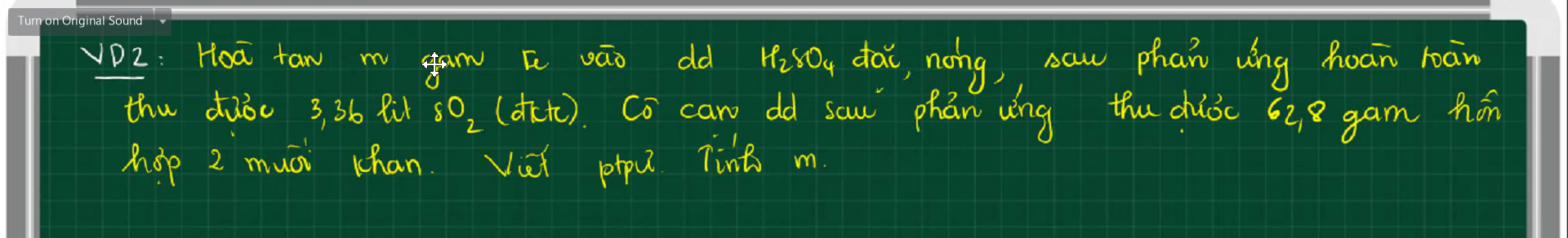





 Giúp hộ mình nha !!!
Giúp hộ mình nha !!! Cảm ơn bạn !!!
Cảm ơn bạn !!!
 Giúp mình nha !!!
Giúp mình nha !!!
 mn giúp e những câu còn lại ạ :)
mn giúp e những câu còn lại ạ :)
Y chứa NaOH, NaAlO2
Gọi số mol NaOH, NaAlO2 trong mỗi phần là x, y (mol)
TN1:
\(n_{HCl}=0,1.1=0,1\left(mol\right)\)
PTHH: NaOH + HCl --> NaCl + H2O
0,1<----0,1
=> x = 0,1 (mol)
TN3: nHCl = 0,75.1 = 0,75 (mol)
PTHH: NaOH + HCl --> NaCl + H2O
0,1--->0,1
NaAlO2 + HCl + H2O --> NaCl + Al(OH)3
y------>y------------------------>y
Al(OH)3 + 3HCl --> AlCl3 + 3H2O
\(\dfrac{0,65-y}{3}\)<-(0,65-y)
=> \(n_{Al\left(OH\right)_3\left(3\right)}=y-\dfrac{0,65-y}{3}=\dfrac{4y-0,65}{3}\left(mol\right)\)
TN2: \(n_{HCl}=1.0,45=0,45\left(mol\right)\)
- Nếu kết tủa không bị hòa tan:
PTHH: NaOH + HCl --> NaCl + H2O
0,1--->0,1
NaAlO2 + HCl + H2O --> NaCl + Al(OH)3
0,35<--0,35-------------------->0,35
Điều kiện: y \(\ge\) 0,35
=> \(n_{Al\left(OH\right)_3\left(2\right)}=0,35\left(mol\right)\)
Do \(n_{Al\left(OH\right)_3\left(2\right)}=3.n_{Al\left(OH\right)_3\left(3\right)}\)
=> \(0,35=4y-0,65\)
=> y = 0,25 (Loại)
=> Kết tủa bị hòa tan 1 phần
PTHH: NaOH + HCl --> NaCl + H2O
0,1--->0,1
NaAlO2 + HCl + H2O --> NaCl + Al(OH)3
y---->y------------------------->y
Al(OH)3 + 3HCl --> AlCl3 + 3H2O
\(\dfrac{0,35-y}{3}\)<--(0,35-y)
=> \(n_{Al\left(OH\right)_3\left(2\right)}=y-\dfrac{0,35-y}{3}=\dfrac{4y-0,35}{3}\left(mol\right)\)
Do \(n_{Al\left(OH\right)_3\left(2\right)}=3.n_{Al\left(OH\right)_3\left(3\right)}\)
=> \(\dfrac{4y-0,35}{3}=4y-0,65\)
=> y = 0,2
Vậy trong Y chứa \(\left\{{}\begin{matrix}NaOH:0,3\left(mol\right)\\NaAlO_2:0,6\left(mol\right)\end{matrix}\right.\)
Bảo toàn Na: nNa = 0,9 (mol)
Bảo toàn Al: nAl = 0,6 (mol)
=> m = 0,9.23 + 0,6.27 = 36,9 (g)
Y chứa NaOH, NaAlO2
Gọi số mol NaOH, NaAlO2 trong mỗi phần là x, y (mol)
TN1:
nHCl=0,1.1=0,1(mol)nHCl=0,1.1=0,1(mol)
PTHH: NaOH + HCl --> NaCl + H2O
0,1<----0,1
=> x = 0,1 (mol)
TN3: nHCl = 0,75.1 = 0,75 (mol)
PTHH: NaOH + HCl --> NaCl + H2O
0,1--->0,1
NaAlO2 + HCl + H2O --> NaCl + Al(OH)3
y------>y------------------------>y
Al(OH)3 + 3HCl --> AlCl3 + 3H2O
0,65−y30,65−y3<-(0,65-y)
=> nAl(OH)3(3)=y−0,65−y3=4y−0,653(mol)nAl(OH)3(3)=y−0,65−y3=4y−0,653(mol)
TN2: nHCl=1.0,45=0,45(mol)nHCl=1.0,45=0,45(mol)
- Nếu kết tủa không bị hòa tan:
PTHH: NaOH + HCl --> NaCl + H2O
0,1--->0,1
NaAlO2 + HCl + H2O --> NaCl + Al(OH)3
0,35<--0,35-------------------->0,35
Điều kiện: y ≥≥ 0,35
=> nAl(OH)3(2)=0,35(mol)nAl(OH)3(2)=0,35(mol)
Do nAl(OH)3(2)=3.nAl(OH)3(3)nAl(OH)3(2)=3.nAl(OH)3(3)
=> 0,35=4y−0,650,35=4y−0,65
=> y = 0,25 (Loại)
=> Kết tủa bị hòa tan 1 phần
PTHH: NaOH + HCl --> NaCl + H2O
0,1--->0,1
NaAlO2 + HCl + H2O --> NaCl + Al(OH)3
y---->y------------------------->y
Al(OH)3 + 3HCl --> AlCl3 + 3H2O
0,35−y30,35−y3<--(0,35-y)
=> nAl(OH)3(2)=y−0,35−y3=4y−0,353(mol)nAl(OH)3(2)=y−0,35−y3=4y−0,353(mol)
Do nAl(OH)3(2)=3.nAl(OH)3(3)nAl(OH)3(2)=3.nAl(OH)3(3)
=> 4y−0,353=4y−0,654y−0,353=4y−0,65
=> y = 0,2
Vậy trong Y chứa {NaOH:0,3(mol)NaAlO2:0,6(mol){NaOH:0,3(mol)NaAlO2:0,6(mol)
Bảo toàn Na: nNa = 0,9 (mol)
Bảo toàn Al: nAl = 0,6 (mol)
=> m = 0,9.23 + 0,6.27 = 36,9 (g)