
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

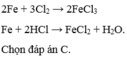

Bài 1)
Mg(OH)2 + H2SO4 => MgSO4 + 2H20
Bài 2)
sinh ra dd ko màu thì chỉ có Al2O3 thôi
Bài 3)
MgO + 2HNO3 => Mg(NO3)2 + H2O
Bài 4)
phương pháp hóa học
+ lấy hh Fe, Cu tác dụng với HCl
Fe +2 HCl => FeCl2 + H2
+ còn đồng ko tác dụng dc với HCl : ta lọc đồng ra khỏi hh òi phơi khô. Ta giả định cho đồng là 4g => mFe = 6g
% Cu = 4*100/10 = 40(%)
% Fe = 100- 40= 60 (%)
phương pháp vật lý
dùng nam châm hút sắt ra khỏi hỗn hợp. Ta có mFe là 6g => m Cu = 4 (g)
% Cu = 4*100/10 = 40(%)
% Fe = 100-40 = 60(%)

Kim loại nào sau đây tác dụng với dung dịch HCl loãng và tác dụng với khí Cl2 cho cùng loại muối clorua kim loại ?
A. Fe B. Zn C. Cu D.Ag
Hướng dẫn giải:
- Kim loại Zn tác dụng với dung dịch HCl loãng và với khi clo cho cùng loại muối clorua kim loại.
Zn + 2HCl → ZnCl2 + H2
Zn + Cl2 t∘→→t∘ ZnCl2
- Kim loại sắt tác dụng với dung dịch HCl loãng và khí clo cho hai loại muối clorua khác nhau là FeCl2 và FeCl3.
Fe + 2HCl → FeCl2 + H2↑
2Fe + 3Cl2 t∘→→t∘ 2FeCl3
Ag, Cu không tác dụng với dung dịch HCl
- Kim loại Zn tác dụng với dung dịch HCl loãng và với khí clo cho cùng loại muối clorua kim loại.
Zn + 2HCl \(\rightarrow\) ZnCl2 + H2.
Zn + Cl2 \(\rightarrow\) ZnCl2.
- Kim loại sắt tác dụng với dung dịch HCl loãng và khí clo cho 2 loại muối clorua khác nhau là FeCl2 và FeCl3.
Fe + 2HCl \(\rightarrow\)FeCl2 + H2.
2Fe + 3Cl2 \(\rightarrow\) 2FeCl3.
Ag, Cu không tác dụng với dung dịch HCl.

nBr2=0,05 mol
SO2 + Br2 + H2O =>H2SO4 +2HBr
0,05 mol<=0,05 mol
Chỉ có Cu pứ vs H2SO4 đặc nguội
Cu =>Cu+2 +2e
0,05 mol<= 0,1 mol
S+6 +2e =>S+4
0,1 mol<=0,05 mol
=>nCu=0,05 mol=>mCu=3,2g
=>mAl=5,9-3,2=2,7g
=>nAl=0,1 mol
Tổng nhh cr=0,1+0,05=0,15 mol

a,khối lượng của Cl là : 20,75-10,1=10,65
số mol của Cl- trong muối là : 10,65 /35,5=0,3 mol Nguyên tử khối trung bình của hai kim loại là: 10,1/0,3=33,67 suy ra hai kim loại là: Na(23);K(39) b,n Cl=nHCl =0,3 mol suy ra: khối lượng của HCl là: 0,3x 36,5= 10,95 g
Trần Hữu Tuyển ; Hồ Hữu Phước ; duy Nguyễn ; Hoàng Thảo Linh ; Nguyễn Trần Duy Thiệu ; Thảo Nguyễn Karry ; Trương Tuyết Nhi ; Lê Đình Thái ; Anh Ngốc ; lê thị hương giang các bạn giúp mình với

Gọi số mol của NO2 và NO là a và b
Ta có hệ phương trình :
\(\left\{{}\begin{matrix}a+b=\frac{1,12}{22,4}\\\frac{46a+30b}{a+b}=16,75.2\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}a=0,01\\b=0,04\end{matrix}\right.\)
\(n_{HNO3}=n_{HNO3_{tao.muoi}}+n_{N\left(pu.khử\right)}=2n_{NO2}+4n_{NO}\)
\(=0,18\left(mol\right)\)
\(\Rightarrow CM_{HNO3}=0,65M\)
\(m_{muoi}=m_{pu}+m_{NO3}=\left(6,25-2,516\right)+\left(0,01.1+0,04.3\right).62\)
\(=11,794\left(g\right)\)

1.
a)
- Cho quỳ tím vào các dung dịch
Quỳ tím chuyển thành màu đỏ : HCl , HNO3 (nhóm 1 )
Quỳ tím chuyển thành màu xanh : KOH , Ba(OH)2 ( nhóm 2 )
Quỳ tím không xảy ra hiện tượng : NaCl và NaNO3 (nhóm 3 )
*Cho AgNO3 vào ( nhóm 1 ) ta được :
Kết tủa trắng : HCl
\(AgNO3+HCl\rightarrow AgCl\downarrow+HNO3\)
Không xảy ra hiện tượng : HNO3
*Cho AgNO3 vào (nhóm 3) ta được :
Kết tủa trắng : NaCl
\(NaCl+AgNO_3\rightarrow NaNO_3+AgCl\downarrow\)
Không xảy ra hiện tượng :NaNO3
*Cho H2SO4 vào ( nhóm 2) ta được :
Kết tủa trắng : Ba(OH)2
\(Ba\left(OH\right)_2+H_2SO_4\rightarrow BaSO_4\downarrow+2H_2O\)
Không xảy ra hiện tượng : KOH
b)
- Cho quỳ tím vào các dung dịch
Quỳ tím chuyển thành màu đỏ : HCl , H2SO4 (nhóm 1)
Quỳ tìm chuyển thành màu xanh : NaOH
Không xảy ra hiện tượng :NaCl , NaBr ; NaI (nhóm 2)
*Cho AgNO3 vào (nhóm 1) ta được
Kết tủa trắng HCl
\(AgNO_3+HCl\rightarrow AgCl\downarrow+HNO_3\)
Không xảy ra hiện tượng H2SO4
Cho AgNO3 vào (nhóm 3) ta được
Kết tủa trắng là : NaCl
\(NaCl+AgNO_3\rightarrow AgCl\downarrow+NaNO_3\)
Chuyển thành màu vàng nhạt là :NaBr
\(AgNO3+NaBr\rightarrow AgBr\downarrow+NaNO_3\)
Chuyển thành màu vàng : NaI
\(AgNO_3+NaI\rightarrow AgI\downarrow+NaNO_3\)
2.
Cho hỗn hợp X vào HCl chỉ có Fe phản ứng:
\(Fe+2HCl\rightarrow FeCl_2+H_2\)
Ta có: \(n_{H2}=\frac{0,448}{22,4}=0,02\left(mol\right)=n_{Fe}\)
Cho X tác dụng với Cl2
\(2Fe+3Cl_2\rightarrow2FeCl_3\)
\(Cu+Cl_2\rightarrow CuCl_2\)
\(\rightarrow n_{FeCl3}=n_{Fe}=0,02\left(mol\right)\)
\(\rightarrow m_{FeCl3}=0,02.\left(56+35,5.3\right)=3,25\left(g\right)\)
\(m_{CuCl2}=7,3-3,25=4,05\left(g\right)\)
\(\rightarrow n_{CuCl2}=\frac{4,05}{64+35,5.2}=0,03\left(mol\right)=n_{Cu}\)
\(\rightarrow m=m_{Fe}+m_{Cu}=0,02.56+0,03.64=3,04\left(g\right)\)
3.
Gọi số mol Al là x; Fe là y
\(\rightarrow27x+56y=8,3\left(g\right)\)
\(Al+3HCl\rightarrow AlCl_3+\frac{3}{2}H_2\)
\(Fe+2HCl\rightarrow FeCl_2+H_2\)
\(\rightarrow n_{H2}=1,5n_{Al}+n_{Fe}=1,5x+y=\frac{5,6}{22,4}=0,25\left(mol\right)\)
Giải được \(x=y=0,1\)
\(\rightarrow m_{Al}=0,1.27=2,7\left(g\right)\)
\(\rightarrow\%m_{Al}=\frac{2,7}{8,3}=32,5\%\rightarrow\%m_{Fe}=100\%-32,5\%=67,5\%\)
Ta có muôí gồm AlCl3 và FeCl2
\(\rightarrow m_{muoi}=0,1.\left(27+35,5.3\right)+0,1.\left(56+35,5.2\right)=20,05\left(g\right)\)
b) Ta có: nHCl phản ứng=2nH2=0,5 mol
\(n_{HCl_{tham.gia}}=0,5.120\%=0,6\left(mol\right)\)
\(\rightarrow V_{HCl}=\frac{0,6}{1}=0,6\left(l\right)\)

Dung dịch Y gồm Al3+ (a mol), Fe2+ (b mol) —> Cl- (3a + 2b mol).
mX = 27a + 56b + 2,4 = 16,2.
ne = b + (3a + 2b) = 0,21.5.
—> a = 0,2 và b = 0,15.
—>%Fe=\(\dfrac{\text{(56b+2,4})}{16,2}\)=66,67