Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

$a)PTHH:2Al+6HCl\to 2AlCl_3+3H_2$
$n_{H_2}=\dfrac{5,04}{22,4}=0,225(mol)$
$\Rightarrow n_{Al}=0,15(mol)$
$\Rightarrow \%m_{Al}=\dfrac{0,15.27}{9,45}.100\%\approx 42,86\%$
$\Rightarrow \%m_{Cu}=100-42,86=57,14\%$
$b)$ Theo PT: $n_{HCl}=2n_{H_2}=0,45(mol)$
$\Rightarrow C_{M_{HCl}}=\dfrac{0,45.110\%}{0,5}=0,99M$

\(Mg + H_2SO_4 \to MgSO_4 + H_2\\ 2Al + 3H_2SO_4 \to Al_2(SO_4)_3 + 3H_2\\ Zn + H_2SO_4 \to ZnSO_4 + H_2\\ n_{H_2} = n_{H_2SO_4} = a(mol)\\ \text{Bảo toàn khối lượng : }\\ 20 + 98a = 58,4 + 2a\\ \Rightarrow a = 0,4\\ \Rightarrow V_1 = \dfrac{0,4}{0,5} = 0,8(lít) = 800(ml)\\ V_2 = 0,4.22,4 = 8,96(lít)\)

Trong G dùng phương pháp đường chéo
ta được
NO2 ( amol) 13,42
30,58
N2O4 ( b mol) 2,58 ( thêm mũi tên chỉ xuống chỉ lên hộ)
Ta có:
a:b = 1:1 và a + b =0,06
=> a = b =0,03
Theo định luật bảo toàn electron
\(n_{enhận}=0,09\left(mol\right)\Rightarrow n_M=\dfrac{0,09}{n}\)
\(\Rightarrow M=18,67n\) khi n = 3
thì M là 56 ( M là Fe)
-Oxit sắt có chứa 27,59% oxi nên đó là Fe3O4
- cho Zn vào dd B , xảy ra pứ:
\(4Zn+NO^-_3+7OH^-\rightarrow4ZnO_4^-+NH_3+2H_2O\left(1\right)\)
Và : \(Zn+2OH^-\rightarrow ZnO^{2-}_2+H_2\left(2\right)\)
=> nZn = 0,37 (mol)
Theo định luật bảo toàn:
nNH3 = 0,09 => nZn (1)
= 0,36 (mol) ; nZn (2) = 0,01 (mol)
=> nH2 = 0,01 (mol) , VH2 = 2,24 (lít)

Ta có: \(m_{H_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\) \(\Rightarrow m_{H_2}=0,2\cdot2=0,4\left(g\right)\)
\(\Rightarrow m_{dd\left(sau.pư\right)}=m_{hh}+m_{ddH_2SO_4}-m_{H_2}=309,6\left(g\right)\)
\(\Rightarrow a=309,6-300=9,6\left(g\right)\)
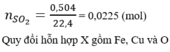
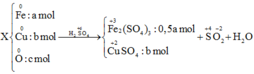
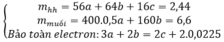
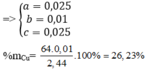






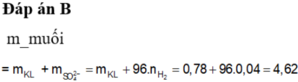
V H2 = 2,24 lít nhé
Chì không tan trong H2SO4 loãng
\(\text{Fe + H2SO4 → FeSO4 + H2↑}\)
nH2 =\(\frac{2,24}{22,4}\) = 0,1 mol
\(\text{nFe = nH2 = 0,1 mol}\)
mPb + mFe = 26,3g
→ mPb =\(\text{ 26,3 - 0,1 . 56 = 20,7(g)}\)
nPb = \(\text{20,7 : 207 = 0,1 mol}\)
Bảo toàn nguyên tố Pb:\(\text{ nPb = nPbO = 0,1 mol}\)
mhh = mFexOy + mPbO
→ mFexOy =\(\text{ 29,5 - 0,1 . 223 = 7,2(g)}\)
mFexOy = mFe + mO trong FexOy
→mO trong FexOy = \(\text{7,2 - 0,1 . 56 = 1,6(g)}\)
nO trong FexOy = \(\text{1,6 : 16 = 0,1 mol}\)
Ta có:
\(\text{x : y = nFe : nO = 0,1 : 0,1 = 1 : 1 }\)
→ CTHH của oxit: FeO
Coi lại đề giúp mk đc k