Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

1)
- Xét phần 1:
\(n_{H_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
PTHH: Fe + 2HCl --> FeCl2 + H2
0,2<-------------------0,2
=> nFe = 0,2 (mol)
- Xét phần 2:
\(n_{SO_2}=\dfrac{13,44}{22,4}=0,6\left(mol\right)\)
PTHH: 2Fe + 6H2SO4 --> Fe2(SO4)3 + 3SO2 + 6H2O
0,2-->0,6-------->0,1--------->0,3
Cu + 2H2SO4 --> CuSO4 + SO2 + 2H2O
0,3<----0,6<------0,3<-----0,3
=> nCu = 0,3 (mol)
m = 2.(0,2.56 + 0,3.64) = 60,8 (g)
2)
\(m_{H_2SO_4\left(bđ\right)}=\dfrac{200.98}{100}=196\left(g\right)\)
=> \(m_{H_2SO_4\left(sau.pư\right)}=196-98\left(0,6+0,6\right)=78,4\left(g\right)\)
mdd sau pư = \(\dfrac{60,8}{2}+200-0,6.64=192\left(g\right)\)
\(\left\{{}\begin{matrix}C\%_{\left(Fe_2\left(SO_4\right)_3\right)}=\dfrac{0,1.400}{192}.100\%=20,83\%\\C\%_{\left(CuSO_4\right)}=\dfrac{0,3.160}{192}.100\%=25\%\\C\%_{\left(H_2SO_4.dư\right)}=\dfrac{78,4}{192}.100\%=40,83\%\end{matrix}\right.\)

Câu 1 :
\(n_{H_2SO_4}=0.2\cdot0.1=0.02\left(mol\right)\)
\(n_{KOH}=0.3\cdot0.1=0.03\left(mol\right)\)
\(2KOH+H_2SO_4\rightarrow K_2SO_4+2H_2O\)
\(2..............1\)
\(0.03............0.02\)
Lập tỉ lệ : \(\dfrac{0.03}{2}< \dfrac{0.02}{1}\) \(\Rightarrow H_2SO_4dư\)
\(n_{K_2SO_4}=\dfrac{0.03}{2}=0.015\left(mol\right)\)
\(n_{H_2SO_{4\left(dư\right)}}=0.02-0.015=0.005\left(mol\right)\)
\(V_{ddX}=0.2+0.3=0.5\left(l\right)\)
\(C_{M_{K_2SO_4}}=\dfrac{0.015}{0.5}=0.03\left(M\right)\)
\(C_{M_{H_2SO_4\left(dư\right)}}=\dfrac{0.005}{0.5}=0.01\left(M\right)\)
Câu 2 :
\(n_{H_2}=\dfrac{0.672}{22.4}=0.03\left(mol\right)\)
Hai kim loại ở 2 chu kỳ liên kết thuộc nhóm IA => Đặt CT chung là : M
\(M+H_2O\rightarrow MOH+\dfrac{1}{2}H_2\)
\(0.06............................0.03\)
\(M_M=\dfrac{0.6}{0.06}=10\)\(\Rightarrow9< 10< 23\)
Hai kim loại là : Li và Na
\(n_{Li}=a\left(mol\right),n_{Na}=b\left(mol\right)\)
\(m_{hh}=9a+23b=0.6\left(g\right)\left(1\right)\)
\(n_{H_2}=0.5a+0.5b=0.03\left(mol\right)\left(2\right)\)
\(\left(1\right),\left(2\right):a=0.056,b=0.004\)
\(\%m_{Li}=\dfrac{0.056\cdot9}{0.6}\cdot100\%=84\%\)
\(\%m_{Na}=100-84=16\%\)

a, \(n_{Fe}=\dfrac{16,8}{56}=0,3\left(mol\right)\)
BT e, có: 3nFe = 2nSO2 ⇒ nSO2 = 0,45 (mol)
⇒ VSO2 = 0,45.22,4 = 10,08 (l)
b, BTNT Fe, có: nFe(OH)3 = nFe = 0,3 (mol)
⇒ mFe(OH)3 = 0,3.107 = 32,1 (g)

Đáp án B
Xét giai đoạn m gam Fe tác dụng với dung dịch H2SO4 loãng:
Sơ đồ phản ứng :
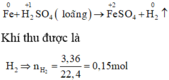
Các quá trình nhường, nhận electron :
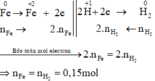
Xét giai đoạn m gam Fe tác dụng với H2SO4 đặc, nóng , dư:
Sơ đồ phản ứng:
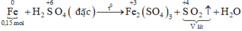
Các quá trình nhường, nhận electron:
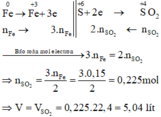

Các PTHH :
2Al + 3 H 2 SO 4 → Al 2 SO 4 3 + 3 H 2 (1)
2Al + 6 H 2 SO 4 → Al 2 SO 4 3 + 3 SO 2 + 6 H 2 O (2)
Cu + 2 H 2 SO 4 → Cu SO 4 + 2 H 2 O + SO 2 (3)
Theo PTHH (1) số mol Al tham gia phản ứng bằng 2/3 số mol H 2 => Khối lượng AI trong hỗn hợp : 2×2/3×0,06×27 = 2,16(g)
Số mol SO 2 được giải phóng bởi Al: 2,16/27 x 3/2 = 0,12 mol
Theo PTHH (2) và (3) số mol SO 2 giải phóng bởi Cu : 2.0,1 - 0,12 = 0,08 (mol)
Theo PTHH (3) khối lượng Cu trong hỗn hợp : 0,08. 64 = 5,12 (g)
Vậy m = 2,16 + 5,12 = 7,28 (g).





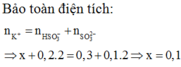

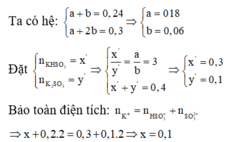
\(n_{H_2}=\dfrac{3,136}{22,4}=0,14\left(mol\right)\)
PTHH: Fe + H2SO4 --> FeSO4 + H2
0,14<--0,14<------------0,14
=> mFe = 0,14.56 = 7,84 (g)
\(C_{M\left(H_2SO_4\right)}=\dfrac{0,14}{0,2}=0,7M\)
\(n_{H_2}=\dfrac{3,136}{22,4}=0,14\left(mol\right)\)
PTHH: Fe + H2SO4 ---> FeSO4 + H2
0,14<-0,14<-------------------0,14
\(\rightarrow\left\{{}\begin{matrix}m=0,14.56=7,84\left(g\right)\\C_{M\left(H_2SO_4\right)}=\dfrac{0,14}{0,2}=0,7M\end{matrix}\right.\)