Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.
Khí metan CH4 có trong khí tự nhiên hoặc trong khí bioga. Khí metan cháy trong không khí sinh ra khí cacbon đioxit và nước:
CH4 + 2O2
#Hỏi cộng đồng OLM
#Mẫu giáo

a) Theo phương trình hóa học, ta thấy nếu đốt cháy hết 1 mol phân tử khí CH4 thì phải cần 2 mol phân tử khí O2 . Do đó thể tích khí oxi cần dùng để đốt cháy hoàn toàn 2 lít khí metan là:
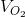 = 2 . 2 = 4 lít
= 2 . 2 = 4 lít
b) Theo phương trình phản ứng, khi đốt cháy hoàn toàn 0,15 mol khí metan thì cũng sinh ra 0,15 mol khí cacbon đioxit. Do đó thể tích khí CO2 thu được là:
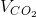 = 0,15 . 22,4 = 3,36 lít
= 0,15 . 22,4 = 3,36 lít
c) Tỉ khối của khí metan và không khí là:
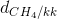 =
= 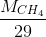 =
= 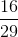 ≈ 0,55
≈ 0,55
Vậy khí metan nhẹ hơn không khí 0,55

Chọn C
Bảo toàn O : 2nO2 = 2nCO2 + nH2O => nO2 = 0,625 mol
=> nkk = 5nO2 = = 3,125 mol => Vkk = 70 lit

Gọi x, y tương ứng là số mol của CH4 và O2. Khối lượng trung bình của A = 12.2 = 24. Suy ra: 16x + 32y = 24(x + y). Thu được x = y.
Trong cùng đk về nhiệt độ và áp suất thì % về thể tích cũng chính là % về số mol. Do đó, mỗi khí chiếm 50% thể tích trong A.

Gọi CT của A là CxHyO2.
CxHyO2 + (x+y/4 - 1)O2 ---> xCO2 + y/2H2O
Trong 3,7 gam khí A, có số mol = 1,6/32 = 0,05 mol. Do đó phân tử khối của A = 3,7/0,05 = 74. Do đó: 12x + y = 74 - 32 = 42.
Mặt khác số mol của CO2 = 6,6/44 = 0,15 mol; số mol H2O = 2,7/18 = 0,15 mol = số mol CO2. Dựa vào pt phản ứng ta có: y = 2x.
Giải hệ 2 pt trên thu được x = 3; y = 6. CT của A: C3H6O2.
Số mol A = 1/3 số mol CO2 = 0,05 mol. Suy ra m = 74.0,05 = 3,7 g.

a) Phương trình hóa học của S cháy trong không khí:
S + O2 → SO2
b. Số mol của S tham gia phản ứng:
nS = = 0,05 mol
Theo phương trình hóa học, ta có: = nS =
= 0,05 mol
=> Thể tích khí sunfurơ sinh ra ở đktc là:
= 22,4 . 0,05 = 1,12 lít
Tương tự thể tích khí oxi cần dùng ở đktc là:
= 22,4 . 0,05 = 1,12 lít
Vì khí oxi chiếm 1/5 thể tích của không khí nên thể tích không khí cần là:
=> Vkk = 5 = 5 . 1,12 = 5,6 lít

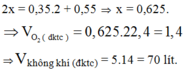
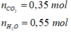



2l hay 2g vậy?
a) Nếu là 2 mol khí metan thì số mol O2 = 4 mol và thể tích V = 4.22,4 = 89,6 lít.
b) số mol CO2 = số mol CH4 = 0,15 mol. V = 0,15.22,4 = 3,36 lít.
c) Khí metan nhẹ hơn kk = 16/29 = 0,55 lần.