Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án A
(b) Sai, Nhỏ từ từ dung dịch H2SO4 loãng vào dung dịch K2Cr2O7 loãng thì màu của dung dịch không có sự thay đổi màu sắc vì phản ứng trên không xảy ra.
(d) Sai, Sục khí H2S đến dư vào dung dịch sắt(II) clorua không thấy hiện tượng gì vì phản ứng trên không xảy ra.
(e) Sai, Nhỏ từ từ đến dư dung dịch HCl vào dung dịch Na2CO3, ban đầu không có hiện tượng sau đó sủi bọt khí không màu

Chọn C
(b) Sai, Nhỏ từ từ dung dịch H2SO4 loãng vào dung dịch K2Cr2O7 loãng thì màu của dung dịch không có sự thay đổi màu sắc vì phản ứng trên không xảy ra.
(d) Sai, Sục khí H2S đến dư vào dung dịch sắt(II) clorua không thấy hiện tượng gì vì phản ứng trên không xảy ra.
(e) Sai, Nhỏ từ từ đến dư dung dịch HCl vào dung dịch Na2CO3, ban đầu không có hiện tượng sau đó sủi bọt khí không màu.

Đáp án B
Cho CrO3 vào dung dịch NaOH dư, thu được dung dịch X gồm Na2CrO4 và NaOH dư
Cho H2SO4 dư vào X thu được dung dịch Y gồm Na2Cr2O7, Na2SO4, H2SO4 dư
(a) Sai, Dung dịch X có màu vàng.

Chọn đáp án D
pV = nRT với p = 1atm; V = 3,813 lít; R = 0,082; T = 273 + 27 = 300K.
khí hóa nâu ngoài không khí là NO ⇒ thay số có nNO = 0,155 mol.
Ø phản ứng xảy ra hoàn toàn nên Fe sẽ lên Fe3+ trong muối Fe(NO3)3.
Bảo toàn electron có: 3nFe + nFeO = 3nNO = 0,465 mol.
Lại có: mFe + mFeO = 9,48 gam ||⇒ giải nFe = 0,15 mol; nFeO = 0,015 mol.
⇒ ∑nFe(NO3)3 = 0,165 mol ⇒ bảo toàn N có ∑nHNO3 cần = 0,65 mol.
⇒ VHNO3 = 0,65 ÷ 0,5 = 1,3 lít ⇋ 1300 mL. Chọn đáp án D

ĐÁP ÁN C
Dd Y chứa ion sắt. Do Y phản ứng được với Cu nên y chứa Fe3+ Do Y làm mất màu dd KMnO4 => y chứa Fe2+
=> X phải là Fe3O4


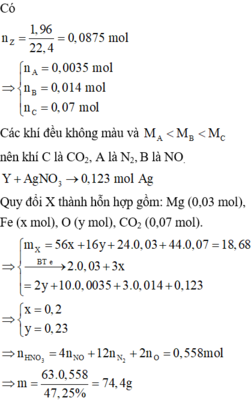


Đáp án A
Phương trình phản ứng:
CuO + 2HNO3 → Cu(NO3)2 + H2O
Dung dịch thu được có màu xanh