Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Ta có: P = E (Do nguyên tử trung hòa về điện)
- Tổng số hạt cơ bản trong M2X là 116.
⇒ 2.2PM + 2NM + 2PX + NX = 116 (1)
- Trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 36.
⇒ 2.2PM + 2PX - 2NM - NX = 36 (2)
- Khối lượng nguyên tử của X lớn hơn M là 9.
⇒ PX + NX - PM - NM = 9 (3)
- Tổng số hạt trong X2- nhiều hơn trong M+ là 17.
⇒ 2PX + NX + 2 - (2PM + NM - 1) = 17 (4)
Từ (1), (2), (3) và (4) \(\Rightarrow\left\{{}\begin{matrix}P_M=11\\N_M=12\\P_X=16\\N_X=16\end{matrix}\right.\)
⇒ AM = 11 + 12 = 23
AX = 16 + 16 = 32

Hợp chất M2X gồm 2 nguyên tử M và 1 nguyên tử X nên tổng số hạt là
2(2ZM + NM) + (2ZX + NX) = 116
Trong 116 hạt đó, số hạt mang điện nhiều hơn không mang điện là 36:
(2.2ZM + 2ZX) – (2NM + NX) = 36
Khối lượng nguyên tử X nhiều hơn M là 9:
ZM + NM + 9 = ZX + NX
Tổng số hạt p, n, e trong X2- nhiều hơn trong M+ là 17:
(2ZM + NM – 1) + 17 = 2ZX + NX + 2
Giải hệ trên được:
ZM = 11 (Na)
NM = 12
ZX = 16 (S)
NX = 16
Số khối của Na = ZM + NM = 23
Số khối của S = ZX + NX = 32

_Tổng số hạt trong M2X là 140:
=>2[2P(M) + N(M)] + 2P(X) + N(X) = 140
<=>4P(M) + 2P(X) + 2N(M) + N(X) = 140(1)
_Số hạt mang điện nhiều hơn không mang điện là 44:
=>4P(M) + 2P(X) - [2N(M) + N(X)] = 44(2)
_Số khối của M{+} nhiều hơn X{2-} là 23:
=>P(M) + N(M) - [P(X) + N(X)] = 23
<=>P(M) - P(X) + N(M) - N(X) = 23(3)
_Tổng số hạt trong M{+} nhiều hơn trong X{2-} là 31:
=>2P(M) + N(M) - 1 - [2P(X) + N(X) + 2] = 31
<=>2[P(M) - P(X)] + N(M) - N(X) = 34(4)
Lấy (1) + (2):
=>8P(M) + 4P(X) = 184(5)
Lấy (4) - (3):
=>P(M) - P(X) = 11(6)
Từ(5)(6) => P(M) = 19 ; P(X) = 8
Vậy M là kali(K) , X là oxi(O)
=>M2X là K2O.

Tổng số các hạt trong phân tử là 140 → 2ZM + NM + 2.(2ZX + NX ) = 140 (1)
Số hạt mang điện nhiều hơn số hạt không mang điện là 44 hạt → 2ZM + 4ZX - NM- 2.NX = 44 (2)
Giải hệ (1), (2) → 2ZM + 4ZX= 92 và NM + 2NX = 48
Tổng số hạt cơ bản trong X nhiều hơn trong M là 16 hạt→ 2ZX + NX - (2ZM + NM) = 16 (3)
Số khối của X lớn hơn số khối của M là 11 → (ZX + NX)- (ZM + NM) = 11 (4)
Lấy (3) - (4) → ZX - ZM = 5
Ta có hệ:
2ZM+4ZX=92
−ZM+ZX=5
⇒ZM=12
ZX=17
M là Mg và X là Cl
Vậy công thức của MX2 là MgCl2.

Gọi Z,N,E,Z',N',E' lần lượt là số p, n, e có trong nguyên tử M và X ta có
Trong phân tử có tổng số hạt p, n, e là 140:
2(Z+E+N)+Z'+E+N' = 2(2Z+N)+2Z'+2N' = 44 (1)
Số hạt mang điện nhiều hơn số hạt không mang điện là 44 hạt:
2(Z+E)+Z'+E'-2N-N' = 4Z+2Z'-2N-N' = 44 (2)
Số khối của M lớn hơn số khối của X là 23: Z+N-Z'-N' = 23 (3)
Tổng số hạt p, n, e trong nguyên tử M nhiều hơn trong nguyên tử X là 34 hạt:
2Z+N-2Z'-N = 34 (4)
Từ (1); (2); (3); (4) ta có:
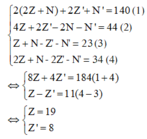
M là Kali và X là O
Vậy công thức phân tử cần tìm là K2O
Đáp án A

Ta có: P = E (Do nguyên tử trung hòa về điện)
- Trong MX3 có tổng số hạt p, e, n là 196.
⇒ 2PM + NM + 3.2PX + 3NX = 196 (1)
- Trong đó, số hạt mang điện nhiều hơn số hạt không mang điện là 60.
⇒ 2PM + 3.2PX - NM - 3NX = 60 (2)
- Khối lượng nguyên tử X lớn hơn M là 8.
⇒ PX + NX - PM - NM = 8 (3)
- Tổng số hạt trong X- nhiều hơn trong M3+ là 16.
⇒ 2PX + NX + 1 - (2PM + NM - 3) = 16 (4)
Từ (1), (2), (3) và (4) \(\Rightarrow\left\{{}\begin{matrix}P_M=13=Z_M\\N_M=14\\P_X=17=Z_X\\N_X=18\end{matrix}\right.\)
→ M là Al, X là Cl.
Vậy: CTHH cần tìm là AlCl3.
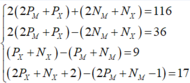
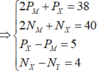
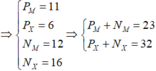
Gọi hóa trị của M là n
\(n_{H_2}=\dfrac{0,2479}{24,79}=0,01\left(mol\right);n_{M\left(OH\right)_n}=0,5.0,04=0,02\left(mol\right)\)
PTHH: \(2M+2nH_2O\rightarrow2M\left(OH\right)_n+nH_2\)
\(\dfrac{0,02}{n}\)<--------------\(\dfrac{0,02}{n}\)<--------0,01
\(M_2O_n+nH_2O\rightarrow2M\left(OH\right)_n\)
Theo PTHH: \(n_{M\left(OH\right)_n}=2n_{M_2O_n}+n_M\)
=> \(n_{M_2O_n}=\dfrac{0,02-\dfrac{0,02}{n}}{2}=0,01-\dfrac{0,01}{n}\left(mol\right)\)
=> \(\dfrac{0,01}{n}< 0,01\Leftrightarrow n>1\)
Do M là kim loại tan trong nước nên n = 2
=> \(n_M=\dfrac{0,02}{2}=0,01\left(mol\right)\)
\(\xrightarrow[]{\text{BTNT M}}n_{MO}=n_{M\left(OH\right)_2}-n_M=0,02-0,01=0,01\left(mol\right)\)
=> \(0,01.\left(M_M+16\right)+0,01.M_M=2,9\)
=> \(M_M=137\left(g/mol\right)\)
=> M là Barium (Ba)
M : x mol ; M2On : y mol
⇒ n M(OH)n = x + 2y = 0,02
+) n = 1 (KL kiềm ) ⇒ x = 0,02 ; y = 0 ⇒ loại
+) n = 2 (KL kiềm thổ) ⇒ x = 0,01 , y = 0,005
⇒ mhh = 0,01.M + 0,005.(2M + 16.2) = 2,9
⇒ M = Ba