Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Câu 1 :
M\(_A\)= 78 g
Do sản phẩm cháy gồm CO2 , H2O nên thành phần của A gồm C , H , có thể có O
Đặt CTPT của A : \(C_xH_yO_z\)
Áp dụng công thức : \(\dfrac{M_X}{m_X}=\dfrac{44x}{m_{CO2}}=\dfrac{9y}{m_{H2O}}\)
\(\Rightarrow\)x=6 , y=6
Với M\(_A\)= 78 \(\Rightarrow\) 12.6 + 6 + 16z = 78 \(\Rightarrow\) z=0
Vậy CTPT của A là C6H6
Câu 2 :
M\(_X\)= 59
Đặt CTPT của X là \(C_xH_yO_zN_t\)
Áp dụng công thức : \(\dfrac{M_X}{m_X}=\dfrac{44x}{m_{CO2}}=\dfrac{y}{m_{H2O}}=\dfrac{11,2t}{V_{N_2}}\)
\(\dfrac{59}{0,295}=\dfrac{44x}{0,44}=\dfrac{y}{0,225}=\dfrac{11,2t}{0,0558}\)
\(\Rightarrow\)x=2 , y=5 , t=1
Với M\(_X\)= 59 \(\Rightarrow\)z=1
Vậy CTPT của X là C2H5ON

%O = 100- (60 + 13,33) = 26,67
Gọi công thức hóa học của A là C x H y O z
Ta có tỷ lệ: x : y : z = 60/12 : 13,33/1 : 26,67/16 = 5 : 13,33 : 1,67 = 3 : 8 : 1
Công thức của hợp chất là C 3 H 8 O n
Ta có: (12.3+1.8+16)n=60
⇔ 60n= 60 → n=1
Vậy công thức phân tử của C x H y O z là C 3 H 8 O

gọi công thức phân tử của hợp chất hữu cơ A là CXHYOZ
Ta có : %O =100-(60+ 13.33)=26.63%
Ta có ;
\(\frac{12x}{60}\)=\(\frac{y}{13.33}\)=\(\frac{16z}{26.67}\)=\(\frac{60}{100}\)= 0.6
do đó : x=\(\frac{60.0,6}{12}\)=3
y=0,6.13,33=8
z=\(\frac{26,67.0,6}{16}\)=1
vậy công thức phân tử của A là C3H8O.

Đặt CTPT : \(C_xH_yO_z\)
=> \(\%m_O=100-48,65-8,11=43,24\%\)
=> \(x:y:z=\frac{48,65}{12}:\frac{8,11}{1}:\frac{43,24}{16}=4:8:3\)
=>CTPT : \(C_4H_8O_3\)

Đáp án A
Thành phần % khối lượng của O = 100 – (52,17 + 13,04) = 34,79%
nC : nH : nO = 52,17/12 : 13,04 : 34,79/16 = 4,35 : 13,04 : 2,17 = 2: 6: 1
=> Công thức đơn giản nhất là C 2 H 6 O 2 .
M = (2x12+6+16)n = 46 => n =1
Vậy công thức phân tử: C 2 H 6 O 2

\(M_Z=\dfrac{5,05}{0,1}=50,5\left(g/mol\right)\)
\(m_{Cl}=\dfrac{50,5.70,3}{100}=35,5\left(g\right)\Rightarrow n_{Cl}=\dfrac{35,5}{35,5}=1\left(mol\right)\)
\(m_H=\dfrac{50,5.5,94}{100}=3\left(g\right)\Rightarrow n_H=\dfrac{3}{1}=3\left(mol\right)\)
\(m_C=50,5-35,5-3=12\left(g\right)\Rightarrow n_C=\dfrac{12}{12}=1\left(mol\right)\)
=> CTPT: CH3Cl
CTCT:




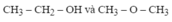


%O=100%-64,856%-13,51%=31,634%
%H=m\(_H\)/m\(_A\).100%
<--> m\(_H\)=%H.m\(_A\)/100=13,51.74/100=10g
-->số phân tử hiđrô là :10/1 = 10 phân tử
tương tự: m\(_C\)=64,865.74/100=48g(gần bằng)
--> số phân tử cacbon là:48/12=4 phân tử
tương tự:m\(_O\)=21,634.74/100=16g(gần bằng)
-->số phân tử O là:16/16=1 phân tử
vậy công thức phân tử của A là:\(C_4H_{10}O\)
kí tự / trong bài là thay cho dấu chia nha bn,chúc bn học tốt
Đặt CTPT của hợp chất A là CxHyOz
%m O = 100% - 64,865%-13,51% = 21,625%
Ta có : \(\dfrac{m_C}{\%m_C}=\dfrac{m_H}{\%m_H}=\dfrac{m_O}{\%m_O}=\dfrac{M_A}{100}\)
\(\Leftrightarrow\) \(\dfrac{12x}{64,865}\)= \(\dfrac{y}{13,51}\)= \(\dfrac{16z}{21,625}\) = \(\dfrac{74}{100}\)
\(\Leftrightarrow\) x = \(\dfrac{74.64,865}{12.100}\) = 4
y = \(\dfrac{74.13,51}{100}\) = 10
z = \(\dfrac{74.21,625}{16.100}\)= 1
Vậy CTPT của A là \(C_4H_{10}O\)