Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Chọn A
Quy đổi hỗn hợp X thành: Ba (x mol); K (y mol); Al (z mol) và O (t mol)
→ m O = 16t = (137x + 39y + 27z + 16t).10% → 13,7x + 3,9y + 2,7z - 14,4t = 0 (1).
Bảo toàn electron có: 2x + y + 3z = 2t + 0,056.2 → 2x + y + 3z – 2t = 0,112 (2)
Theo bài ra kết tủa gồm
BaSO
4
: x mol và
Al
(
OH
)
3
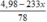 mol
mol
Dung dịch X gồm:
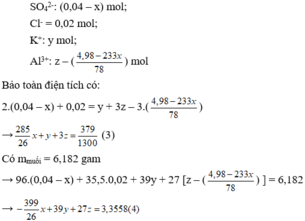
Từ (1); (2); (3) và (4) có x ≈ 0,012; y ≈ 0,076; z ≈ 0,03; t ≈ 0,036.
Vậy m = 0,012. 137 + 0,076.39 + 0,03.27 + 0,038.16 ≈ 6 (gam).

nH+=0,4+0,1.a
nNO3-=0,1a
bạn viết phương trình Mg+H+ +NO3- dưới dạng pt ion
H++NO3 ttuowng đương với HNO3 loãng
rồi bạn sử dụng phương pháp đường chéo, định luật bảo toàn nguyên tố và electron

Em moi hoc lop7 k the lam dc bai nay, nhung cj dat kl cua moi chat la x;y rồi viet pt hóa hoc, tim moi lien he x;y

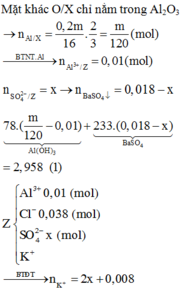
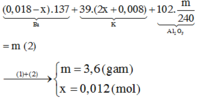

Chọn đáp án A