Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án A
A gồm CnH2nO2 a mol và CmH2m-2O2 b mol với m ≥3
⇒ muối CnH2n-1O2Na a mol và CmH2m-3O2Na b mol
nhh A = nNaOH phản ứng = 0,15 x 2 - 0,1 x 1 ⇒ a + b = 0,2 (1)
Rắn khan gồm: CnH2n-1O2Na a mol, CmH2m-3O2Na b mol và NaCl 0,1 mol
⇒ m chất rắn = a(14n+54) + b(14m+52) + 58,5 x 0,1 = 22,89 ⇒ 14(na+mb) + 2a = 6,64 (2)
Đốt cháy A ⇒ nCO2 = na + mb và nH2O = na + mb - b
Từ: mCO2 + mH2O = 44(na + mb) + 18(na + mb - b) = 26,7 ⇒ 62(na+mb) - 18b = 26,72 (3)
Từ (1), (2) và (3) ⇒ a = b = 0,1 và na + mb = 0,46 ⇒ n + m = 4,6
⇒ n = 1 và m = 3,6 ⇒ axit no HCOOH 0,1 mol hai axit không no là C3H4O2x mol và C4H6O2y mol
Trong đó: x + y = b = 0,1 và số nguyên tử C trung bình = 3,6
Bằng qui tắc đường chéo ⇒ x = 0,04 và y = 0,06
⇒ mA = 46 x 0,1 + 72 x 0,04 + 86x 0,06 = 12,64 gam ⇒ %mC3H4O2 = 22,78%

Đáp án A
Do các axit đơn chức nên ta có: nA = nNaOH pư = nNaOH bđ – nHCl = 0,3 – 0,1 = 0,2 mol
=> nO(A) = 2nA = 0,4 mol
nH2O sinh ra = nNaOH bđ = 0,3 mol
BTKL: mA + mNaOH bđ + nHCl = m chất rắn + mH2O
=> mA + 0,3.40 + 0,1.36,5 = 22,89 + 0,3.18 => mA = 12,64 (g)
Giả sử khi đốt cháy: nCO2 = x mol và nH2O = y mol
BTNT => nC(A) = x mol; nH(A) = 2y mol
+ m bình tăng = mCO2 + mH2O => 44x + 18y = 26,72 (1)
+ mA = mC + mH + mO => 12x + 2y + 0,4.16 = 12,64 (2)
Giải (1) và (2) được x = 0,46 và y = 0,36
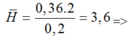 1 axit có 2H (do các axit không no có một nối đôi
1 axit có 2H (do các axit không no có một nối đôi
đơn chức có từ 4H trở đi)
=> A có chứa HCOOH
naxit không no = nCO2 – nH2O = 0,46-0,36 = 0,1 mol
=> nHCOOH = 0,2-0,1 = 0,1 mol
![]()
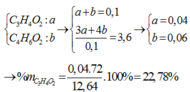

Đáp án D
nNaOH dư = 0,3(mol); nNaOH dư = nHCl = 0,l(mol)
=> nNaOH phản ứng = naxit = 0,2 (mol)
Gọi công thức chung của các axit là RCOOH
=> Cô cạn D thu được hỗn hợp muối gồm 0,2 mol RCOONa và 0,1 mol NaCl
m R C O O N a = 22 , 89 - 0 , 1 . 58 , 5 = 17 , 04 ( g )
Áp dụng phương pháp tăng giảm khối lượng ta có:
m R C O O N a = m a x i t + 22 n a x i t ⇒ m a x i t = 12 , 64 ( g )
Gọi số mol CO2 và H2O khi đốt cháy A lần lượt là x, y(mol)
Khi hấp thụ sản phẩm cháy vào dung dịch NaOH đặc thì khối lượng bình tăng chính là tổng khối lượng của CO2 và H2O => 44x + 18y = 26,72(g) (1)
Lại có: maxit = mC + mH + mO = 12 n C O 2 + 2 n H 2 O + 16n O trong axit
Vì axit đơn chức => nO trong axit = 2naxit = 0,4(mol)
=> 12,64 = 12x+2y+16.0,4 => 12x+2y = 6,24 (2)
(1) và (2) suy ra x = 0,46(mol); y = 0,36(mol)
Khi đốt cháy A ta thấy
n C O 2 - n H 2 O = n a x i t k h ô n g n o = 0 , 1 ( m o l ) ⇒ n a x i t n o = 0 , 1 ( m o l )
Vì axit không no có ít nhất 3 nguyên tử C trong phân tử
⇒ n C O 2 d o đ ố t c h á y a x i t k h ô n g n o > 0 , 3 ( m o l ) ⇒ n C O 2 d o đ ố t c h á y a x i t n o < 0 , 16 ( m o l )
=> axit không no chỉ có thể là HCOOH
⇒ n C O 2 d o đ ố t c h á y a x i t n o = 0 , 1 ( m o l ) ⇒ n C O 2 d o đ ố t c h á y a x i t k h ô n g n o = 0 , 36 ( m o l )
=> 2 axit không no là C2H3COOH và C3H5COOH.
Gọi số mol của chúng lần lượt là a,b(mol)
⇒ a + b = 0 , 1 3 a + 4 b = 0 , 36 ⇒...

Chất A có CTPT là C n H 2 n O 2 , CTCT là C n - 1 H 2 n - 1 C O O H Chất B có CTPT là C n H 2 n + 2 O , CTCT là C n H 2 n + 1 O H .
Phần (1):
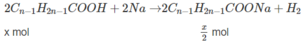
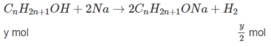
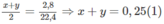
Phần (2) :
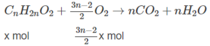
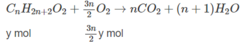
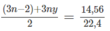
⇒ (3n − 2)x + 3ny = 1,3 (2)
Khối lượng mỗi phần : (14n + 32)x + (14n + 18)y = 12,9 (3)
Từ hệ các phương trình (1), (2), (3), tìm được n = 2; x = 0,1; y = 0,15.
Chất A: C 2 H 4 O 2 hay C H 3 C O O H (axit axetic) chiếm :
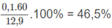
khối lượng hỗn hợp.
Chất B: C 2 H 6 O hay C H 3 - C H 2 - O H (ancol etylic) chiếm: 100% - 46,5% = 53,5% khối lượng hỗn hợp.

Đặt công thức chung của 2 axit là C n H 2 n + 1 C O O H
Phần 1 :
C n H 2 n + 1 C O O H + NaOH → C n H 2 n + 1 C O O N a + H 2 O
x mol x mol
(14 n + 68)x = 4,26 (1)
Phần 2 :
C n H 2 n + 1 C O O H + B a ( O H ) 2 → ( C n H 2 n + 1 C O O ) 2 B a + 2 H 2 O
x mol x 2 mol
(28 n + 227) x 2 = 6,08 (2)
Từ (1) và (2) tìm được n = 2,75; x = 0,04.
Axit thứ nhất là C 2 H 5 C O O H ( C 3 H 8 O 2 ) có số mol là a mol.
Axit thứ hai là C 3 H 7 C O O H ( C 4 H 8 O 2 ) có số mol là b mol.
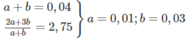
C
M
của
C
2
H
5
C
O
O
H
là: 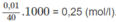
C
M
của
C
3
H
7
C
O
O
H
là: 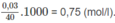

Khi đốt 0,5 mol hỗn hơp M, số mol C O 2 thu đươc là :
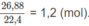
Nếu đốt 1 mol hỗn hợp M, số mol C O 2 thu được sẽ là 2,4 (mol).
Như vậy chất A và chất B có chứa trung bình 2,40 nguyên tử cacbon , chất A lại kém chất B 1 nguyên tử cacbon. Vậy, A có 2 và B có 3 nguyên tử cacbon.
A là ancol no có 2 cacbon: C 2 H 6 - x ( O H ) x hay C 2 H 6 O x
B là axit đơn chức có 3 cacbon: C 3 H y O 2 .
Đặt số mol A là a, số mol B là b :
a + b = 0,5 (1)
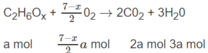
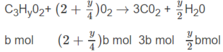
Số mol O 2 là: (3,5 - 0,5x)a + (2 + 0,25y)b = 1,35 (mol) (2)
Số mol C O 2 là: 2a + 3b = 1,2 (mol) (3)
Số mol C O 2 là:
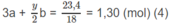
Giải hệ phương trình đại số tìm được: a = 0,3; b = 0,2; x = 2; y = 4.
Chất A:
C
2
H
6
O
2
hay 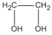 etanđiol (hay etylenglicol)
etanđiol (hay etylenglicol)
Chiếm  khối lượng M.
khối lượng M.
Chất B: C 3 H 4 O 2 hay C H 2 = C H - C O O H , axit propenoic chiếm 43,64% khối lượng M.

Số mol
C
O
2
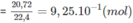
Khối lượng C trong đó là: 9,25. 1 - 1 .12= 11,1(g)
Đó cũng là khối lượng C trong 13,2 g hỗn hợp M.
Khối lượng H trong 13,2 g M là: 13,2 - 11,1 = 2,1 (g)
Số mol
H
2
O
tạo thành: 
Vì số mol H 2 O tạo thành > số mol C O 2 nên hai chất trong hỗn hợp M đều là ankan.
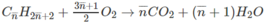
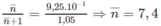
Công thức phân tử hai chất là C 7 H 16 (x mol) và C 8 H 18 (y mol).
Khối lượng hai chất là : 100x + 114y = 13,2.
Số mol C O 2 là : 7x + 8y = 9,25. 10 - 1
⇒ x = 0,75. 10 - 1 ; y = 0,5. 10 - 1 .
Thành phần phần trăm theo khối lượng:
C
7
H
16
chiếm: 
C 8 H 18 chiếm: 100% - 56,8% = 43,2%

Đặt công thức của 2 ancol là C n H 2 n + 1 O H
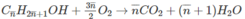
Theo phương trình:
(14
n
+ 18) g ancol tác dụng với 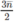 mol
O
2
mol
O
2
Theo đầu bài: 35,6 g ancol tác dụng với 2,850 mol O 2
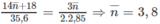
⇒ Hai ancol là C 3 H 7 O H (x mol) và C 4 H 9 O H (y mol)
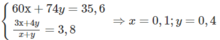
Từ đó tính được phần trăm khối lượng từng chất (như ở trên).

Giải thích: Đáp án B
mG = 23,02 + 0,46.40 – 0,46.18 = 33,14g
mO2 cần đốt cháy = 0,23.106 + 22,04 – 33,14 = 13,28g
=> nO2 = 0,415 mol
Bảo toàn O : nH2O + 2nCO2 = 1,06 mol
mCO2 + mH2O = 22,04g
=> nCO2 = 0,37 ; nH2O = 0,32 mol
Số C trung bình = (0,37 + 0,23)/0,46 = 1,3 => Y là HCOOH và Z là CH3COOH
=> nX = nCO2 – nH2O = 0,05 mol
=> Tổng số mol của Y và Z là 0,41 mol
0,41 < nCO2(Y,Z) < 0,41.2 = 0,82 mol
Nếu X có 3C => nCO2(Y,Z) = 0,45 mol (thỏa mãn)
Nếu X có 4C trở lên => nCO2(Y,Z) < 0,4 mol (không thỏa mãn)
=> X là C2H3COOH
Đặt nHCOOH = x ; nCH3COOH = y mol
=> x + 2y = 0,6 – 0,05.3
Và x + y = 0,41 mol
=> x = 0,37 ; y = 0,04 mol
=> mZ = 2,4g
Các axit đơn chức tác dụng với NaOH như sau :
RCOOH + NaOH → RCOONa + H 2 O
Cứ 1 mol RCOOH biến thành 1 mol RCOONa thì khối lượng tăng thêm: 23 - 1 = 22 (g).
Khi 29,6 g M biến thành hỗn hợp muối, khối lượng đã tăng thêm: 40,6 - 29,6= 11 (g).
Vậy số mol 3 axit trong 29,60 g M là :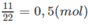
Khối lượng trung bình của 1 mol axit trong hỗn hợp là:
Vậy trong hỗn hợp M phải có axit có phân tử khối nhỏ hơn 59,2. Chất đó chỉ có thể là H-COOH. Nhưng M có 2 axit no kế tiếp nhau trong dãy đồng đẳng nên đã có HCOOH thì phải có C H 3 C O O H .
Giả sử trong 8,88 g M có x mol HCOOH, y mol C H 3 C O O H và z mol C n H 2 n - 1 C O O H :
2HCOOH + O 2 → 2 C O 2 + 2 H 2 O
x mol x mol
C H 3 C O O H + 2 O 2 → 2 C O 2 + 2 H 2 O
y mol 2y mol
x + 2y + (n + 1)z = 0,3 (3)
Cách giải hệ phượng trình :
Nhân 2 vế của phương trình (3) với 14 ta có
14x + 28y + (14n + 14)z = 4,2 (3’)
Lấy (2) trừ đi (3') :
32x + 32y + 30z = 4 68 (2')
Nhân (1) với 30 ta có:
30x + 30y + 30z = 4,50 (1')
Lấy (2') trừ đi (1'): 2x + 2y = 0,18 ⇒ x + y = 0,09 ⇒ z = 0,15 - 0,09 = 0,06
Thay các giá trị vừa tìm được vào phương trình (3), ta có :
0,09 + y + 0,06(n + 1) = 0,3
y = 0,15 - 0,06n
0 < y < 0,09 ⇒ 0 < 0,15 - 0,06n < 0,09
1 < n < 2,5
⇒ n = 2 ; y = 0,15 - 0,06.2 = 0,03 ⇒ x = 0,06.
Thành phần khối lượng của hỗn hợp:
H-COOH( C H 2 O 2 ) axit metanoic là:
C H 3 -COOH( C 2 H 4 O 2 ) axit etanoic là
C H 2 = CH-COOH( C 3 H 4 O 2 ) axit propenoic là: