Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Vì khối lượng của hỗn hợp trước và sau phản ứng là bằng nhau
=> n hh trước phản ứng : n hh sau phản ứng = 25 : 15 = 5 : 3
Coi tổng số mol trước phản ứng là 5 => tổng số mol sau phản ứng là 3 mol
Ta có khối lượng hỗn hợp là : 5 . 15 = 75 g
Ta có hệ :
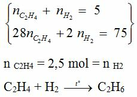
Ban đầu 2,5 2,5
Phản ứng x x
Kết thúc : 2,5 – x 2,5– x x
=> Tổng số mol sau phản ứng là : : 2,5 – x + 2,5– x + x = 5–x
=> 5 – x = 3 => x = 2 mol
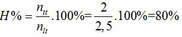

trong 1 mol hh ban đầu có nH2 =0,75 mol , nC2H4 =0,25 mol
nsau= 2,125.13/34=0,8125
=> nH2 pứ =ntrc -nsau =1- 0.8125=0,1875
=> H= 0,1875/0,75 .100= 25%

Gọi số mol $SO_2$ và $O_2$ lần lượt là 1 và 1 (Dựa theo tỉ khối hơi)
a, $2SO_2+O_2\rightarrow 2SO_3$
b, $\%V_{SO_2}=\%V_{O_2}=50\%$
Gọi số mol $SO_2$ phản ứng là a (mol)
Sau phản ứng hỗn hợp hơi thu được a mol $SO_3$; $1-0,5a$ mol $O_2$ và $1-a$ mol $SO_2$
Ta có: \(\dfrac{80a+\left(1-0,5a\right).32+\left(1-a\right).64}{a+1-0,5a+1-a}=60\Rightarrow a=0,8\)
Suy ra $\%V_{O_2}=37,5\%;\%V_{SO_2}=12,5\%;\%V_{SO_3}=50\%$

a. Phương trình phản ứng :
C2H2 + 2Br2 → C2H2Br4 (1)
C2H4 + Br2 → C2H4Br2 (2)
b. Hỗn hợp khí B gồm có H2, C2H6. Gọi x, y ( mol ) lần lượt là số mol của H2 và C2H6 có trong 6,72 lít hỗn hợp B.
nB = x + y = 6,72 : 22,4 = 0,3 mol (I)
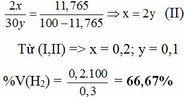
% V(C2H6) = 100% – 66,67% = 33,33%
c. nA = 11,2 : 22,4 = 0,5 mol , M A = 0,4 . 44 = 17,6 g/ mol
mA = 0,5 . 17,6 = 8,8 gam
mB = 0,2 . 2 + 0,1 . 30 = 3,4 gam
Vậy khối lượng bình Br2 tăng: m = mA – mB = 8,8 – 3,4 = 5,4 gam.

a.
BTKL ta có mX = mY => nX . MX = nY . mY
MX / My = nY / mY =0.75
Đặt nX = 1 mol => nY = 0,75 mol => nH2 phản ứng = 1 – 0,75 = 0,25mol
* TH hidrocacbon là anken: n anken = n H2 = 0,25 mol => n H2 trong X = 0,75 => M = (6,75 – 0,75 . 2)/0,25 = 21 (loại) * TH là ankin: => n akin = 0,25/2 = 0,125 => n H2 trong X = 0,875 mol => M = (6,75 – 0,875 . 2)/0,125 = 40 =>C3H4
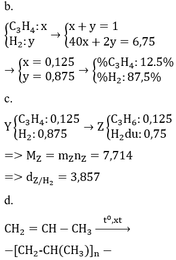




Giả sử trong 1 mol hỗn hợp A có x mol C2H4 và (1 – x) mol H2
\(M_A=28x+2\left(1-x\right)=7,5.2=15\left(\frac{g}{mol}\right)\)
\(\Rightarrow x=0,5\left(mol\right)\)
a,\(V\%_{C2H4}=\frac{0,5}{1}.100\%=50\%=V\%_{H2}\)
Giả sử khi dẫn 1 mol A qua chất xúc tác Ni, có n mol C2H4 tham gia phản ứng :
\(C_2H_4+H_2\rightarrow C_2H_6\)
BTKL:
\(m_A=m_B=15\left(g\right)\)
\(M_B=9.2=18\Rightarrow n_B=0,83\left(mol\right)\)
\(n_{H2\left(pư\right)}=1-0,83=0,167\left(mol\right)\)
\(\Rightarrow H=\frac{0,167}{0,5}.100\%=33,33\%\)