Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Gọi \(\left\{{}\begin{matrix}n_{Al}=x\left(mol\right)\\n_{Fe}=y\left(mol\right)\end{matrix}\right.\)
\(n_{H_2}=\dfrac{4,48}{22,4}=0,2mol\)
\(2Al+6HCl\rightarrow2AlCl_3+3H_2\)
\(Fe+2HCl\rightarrow FeCl_2+H_2\)
Theo pt: \(\Rightarrow\left\{{}\begin{matrix}3x+y=0,2\\27x+56y=5,5\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}x=\dfrac{19}{470}\\y=\dfrac{37}{470}\end{matrix}\right.\)
\(\%m_{Al}=\dfrac{\dfrac{19}{470}\cdot27}{5,5}\cdot100\%=19,84\%\)
\(\%m_{Fe}=100\%-19,84\%=80,16\%\)

dạ em cảm ơn anh/thầy nhưng mà cái tổng HCl ra m bấm máy sai rồi ạ vs cảm ơn anh/thầy giúp em giải bài nha

Ta có: \(n_{H_2}=\dfrac{7,84}{22,4}=0,35\left(mol\right)\)
PT: \(Mg+2HCl\rightarrow MgCl_2+H_2\)
\(2Al+6HCl\rightarrow2AlCl_3+3H_2\)
\(Fe+2HCl\rightarrow FeCl_2+H_2\)
Theo PT: \(n_{HCl\left(1\right)}=2n_{H_2}=0,7\left(mol\right)\)
Theo ĐLBT KL: mA + mHCl = m muối do hh A sinh ra + mH2
⇒ m muối do hh A sinh ra = 10,7 + 0,7.36,5 - 0,35.2 = 35,55 (g)
Có: \(n_{CuO}=\dfrac{8}{80}=0,1\left(mol\right)\)
PT: \(CuO+2HCl\rightarrow CuCl_2+H_2O\)
____0,1____________0,1 (mol)
⇒ c = m muối do hh A sinh ra + mCuCl2 = 35,55 + 0,1.135 = 49,05 (g)
Bạn tham khảo nhé!

\(n_{Ca}=\dfrac{4}{40}=0,1\left(mol\right)\)
PT: \(Ca+2H_2O\rightarrow Ca\left(OH\right)_2+H_2\)
Theo PT: \(n_{H_2}=n_{Ca}=0,1\left(mol\right)\)
- Khử oxit:
\(CuO+H_2\underrightarrow{t^o}Cu+H_2O\)
\(FeO+H_2\underrightarrow{t^o}Fe+H_2O\)
Ta có: 80nCuO + 72nFeO = 11,6 (1)
Theo PT: \(n_{H_2}=n_{CuO}+n_{FeO}=0,1\left(2\right)\)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}n_{CuO}=\\n_{FeO}=\end{matrix}\right.\)
Đến đây thì ra số mol âm, bạn xem lại đề nhé.

\(n_{H_2}=a\left(mol\right)\)
\(\text{Coi hỗn hợp là : kim loại M}\)
\(2M+2nHCl\rightarrow2MCl_n+nH_2\)
\(\text{Từ PTHH ta thấy : }\)
\(n_{HCl}=2n_{H_2}=2a\left(mol\right)\)
\(\text{Bảo toàn khối lượng : }\)
\(m_{hh}+m_{HCl}=m_{Muối}+m_{H_2}\)
\(\Leftrightarrow5+36.5\cdot2a=5.71+2a\)
\(\Leftrightarrow a=0.01\)
\(V_{H_2}=0.01\cdot22.4=0.224\left(l\right)\)
\(b.\)
\(CuO+H_2\underrightarrow{^{^{t^0}}}Cu+H_2O\)
\(FeO+H_2\underrightarrow{^{^{t^0}}}Fe+H_2O\)
\(n_{H_2O}=n_{H_2}=0.01\left(mol\right)\)
\(\text{Bảo toàn khối lượng : }\)
\(m_{hh}=m_{kl}+m_{H_2O}-m_{H_2}=0.6+0.01\cdot18-0.01\cdot2=0.76\left(g\right)\)

2. Ta có : \(n_{Na}>n_{Al}\) nên Al sẽ tan hết
Số mol H2 thu được: \(\dfrac{5 + 4.3}{2}=8,5 \)(mol)
Như vậy, khi cho Fe vào H2SO4 sẽ thu được 2,125 mol khí
\(\Rightarrow n_{Fe}=2,125 \) (mol)
=>\(\%m_{Na}=\dfrac{5.23}{5.23+4.27+56.2,125}.100=33,63\%\)
=> Chọn B
\(\begin{cases} nMg=a (mol)\\ nAl=b (mol) \end{cases} \)=> 24a +27b=12,6 (1)
n(H2)= 0,6mol
Mg+H2SO4 ---> MgSO4 +H2
a. a a. (Mol)
2Al + 3H2SO4 ---> Al2(SO4)3 + 3H2
b. 1,5b 0,5b 1,5b. (Mol)
=> a+1,5b=0,6 (2)
Từ (1) và (2) => \(\begin{cases} a=0,3\\ b=0,2 \end{cases}\)
n(H2SO4) =n(H2) =0,6mol
m(H2SO4)= 0,6*98=58,8(g)
m(dd H2SO4)=58,8*100/20 =294(g)
mdd= 12,6+294-0,6*2=305,4(g)
C%(Al2(SO4)3)= \(\dfrac{0,5*0,2*342*100%}{305,4}\)=11,198%
Câu 1 Chọn B

Gọi: \(\left\{{}\begin{matrix}n_{Al}=x\left(mol\right)\\n_{Fe}=y\left(mol\right)\end{matrix}\right.\) ⇒ 27x + 56y = 5,5 (1)
PT: \(2Al+6HCl\rightarrow2AlCl_3+3H_2\)
\(Fe+2HCl\rightarrow FeCl_2+H_2\)
Theo PT: \(n_{H_2}=\dfrac{3}{2}n_{Al}+n_{Fe}=\dfrac{3}{2}x+y=\dfrac{4,48}{22,4}=0,2\left(mol\right)\left(2\right)\)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}x=0,1\left(mol\right)\\y=0,05\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}\%m_{Al}=\dfrac{0,1.27}{5,5}.100\%\approx49,09\%\\\%m_{Fe}\approx50,91\%\end{matrix}\right.\)

1. Gọi mol của Mg và Al là x, y mol
=> 24x + 27y = 12,6 (1)
nH2 = 0,6 mol => x + 1,5y = 0,6 (2)
Từ (1) (2) => x = 0,3 ; y = 0,2
=> %Mg = 57,14%
=> %Al = 42,86%
nH2=13,44/22,4=0,6(mol)
Đặt: nMg=a(mol); nAl=b(mol) (a,b>0)
1) PTHH: Mg + H2SO4 -> MgSO4 + H2
a__________a________a_____a(mol)
2Al +3 H2SO4 -> Al2(SO4)3 + 3 H2
b___1,5b______0,5b____1,5b(mol)
Ta có hpt:
\(\left\{{}\begin{matrix}24a+27b=12,6\\a+1,5b=0,6\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}a=0,3\\b=0,2\end{matrix}\right.\)
=> mMg=0,3.24=7,2(g)
=>%mMg= (7,2/12,6).100=57,143%
=>%mAl=42,857%
2) mMgSO4=120.a=120.0,3=36(g)
mAl2(SO4)3=342.0,5b=342.0,5.0,2= 34,2(g)
mH2SO4= (0,3+0,2.1,5).98=58,8(g)
=>mddH2SO4=58,8: 14,7%=400(g)
=>mddsau= 12,6+400 - 2.0,6= 411,4(g)
=>C%ddAl2(SO4)3= (34,2/411,4).100=8,313%
C%ddMgSO4=(36/411,4).100=8,751%

nH2O=0.2
nCuO=x,nAl2O3=y,nFeO=z
80x + 102y + 72z = 17.86
x + z =0.2
135x + 267y + 127z = 33.81
=> y=0.03 => mAl2O3=3.06g =>D
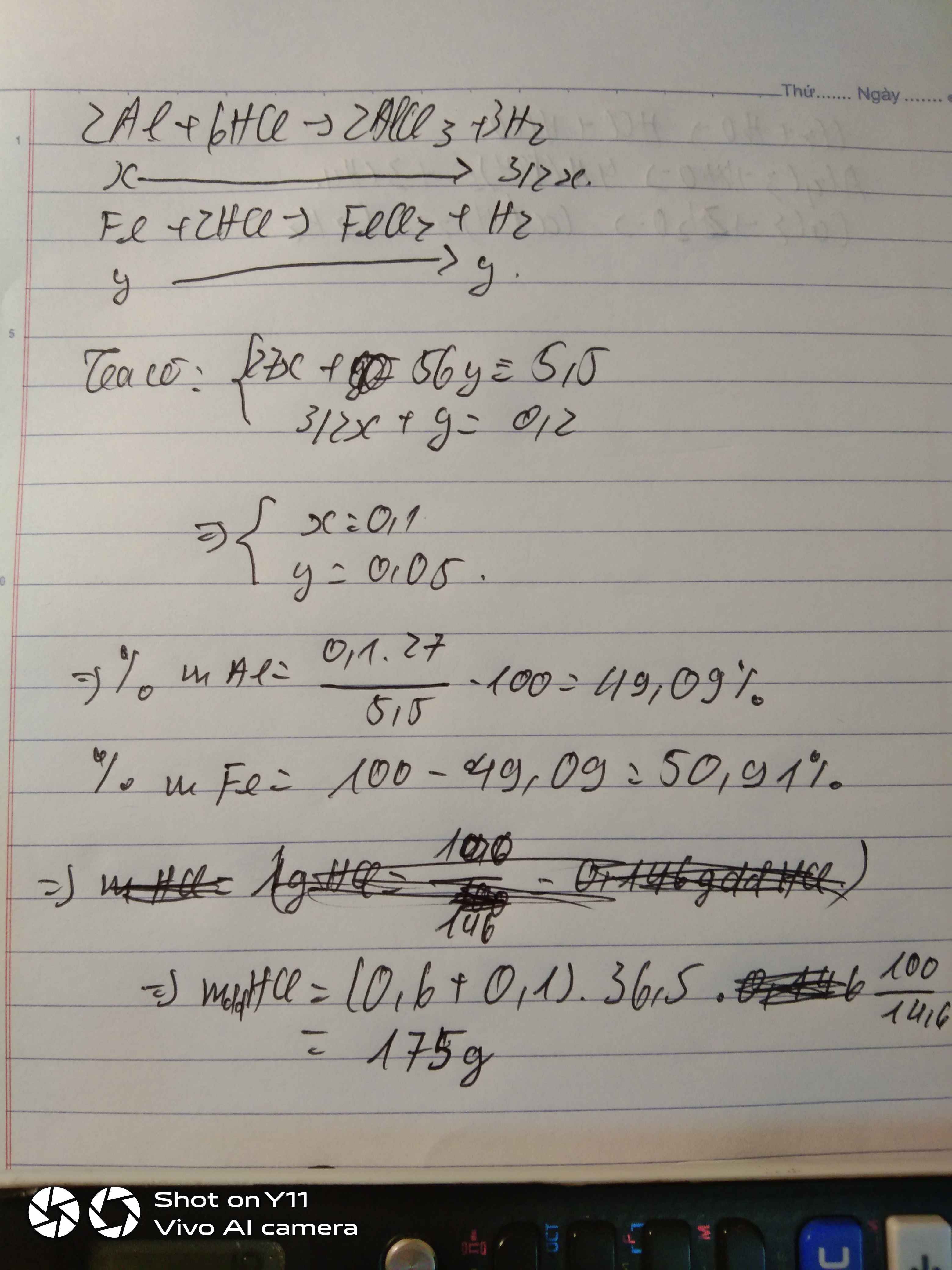

\(a.Đặt:\left\{{}\begin{matrix}n_{CuO}=x\left(mol\right)\\n_{Al_2O_3}=y\left(mol\right)\\n_{FeO}=z\left(mol\right)\end{matrix}\right.\\ Tacó:80x+102y+72z=47,8\left(g\right)\left(1\right)\\ \\ Phần1:\left\{{}\begin{matrix}n_{CuO}=\dfrac{x}{2}\left(mol\right)\\n_{Al_2O_3}=\dfrac{y}{2}\left(mol\right)\\n_{FeO}=\dfrac{z}{2}\left(mol\right)\end{matrix}\right.\\ CuO+2HCl\rightarrow CuCl_2+H_2O\\ Al_2O_3+6HCl\rightarrow2AlCl_3+3H_2O\\ FeO+2HCl\rightarrow FeCl_2+H_2O\\ n_{HCl}=\dfrac{x}{2}.2+\dfrac{y}{2}.6+\dfrac{z}{2}.2=\dfrac{400.8,2125\%}{36,5}=0,9\left(mol\right)\left(2\right)\\ Phần2:\\ CuO+H_2SO_{4\left(đ,n\right)}\rightarrow CuSO_4+H_2O\\ Al_2O_3+3H_2SO_{4\left(đ,n\right)}\rightarrow Al_2\left(SO_4\right)_3+3H_2O\\ 2FeO+4H_2SO_4\rightarrow Fe_2\left(SO_4\right)_3+SO_2+4H_2O\\ n_{FeO}=\dfrac{z}{2}=2n_{SO_2}=2.\dfrac{1,68}{22,4}=0,15\\ \Rightarrow z=0,3\left(mol\right)\left(3\right)\\ Từ\left(1\right),\left(2\right),\left(3\right)\Rightarrow\left\{{}\begin{matrix}x=0,126\\y=0,158\\z=0,3\end{matrix}\right.\\ \Rightarrow\%CuO=21,09,\%Al_2O_3=33,72\%,\%FeO=45,19\%\\ b.m_{ddB}=\dfrac{47,8}{2}+400=123,9\left(g\right)\\ n_{CuCl_2}=\dfrac{0,126}{2}=0,063\left(mol\right)\\ n_{AlCl_3}=\dfrac{0,158}{2}.2=0,158\left(mol\right)\\ n_{FeCl_2}=\dfrac{0,3}{2}=0,15\left(mol\right)\\ C\%_{CuCl_2}=\dfrac{0,063.135}{123,9}.100=6,86\%\\ C\%_{AlCl_3}=\dfrac{0,158.133.5}{123,9}.100=17,02\%\\ C\%_{FeCl_2}=\dfrac{0,15.127}{123,9}.100=15,38\%\)