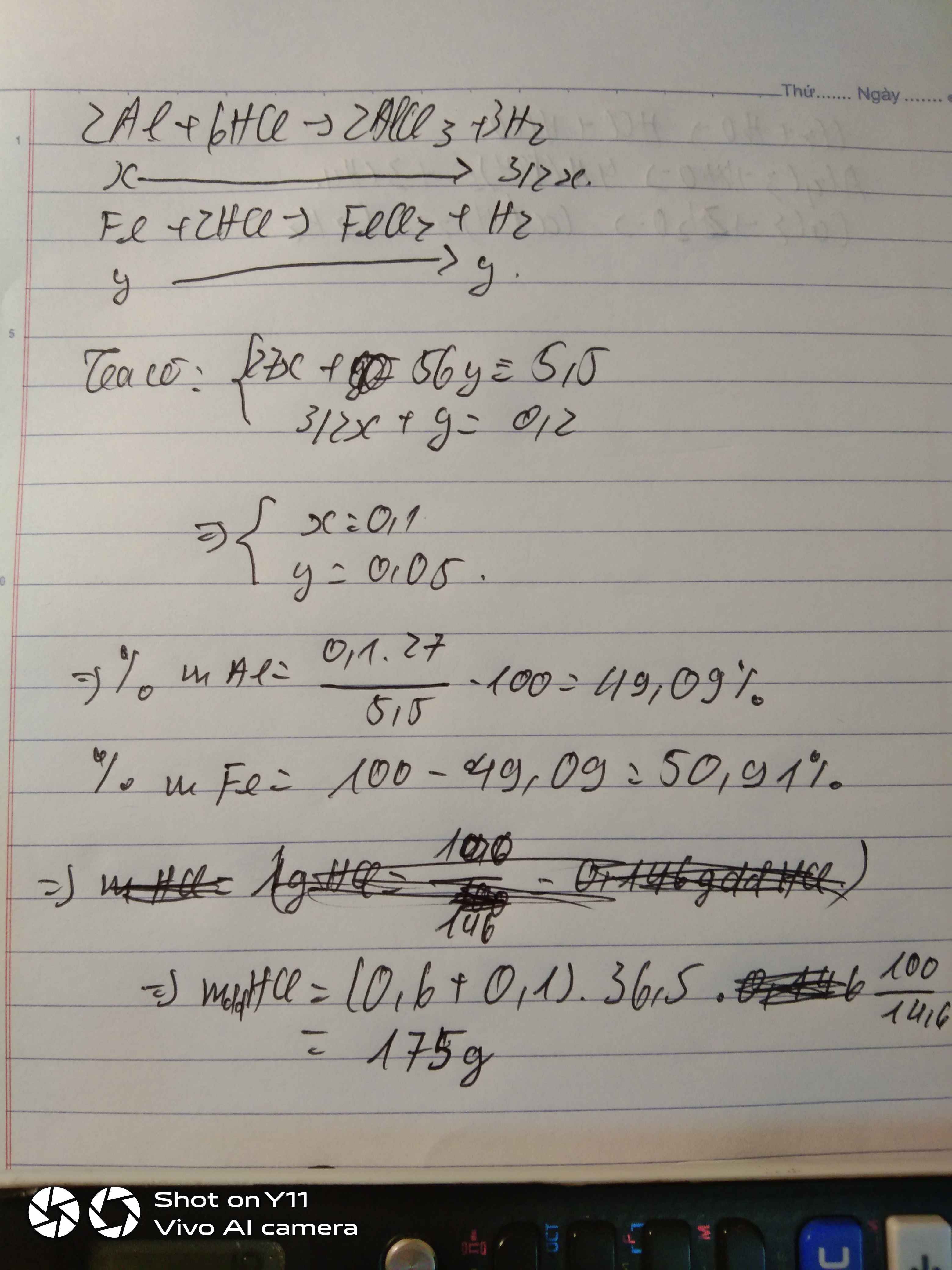Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

4) x,y lần lượt là số mol của M và M2O3
=> nOxi=3y=nCO2=0,3 => y=0,1
Đề cho x=y=0,1 =>0,1M+0,1(2M+48)=21,6 =>M=56 => Fe và Fe2O3
=> m=0,1.56 + 0,1.2.56=16,8
2)X + 2HCl === XCl2 + H2
n_h2 = 0,4 => X = 9,6/0,4 = 24 (Mg)
=>V_HCl = 0,4.2/1 = 0,8 l

Gọi \(\left\{{}\begin{matrix}n_{Al}=x\left(mol\right)\\n_{Fe}=y\left(mol\right)\end{matrix}\right.\)
\(n_{H_2}=\dfrac{4,48}{22,4}=0,2mol\)
\(2Al+6HCl\rightarrow2AlCl_3+3H_2\)
\(Fe+2HCl\rightarrow FeCl_2+H_2\)
Theo pt: \(\Rightarrow\left\{{}\begin{matrix}3x+y=0,2\\27x+56y=5,5\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}x=\dfrac{19}{470}\\y=\dfrac{37}{470}\end{matrix}\right.\)
\(\%m_{Al}=\dfrac{\dfrac{19}{470}\cdot27}{5,5}\cdot100\%=19,84\%\)
\(\%m_{Fe}=100\%-19,84\%=80,16\%\)

Bài 1:
Ta có: \(n_{HCl}=0,2.0,5=0,1\left(mol\right)\)
BTNT H, có: \(n_{HCl}=2n_{H_2O}\Rightarrow n_{H_2O}=0,05\left(mol\right)\)
Theo ĐL BTKL, có: m oxit + mHCl = mmuối + mH2O
⇒ mmuối = 2,8 + 0,1.36,5 - 0,05.18 = 5,55 (g)
Bài 2:
\(m_{KOH}=200.5,6\%=11,2\left(g\right)\Rightarrow n_{KOH}=\dfrac{11,2}{56}=0,2\left(mol\right)\)
PT: \(2KOH+CuCl_2\rightarrow2KCl+Cu\left(OH\right)_2\)
Theo PT: \(n_{Cu\left(OH\right)_2}=\dfrac{1}{2}n_{KOH}=0,1\left(mol\right)\)
\(\Rightarrow m_{Cu\left(OH\right)_2}=0,1.98=9,8\left(g\right)\)

\(n_{Fe}=\dfrac{8,4}{56}=0,15\left(mol\right)\)
PTHH :
\(Fe+2HCl\rightarrow FeCl_2+H_2\uparrow\)
0,15 0,3 0,15 0,15
\(V_{H_2}=n.22,4=0,15.22,4=3,36\left(l\right)\)
Còn lại đề thiếu dữ kiện , bạn bổ sung và nếu cần thì đăng lại nha

a,Fe + 2HCl → FeCl + H2 (1)
FeO + 2HCl → FeCl + H2O (2)
nH2 = 3,36/ 22,4 = 0,15 ( mol)
Theo (1) nH2 = nFe = 0,15 ( mol)
mFe = 0,15 x 56 = 8.4 (g)
m FeO = 12 - 8,4 = 3,6 (g)
a, \(n_{H_2}=\frac{3,36}{22,4}=0,15\left(mol\right)\)
\(Fe+2HCl->FeCl_2+H_2\left(1\right)\)
\(FeO+2HCl->FeCl_2+H_2O\left(2\right)\)
theo (1) \(n_{Fe}=n_{H_2}=0,15\left(mol\right)\)
=> \(m_{Fe}=0,15.56=8,4\left(g\right)\)
=> \(m_{FeO}=12-8,4=3,6\left(g\right)\)

ta thấy : nFe =nH2 = 0,15
=> mFe =0,15 x 56 = 8,4g
%Fe=8,4/12 x 100 = 70%
=>%FeO = 100 - 70 = 30%
b) BTKLra mdd tìm mct of HCl
c) tìm mdd sau pứ -mH2 nha bạn

a) nHCl = 0,8.0,35 = 0,28 (mol)
mmuối = mKL + mCl = 3,64 + 0,28.35,5 = 13,58 (g)
b)
3,64 gam X phản ứng vừa đủ với 0,28 mol HCl
=> 3,64 gam X phản ứng vừa đủ với 0,28 mol H+
=> 1,82 gam X phản ứng vừa đủ với 0,14 mol H+
=> 1,82 gam X phản ứng vừa đủ với \(\dfrac{0,14}{2}=0,07\) mol H2SO4
mH2SO4 = 0,07.98 = 6,86 (g)
Cần thêm C% để tính m dung dịch nhé :)

Bài 1:
PTHH: \(Mg+2HCl\rightarrow MgCl_2+H_2\uparrow\)
Ta có: \(n_{Mg}=\dfrac{4,8}{24}=0,2\left(mol\right)\)
\(\Rightarrow\left\{{}\begin{matrix}n_{HCl}=0,4\left(mol\right)\\n_{H_2}=0,2\left(mol\right)\end{matrix}\right.\) \(\Rightarrow\left\{{}\begin{matrix}m_{ddHCl}=\dfrac{0,4\cdot36,5}{14,6\%}=100\left(g\right)\\V_{H_2}=0,2\cdot22,4=4,48\left(l\right)\end{matrix}\right.\)
Bài 2:
PTHH: \(2KOH+H_2SO_4\rightarrow K_2SO_4+2H_2O\)
Ta có: \(\left\{{}\begin{matrix}n_{KOH}=\dfrac{100\cdot11,2\%}{56}=0,2\left(mol\right)\\n_{H_2SO_4}=\dfrac{150\cdot9,8\%}{98}=0,15\left(mol\right)\end{matrix}\right.\)
Xét tỉ lệ: \(\dfrac{0,2}{2}< \dfrac{0,15}{1}\) \(\Rightarrow\) H2SO4 còn dư, KOH p/ứ hết
\(\Rightarrow\left\{{}\begin{matrix}n_{K_2SO_4}=0,1\left(mol\right)\\n_{H_2SO_4\left(dư\right)}=0,05\left(mol\right)\end{matrix}\right.\) \(\Rightarrow\left\{{}\begin{matrix}m_{K_2SO_4}=0,1\cdot174=17,4\left(g\right)\\m_{H_2SO_4\left(dư\right)}=0,05\cdot98=4,9\left(g\right)\end{matrix}\right.\)
Mặt khác: \(m_{dd}=m_{ddKOH}+m_{ddH_2SO_4}=250\left(g\right)\)
\(\Rightarrow\left\{{}\begin{matrix}C\%_{K_2SO_4}=\dfrac{17,4}{250}\cdot100\%=6,96\%\\C\%_{H_2SO_4\left(dư\right)}=\dfrac{4,9}{250}\cdot100\%=1,96\%\end{matrix}\right.\)