Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(1,n_{HF}=\dfrac{2,5.40\%}{100\%.20}=0,05(kmol)\\ PTHH:CaF_2+H_2SO_4\to CaSO_4+2HF\\ \Rightarrow n_{CaF_2}=0,025(kmol)\\ \Rightarrow m_{CaF_2}=0,025.78=1,95(kg)\\ 2,\text {Đặt }\begin{cases} n_{Fe}=x(mol)\\ n_{Al}=y(mol) \end{cases} \Rightarrow 56x+27y=11(1)\\ n_{H_2}=\dfrac{8,96}{22,4}=0,4(mol)\\ PTHH:Fe+2HCl\to FeCl_2+H_2\\ 2Al+6HCl\to 2AlCl_3+3H_2\\ \Rightarrow x+1,5y=0,4(2)\\ (1)(2)\Rightarrow \begin{cases} x=0,1(mol)\\ y=0,2(mol) \end{cases} \Rightarrow \begin{cases} \%_{Fe}=\dfrac{0,1.56}{11}.100\%=50,91\%\\ \%_{Al}=100\%-50,91\%=49,09\% \end{cases}\)
\(b,\Sigma n_{HCl}=2n_{Fe}+3n_{Al}=0,2+0,6=0,8(mol)\\ \Rightarrow V_{dd_{HCl}}=\dfrac{0,8}{2}=0,4(l)\)

a)
Gọi CT của ankan là CnH2n+2
CnH2n+2 + O2 \(\underrightarrow{t^o}\) nCO2 + (n+1)H2O
Theo đầu bài ta có: mCO2 + mH2O = 20,4
n = 3
Vậy CTPT của X là C3H8. …
Vì hỗn hợp Z tác dụng với dung dịch AgNO3/NH3 thu được kết tủa \(\rightarrow\) hiđrocacbon B có liên kết 3 đầu mạch.
Gọi CTTB của 2 hidrocacbon A và B là \(C_{\overline{x}}H_{\overline{y}}\)
\(C_{\overline{x}}H_{\overline{y}}\) + O2 \(\rightarrow\overline{x}\)CO2 + \(\frac{\overline{y}}{2}\)H2O
Theo đề bài ta có \(\overline{x}\) = 2,6 (vì \(\overline{x}\) = 2,6 nên hiđroccacbon B có số nguyên tử nhỏ hơn 2,6).
Vậy hiđrocacbon B là C2H2
Gọi \(n_{C_2H_2}=x,\) \(n_{C_3H_8}=y\) .Ta có: \(\begin{cases}x+y=0,1\\2x+3y=0,26\end{cases}\)\(\rightarrow\begin{cases}x=0,04\\y=0,06\end{cases}\)
Khối lượng kết tủa là C2Ag2 m = 9,6 gam
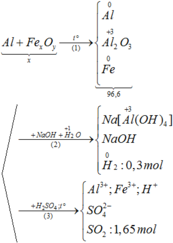
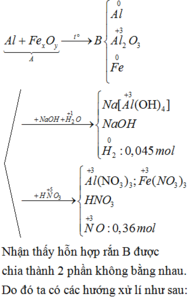

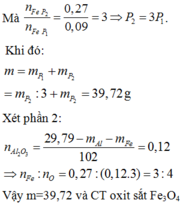

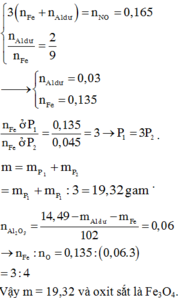

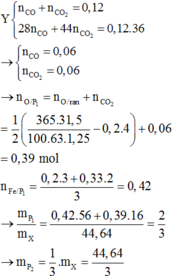

Lần sau nhớ ghi đề đúng nha cậu.
Ta có :
Trong 6.4g hh có a (mol) Fe và b (mol) FexOy
Trong 3.2g hh có 0.5a (mol) Fe và 0.5b (mol) FexOy
TN1:
Fe + 2HCl --> FeCl2 + H2
a__________________a
nH2= 2.24/22.4=0.1 mol
=> a= 0.1
mhh= 0.1*56 + b(56x + 16y ) = 6.4 g
=> b(56x + 16y ) = 0.8 (1)
TN2:
nH2O= 0.1/18=1/180 mol
FexOy + yH2O -to-> xFe + yH2O
1/180y__________________1/180
nFexOy = 0.5b= 1/180y
=> b= 1/90y
Từ (1) :
b(56x + 16y)=0.8
=> 1/90y*(56x + 16y ) = 0.8
=> 56x = 56y
=> x/y= 1/1
Vậy: CT của oxit sắt : FeO
FexOy nhé không phải là FeS