Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Ta có: mMuối = mKim loại + mNO3– = 17,84 + mNO3–
+ Mà nNO3– = 3nNO = 0,54 mol.
⇒ mMuối = 17,84 + 0,54×62 = 51,32 gam.
Đáp án D

Quy đổi hỗn hợp thành hỗn hợp Fe (a mol) và O (b mol) =>56a + 16b = 11,36
Bảo toàn electron
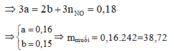
Đáp án D

Đáp án D
Giải hệ số mol khí ta có 0,04mol N2O và 0,26 mol NO
Hỗn hợp X tác dụng với HNO3 và H2SO4 đều dùng dư nên lượng electron cho ở hai trường hợp trên như nhau.
Lượng electron nhận ở hai thí nghiệm: 8.0,04 + 3.0,26 = 1,1mol < 0,7.2 = 1,4mol
Có NH4NO3 nên chênh lệch trên → có (1,4 – 1,1) : 8 = 0,0375 mol NH4NO3
⇒ ∑ mmuối nitrat kim loại = 129,4 – 0,0375.80
= 126,4 gam dạng M(NO3)n
Lại có 104 gam muối sunfat kim loại dạng M2(SO4)n || Tương quan 1SO4 ⇄ 2NO3
→ Tăng giảm khối lượng có số mol gốc sunfat = (126,4 – 104) : (62.2 – 96) = 0,8mol
→ Bảo toàn nguyên tố S có: 0,8 + 0,7 = 1,5mol H2SO4, tiếp tục bảo toàn H có 1,5mol H2O
→ BTKL phản ứng X + H2SO4 ta có m = 104 + 0,7.64 + 1,5.18 – 1,5.98 = 28,8gam



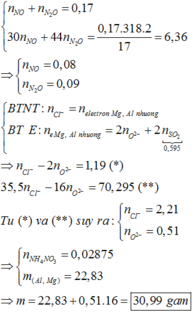
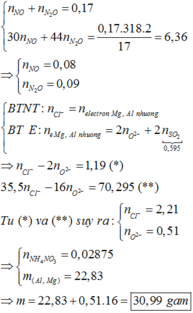
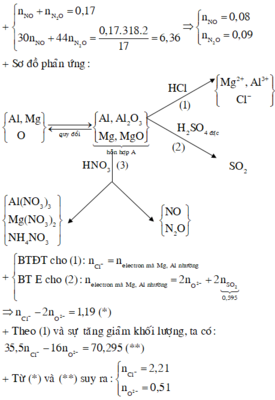

Đáp án: A
nNO= 0,01 mol=> nNO3-= 0,03 mol
m muối= m kim loại + m NO3- = 2+ 0,03.62= 3,86 gam