Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Bài 1:
A + Cl2 → ACl2 (1)
Fe + ACl2 → FeCl2 + A (2)
x x x (mol)
gọi số mol của Fe phản ứng với một số mol của ACl2 là x
khối lương thanh sắt sau phản ứng là:11,2 - 56x + xMA = 12
=> x =
Ta có:
= 0,25.0,4 = 0,1 (mol)
=> MA = 64 g/mol; Vậy kim loại A là Cu
= nCu =
= 0,2 (mol) =>
= 0,5M
bài 2:
(C17H35COO)3C3H5 + 3NaOH -> 3 C17H35COONa + C3H5(OH)3
890 kg 918 kg
x kg 720 kg
=> x = 698,04 kg.

Bạn bấn vào đây, có người hỏi bài này rồi nhá Câu hỏi của Mạc Nhược Ca - Hóa học lớp 12 | Học trực tuyến

Gọi a và b lần lượt là số mol của nhôm và của nhôm nitrat.
mX=mnhôm nitrat ⇔ 27a+213b=\(\dfrac{a+b}{2}\).102 ⇔ b=\(\dfrac{4}{27}\)a.
BTe: 3nnhôm=3nNO=3.0,81 ⇒ nnhôm=a=0,81 mol ⇒ b=nnhôm nitrat=0,12 mol.
Rắn khan trong Y chỉ chứa Al(NO3)3 (0,81+0,12=0,93 (mol)) với khối lượng là 0,93.213=198,09 (g).
Chọn B.

Đáp án C
Cho m gam hỗn hợp rắn gồm Fe, Fe(NO3)2 vào dung dịch chứa 0,08 mol Cu(NO3)2, 0,02 mol Fe(NO3)3 và HCl thu được dung dịch X và hỗn hợp hai khí không màu, có một khí hóa nâu trong không khí là NO
Ta có: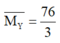 nên khí còn lại là H2 và tỉ lệ số mol NO: H2 là 5:1.
nên khí còn lại là H2 và tỉ lệ số mol NO: H2 là 5:1.
Cho AgNO3 dư vào dung dịch X thấy thoát ra 0,045 mol khí NO nên H+ dư trong X là 0,18 mol, do vậy X không chứa NO3-.
Mặt khác vì còn lại rắn không tan nên trong X chỉ chứa Fe2+ nên X chứa HCl dư và FeCl2.
Do còn H+ dư nên Fe hết ® rắn còn lại là Cu 0,08 mol
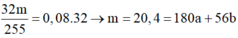
Gọi số mol Fe(NO3)2 là a mol; Fe là b mol và HCl là c mol
Bảo toàn N:![]()
![]()
Bảo toàn H:![]()
![]()
Bảo toàn nguyên tố Fe: ![]()
Giải hệ: a=0,04; b=0,6; c=1,5
Bảo toàn Cl:![]()
Bảo toàn e: ![]()
![]()
![]()

nCu = 0,02; nAg = 0,005 → Tổng số mol e cho tối đa: = 0,02.2 + 0,005.1 = 0,45
nH+ = 0,09; nNO3- = 0,06 (dư)
4H+ + NO3- + 3e → NO + 2H2O
0,06 0,045 0,015
Cu, Ag đã phản ứng hết
2NO + O2 → 2NO2
0,015 0,0075 0,015
4NO2 + O2 + 2H2O → 4HNO3
0,015 0,015
Nồng độ mol HNO3 = 0,015:0,15 = 0,1 → pH = 1
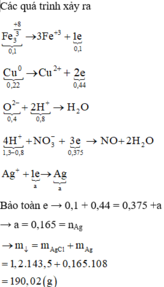

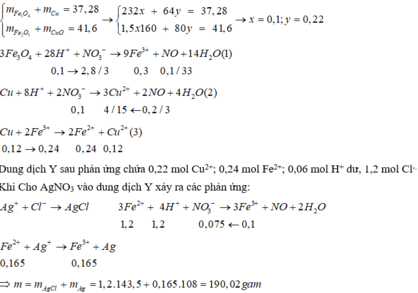
 với các chất sau:
với các chất sau:
Đáp án B
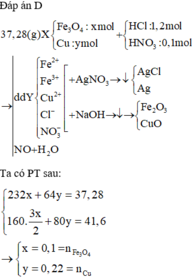
Đặt nFe₃O₄ = x; nCu = y ⇒ mX = 232x + 64y = 37,28(g).
~ Chú ý: "hòa tan hết" ⇒ toàn bộ nguyên tố Fe và Cu sẽ đi hết vào oxit :P
Mặt khác, nung trong KHÔNG KHÍ
⇒ oxit là Fe₂O₃ (1,5x mol) và CuO (y mol).
⇒ m oxit = 41,6(g) = 160.1,5x + 80y
⇒ giải hệ có: x = 0,1 mol; y = 0,22 mol
► nHCl = 1,2 mol; nHNO₃ = 0,1 mol
⇒ nH⁺ = 1,3 mol; nNO₃⁻ = 0,1 mol.
Do Y + AgNO₃ -> sinh ra khí NO
⇒ Y có chứa H⁺, Fe²⁺ và không chứa NO₃⁻
(vì nếu có NO₃⁻ sẽ phản ứng sinh ra NO rồi :P)
Bỏ qua phần H⁺ "trung hòa" oxi trong oxit: 2H⁺ + O → H₂O thì còn
nH⁺ = 1,3 - 0,4 × 2 = 0,5 mol
● Xét toàn bộ các quá trình cho - nhận electron:
– Cho e: 3Fe⁺⁸/₃ → 3Fe⁺³ + e
Cu → Cu²⁺ + 2e
– Nhận e: 4H⁺ + NO₃⁻ + 3e → NO + 2H₂O
Ag⁺ + e → Ag
Do NO₃⁻ cả quá trình dư (vì AgNO₃ dư) nên:
⇒ bảo toàn electron cả quá trình:
nFe₃O₄ + 2nCu = ³/₄nH⁺ + nAg
⇒ nAg = 0,165 mol (nH⁺ đây là nH⁺ không tính phần "trung hòa" oxi trong oxit )
BTNT(Cl) ⇒ nAgCl = nHCl = 1,2 mol
⇒ m = 0,165 × 108 + 1,2 × 143,5 = 190,02(g)