Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Có : nFe = nAl = nMg = 0,12 mol
Y : N2 ; N2O ; NO và NO2( N2 và NO2 có số mol bằng nhau)
=> Qui đổi : NO2 +N2 -> NO + N2O
=> Y trở thành : NO và N2O với số mol lần lượt là x và y.
Có : MY = 37g => mY = 37(x + y) = 30x + 44y
=> x = y(1)
Giả sử có z mol NH4NO3 trong muối
Bảo toàn e : 3nFe + 3nAl + 2nMg = 3nNO + 8nN2O + 8nNH4NO3
=> 3x + 8y + 8z = 0,96 mol(2)
Và : nHNO3 = (4x + 10y + 10z)
=> nH2O = ½ (nHNO3 – 4nNH4NO3) = (2x + 5y + 3z) mol
Bảo toàn khối lượng :
mY = mKL + mHNO3 – mH2O - mmuối X = (216x + 540y + 576z) – 62,52 = 37(x + y)
=> 179x + 503y + 576z = 62,52(3)
Từ (1),(2),(3) => x = y = 0,06 ; z = 0,0375 mol
=> nHNO3 pứ = 4x + 10y + 10z = 1,215 mol

Đáp án B
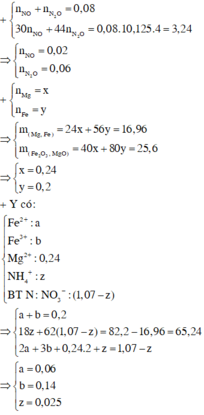
n o trong Z = 0 , 17 C % Fe NO 3 3 = 0 , 14 . 242 16 , 96 + 0 , 17 . 2 + 242 - 3 , 24 . 100 ≈ 13 %

- Viết đúng ptpư:
\(Fe+4HNO_3\rightarrow Fe\left(NO_3\right)_3+NO+2H_2O\)
\(3Cu+8HNO_3\rightarrow2Cu\left(NO_3\right)_2+2NO+4H_2O\)
\(nNO=0,04\left(mol\right)\)
Gọi nFe là x(mol) ; nCu là y(mol)
ta có hệ pt:
\(\left\{{}\begin{matrix}m_{hh}=56x+64y=3,04\\nNO=x+\dfrac{2}{3y}=0,04\end{matrix}\right.\)
Giải hệ ta được: x = 0,02 mol ; y = 0,03 mol
\(\Rightarrow mFe=0,02.56=1,12\left(g\right)\)
\(mCu=0,03.64=1,92\left(g\right)\)

Ta có nMg=0,145 mol
Gọi x và y lần lượt là số mol của H2 và N2
Ta có: x+ y= 0,025; 2x+ 28y= 0,025.(11,4.2) → x= 0,005; y= 0,02
Vì có khí H2 thoát ra → NO3- hết → Muối thu được là muối clorua
QT cho e:
Mg → Mg2++ 2e (1)
0,145→ 0,29 mol
QT nhận e:
2N+5+ 10e →N2 (2)
0,2← 0,02 mol
2H+1+2e→ H2 (3)
0,01← 0,005 mol
Nếu chỉ có quá trình nhận (2) và (3) thì
ne nhận= 0,2+ 0,01= 0,21 mol≠ 0,29 mol
→ Còn có quá trình nhận e tạo muối NH4+
Theo ĐL bảo toàn e: ne cho=n e nhận= 0,29 mol → e nhận ở (4)= 0,29-0,21=0,08 mol
NO3-+ 8e+ 10H+ → NH4++ 3H2O (4)
0,08 → 0, 01 mol
Bảo toàn nguyên tố N ta có
nN(KNO3)= nN(N2)+ nN (NH4+)=2.0,02+ 0,01= 0,05 mol= nKNO3= nK+
Muối chứa Mg2+: 0,145 mol, NH4+: 0,01 mol, K+: 0,05 mol, Cl-
Dùng bảo toàn điện tích: 0,145.2+ 0,01.1+ 0,05= nCl-= 0,35 mol
→mmuối=m= 0,145.24+ 0,01.18+ 0,05.39+ 0,35.35,5= 18,035 gam
Đáp án D

Gọi số mol của Cu là a => nAl= 2a, nMg= 3a
mCu+mAl+mMg = 19 => a=0,1 =>nCu=0,1(mol);nAl=0,2(mol);nMg=0,3(mol)
dY/H2 =18,5 => M(Y)= 37 (dùng pp đường chéo) => nNO=nN2O
n(Y)= \(\dfrac{4,48}{22,4}\) =0,2 (mol)
Suy ra: nNO=nN2O= 0,1 (mol)
nNH4NO3 =\(\dfrac{\text{0,1.2+0,2.3+0,3.2−0,1.3−0,1.8 }}{8}\)=0,0375 (mol) bảo toàn e nhe
mm′ = mCu(NO3)2+ mAl(NO3)3 +mMg(NO3)2+mNH4NO3 = 108,8(g) ( khúc này bảo toàn nguyên tố Cu,Al,Mg => số mol của muối Cu2+,Al3+,Mg2+ )

\(\left\{{}\begin{matrix}n_{N_2O}+n_{NO}=0,04\\44n_{N_2O}+30n_{NO}=18,5.2.0,04=1,48\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}n_{N_2O}=0,02\left(mol\right)\\n_{NO}=0,02\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}\%m_{N_2O}=\dfrac{0,02.44}{1,48}.100\%=59,46\%\\\%m_{NO}=\dfrac{0,02.30}{1,48}.100\%=40,54\%\end{matrix}\right.\)
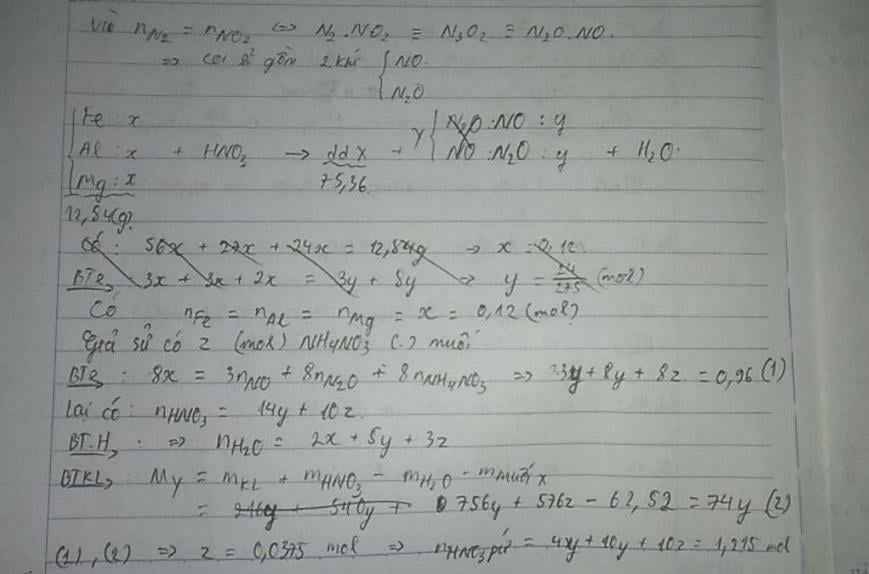

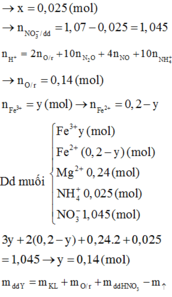
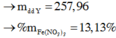

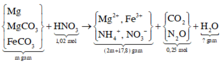
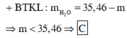
Đặt \(\hept{\begin{cases}x=n_{NO}\\y=n_{N_2}\end{cases}}\)
Sử dụng công thức \(P.V=n.R.T\Leftrightarrow1.0,9856=n.0,082.\left(27,3+273\right)\rightarrow n_{HH}=0,04mol\)
Lập hệ phương trình \(\hept{\begin{cases}x+y=0,04\\30x+28y=14,75.2.0,04\end{cases}}\)
\(\rightarrow\hept{\begin{cases}x=0,03mol\\y=0,01mol\end{cases}}\)
Đặt \(\hept{\begin{cases}a=n_{Fe}\\b=n_{Mg}\end{cases}}\)
Xét sự thay đổi e
\(Fe^0\rightarrow Fe^{+3}+3e\)
\(Mg^0\rightarrow Mg^{+2}+2e\)
\(N^{+5}+3e\rightarrow N^{+2}\)
\(2N^{+5}+10e\rightarrow2N^0\)
Có số mol e nhường = số mol e nhận
\(\Leftrightarrow3.n_{Fe}+2.n_{Mg}=3.n_{NO}+10.n_{N_2}\)
\(\Leftrightarrow3x+2y=3.0,03+10.0,01\)
Lệ hệ phương trình \(\hept{\begin{cases}56x+27y=2,88\\3x+2y=0,19\end{cases}}\)
\(\rightarrow\hept{\begin{cases}x=0,03mol\\y=0,05mol\end{cases}}\)
\(\%m_{Fe}=\frac{0,03.56.100}{2,88}=58,33\%\)
\(\%m_{Mg}=100-58,33=41,67\%\)