Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

$2Al + 6HCl \to 2AlCl_3 + 3H_2$
$Zn + 2HCl \to ZnCl_2 + H_2$
$n_{Al} = \dfrac{a}{27} (mol) \Rightarrow n_{H_2} = \dfrac{3}{2}n_{Al} = \dfrac{a}{18}(mol)$
$n_{Zn} = \dfrac{b}{65}(mol) \Rightarrow n_{H_2} = n_{Zn} = \dfrac{b}{65}(mol)$
$\Rightarrow \dfrac{a}{18} = \dfrac{b}{65}$
$\Rightarrow \dfrac{a}{b} = \dfrac{18}{65}$

Gọi \(n_{H_2}=x\)
\(2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\)
\(\dfrac{2}{3}x\) x ( mol )
\(Zn+H_2SO_4\rightarrow ZnSO_4+H_2\)
\(x\) x ( mol )
\(a:b=\dfrac{\dfrac{2}{3}x.27}{65x}=\dfrac{18x}{65x}=\dfrac{18}{65}\)

Giả sự đều sinh ra 1 mol H2
2Al+3H2SO4--->Al2(SO4)3+3H2
2/3_______________________1
=>a=2/3.27=18
Zn+H2SO4--->ZnSO4+H2
1___________________1
=>b=65
===> a/b=18/65

PTHH fe+2hcl =>fecl2 +h2
a) CM = n/v => v=n/CM =5,6/2=2,8 l
b) nFe=5,6/56=0,1 mol
ta có nFe=nH2 => nH2 =0,1 mol
=>vH2= nH2*22,4=0,1 *22,4 =2,24 l

Số mol của Fe:
n=\(\frac{m}{M}\) \(\frac{5,6}{56}\) =0,1(mol)
PTPƯ: Fe + 2HCl -> FeCl2 + H2
0,1 0,2 0,1
a) Thể tích của HCl :
VHCl= \(\frac{n}{CM}\) =\(\frac{0,2}{2}\) =0,1(lít)
b)Thể thích của hidro:
VH2 = 22,4 . 0,1 =2,24(lít)

PTHH : 2Al + 6HCl → 2AlCl3 + 3H2
Zn + 2HCl → ZnCl2 + H2
Vì thể tích khí H2 bằng nhau nên số mol khí H2 bằng nhau = x
Nhìn vào PTHH , ta thấy : nAl = \(\dfrac{2}{3}x\)
Ta có : mAl = n.M = \(\dfrac{2}{3}x\).27 = 18x ( g)
Lại có : nZn = \(n_{H_2}\) = x ⇒ mZn = n.M = 65x ( g)
⇒ \(\dfrac{a_1}{a_2}=\dfrac{18x}{65x}=\dfrac{18}{65}\)
⇒ mHCl = ( 3x + 2x).( 1 + 35,5) = 182,5x ( g)
P/s : T rất ngu hóa , làm bừa vậy thoy chứ chắc chắn sai , c nhờ mấy bác giỏi làm hộ ý :((
PTHH:
(1) Al + 2HCl → AlCl2 + H2
\(\dfrac{a_1}{27}mol\) x mol
(2) Zn + 2HCl → ZnCl2 + H2
\(\dfrac{a_2}{65}mol\) x mol
Theo ĐB ta có:
\(\dfrac{a_1}{27}\)=\(\dfrac{a_2}{65}\)
↔ \(\dfrac{a_1}{a_2}\)= \(\dfrac{27}{65}\)

Gọi \(\left\{{}\begin{matrix}n_{Al}=x\left(mol\right)\\n_{Fe}=y\left(mol\right)\end{matrix}\right.\)
\(n_{H_2}=\dfrac{4,48}{22,4}=0,2mol\)
\(2Al+6HCl\rightarrow2AlCl_3+3H_2\)
\(Fe+2HCl\rightarrow FeCl_2+H_2\)
Theo pt: \(\Rightarrow\left\{{}\begin{matrix}3x+y=0,2\\27x+56y=5,5\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}x=\dfrac{19}{470}\\y=\dfrac{37}{470}\end{matrix}\right.\)
\(\%m_{Al}=\dfrac{\dfrac{19}{470}\cdot27}{5,5}\cdot100\%=19,84\%\)
\(\%m_{Fe}=100\%-19,84\%=80,16\%\)

a, PT: \(Mg+2HCl\rightarrow MgCl_2+H_2\)
Ta có: \(n_{Mg}=\dfrac{7,2}{24}=0,3\left(mol\right)\)
Theo PT: \(n_{H_2}=n_{Mg}=0,3\left(mol\right)\)
\(\Rightarrow V_{H_2}=0,3.22,4=6,72\left(l\right)\)
b, PT: \(Fe_2O_3+3H_2O\underrightarrow{t^o}2Fe+3H_2O\)
Ta có: \(n_{Fe_2O_3}=\dfrac{19,2}{160}=0,12\left(mol\right)\)
Xét tỉ lệ: \(\dfrac{0,12}{1}>\dfrac{0,3}{3}\), ta được Fe2O3 dư.
Theo PT: \(n_{Fe}=\dfrac{2}{3}n_{H_2}=0,2\left(mol\right)\)
\(\Rightarrow m_{Fe}=0,2.56=11,2\left(g\right)\)
Bạn tham khảo nhé!
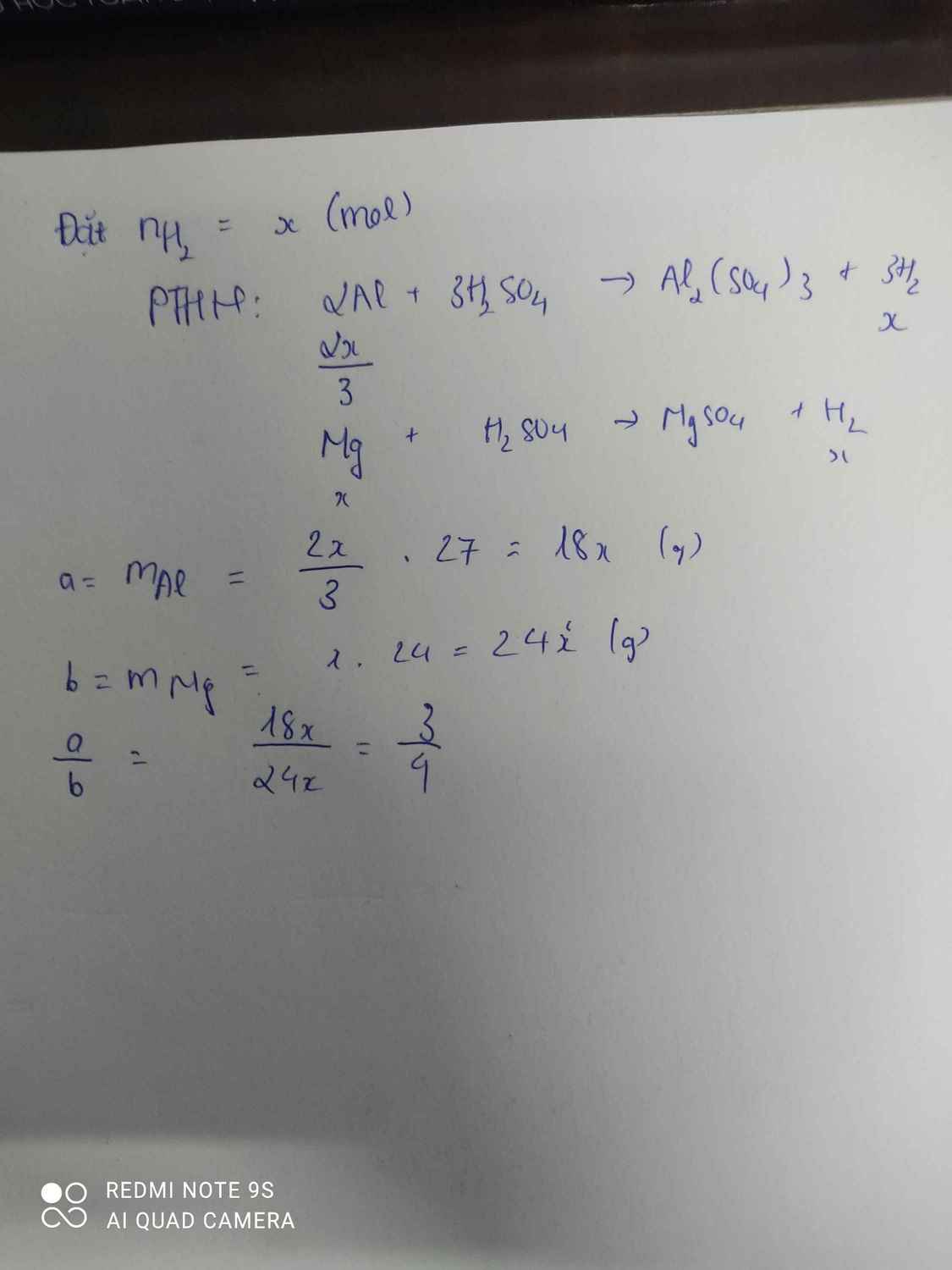
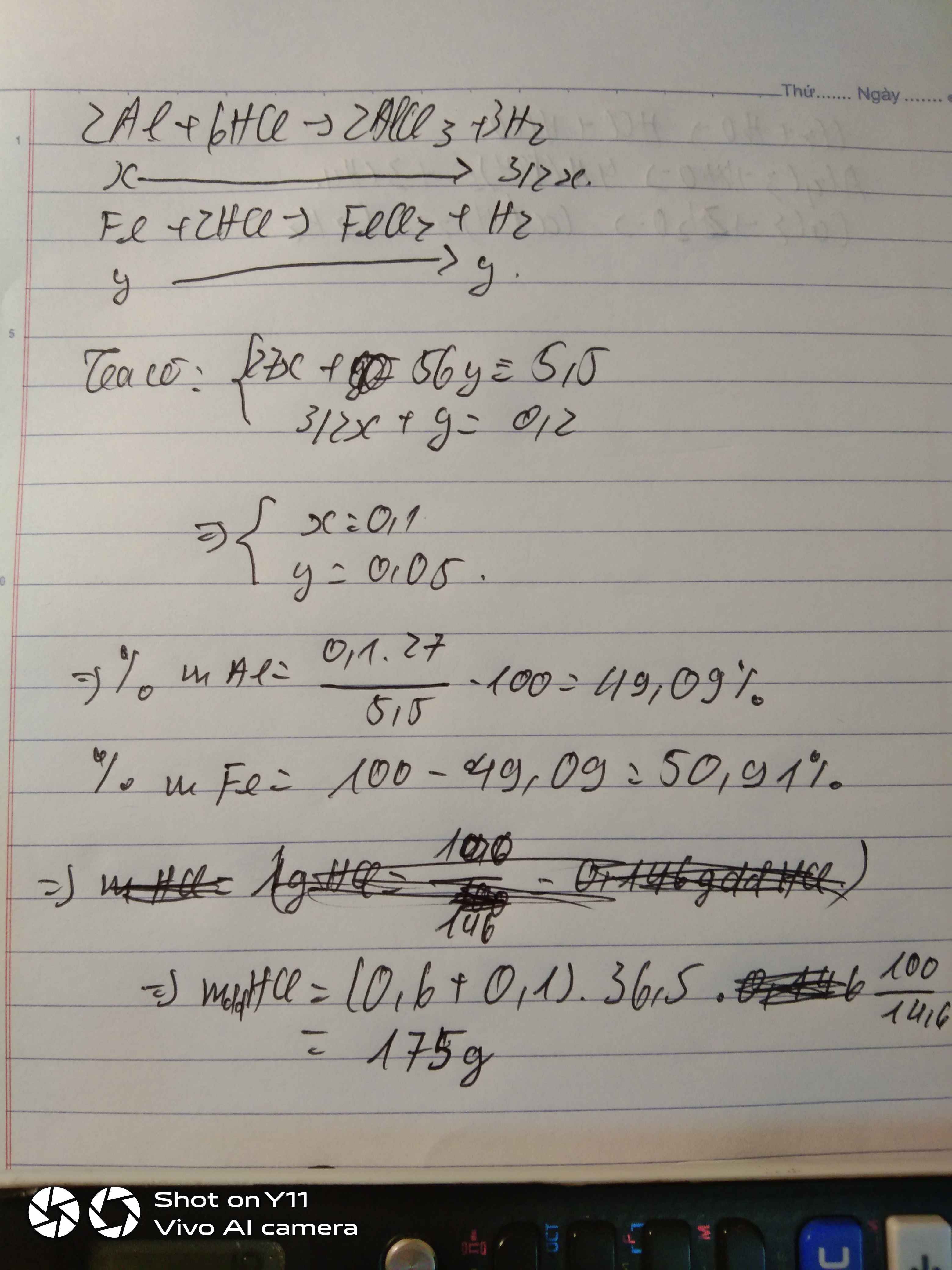
2Al+6HCl-->2AlCl3+3H2 (1)
Zn+2HCl-->ZnCl2+H2 (2)
Gọi số mol của H2 ở 2 pt là a(mol)
Số mol của Al là:
nAl=2/3nH2=2/3.a(mol)
K/lượng của Al là:
m=n.M=2/3a.27=18a(g)
Số mol của Zn là:
nZn=nH2=a(mol)
K/lượng của Zn là:
m=n.M=a.65(g)
Tỉ lệ a,b là:
a/b=mAl/mZn=18a/65a=18/65
Vậy tỉ lệ a/b là 18/65