Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Muối = Kim loại + gốc Cl
➝ Khối lượng của gốc Cl là: mCl = 49,8 - 14,3 = 35,5 gam
➝ nCl = nHCl = 35,5/35,5 = 1 mol
Khi viết phương trình ra sẽ thấy mối liên hệ: nHCl = 2nH2
➝ nH2 = 0,5 mol ➝ VH2 = 0,5.22,4 = 11,2 lít

a) nAl = 43,2/27 = 1,6 mol
2Al + 6HCl → 2AlCl3 + 3H2
1,6 \(\dfrac{1,6\times3}{2}=2,4\)
→ nH2 = 2,4 mol → VH2 = 2,4 x 22, 4 = 53,76 lít
b) nCuO = 64/80 = 0,8 mol
nH2 = 2,4 mol
→ H2 dư, phương trình tính theo số mol của CuO
CuO + H2 → Cu + H2O
0,8 0,8 0,8 0,8
Chất rắn sau phản ứng có Cu
mCu = 0,8 x 64 = 51,2 gam

\(n_{Ba}=\dfrac{24,66}{137}=0,18\left(mol\right)\\
pthh:Ba+2H_2O\rightarrow Ba\left(OH\right)_2+H_2\)
0,18 0,18
\(\Rightarrow V_{H_2}=0,18.22,4=4,032\left(L\right)\\
n_{CuO}=\dfrac{15,2}{80}=0,19\left(mol\right)\\
pthh:H_2+CuO\underrightarrow{t^o}Cu+H_2O\)
\(LTL:0,18< 0,19\)
=> CuO dư
theo pthh : \(n_{CuO\left(p\text{ư}\right)}=n_{Cu}=n_{H_2}=0,18\left(mol\right)\)
=> \(m_{Kl}=\left(64.0,18\right)+\left(80.0,1\right)=19,52\left(g\right)\)

a) PTHH: Zn + H2SO4 -> ZnSO4 + H2
H2 + CuO -to-> Cu + H2O
b) nH2=nZnSO4= nZn=0,3(mol)
nCuO=36/80=0,45(mol)
Ta có: 0,3/1 <0,45/1
=>H2 hết, CuO dư.
=> Sau phản ứng các chất thu được gồm có: ZnSO4, Cu và CuO(dư)
nCuO(P.ứ)=nCu=nH2=0,3(mol)
=> nCuO(dư)=0,45-0,3=0,15(mol)
mCuO(dư)=0,15.80=12(g)
mCu=0,3.64=19,2(g)
mZnSO4=0,3. 161= 48,3(g)

a) Mg + H2SO4 --> MgSO4 + H2
b) \(n_{Mg}=\dfrac{3}{24}=0,125\left(mol\right)\)
PTHH: Mg + H2SO4 --> MgSO4 + H2
0,125->0,125-->0,125-->0,125
=> VH2 = 0,125.22,4 = 2,8 (l)
\(V_{dd.H_2SO_4}=\dfrac{0,125}{2}=0,0625\left(l\right)\)
c) Sản phẩm là Magie sunfat và khí hidro
\(m_{MgSO_4}=0,125.120=15\left(g\right)\)
mH2 = 0,125.2 = 0,25 (g)
d)
\(n_{CuO}=\dfrac{16}{80}=0,2\left(mol\right)\)
PTHH: CuO + H2 --to--> Cu + H2O
Xét tỉ lệ: \(\dfrac{0,2}{1}>\dfrac{0,125}{1}\) => Hiệu suất tính theo H2
Gọi số mol CuO bị khử là a (mol)
PTHH: CuO + H2 --to--> Cu + H2O
a--->a-------->a
=> 16 - 80a + 64a = 14,4
=> a = 0,1 (mol)
=> nH2(pư) = 0,1 (mol)
=> \(H=\dfrac{0,1}{0,125}.100\%=80\%\)

a)\(n_{Fe}=\dfrac{16,8}{56}=0,3mol\)
\(Fe+2HCl\rightarrow FeCl_2+H_2\)
0,3 0,3 0,3
\(V_{H_2}=0,3\cdot22,4=6,67l\)
\(m_{FeCl_3}=0,3\cdot127=38,1g\)
b)\(n_{Fe_2O_3}=\dfrac{18}{160}=0,1125mol\)
\(Fe_2O_3+3H_2\rightarrow2Fe+3H_2O\)
0,1125 0,3 0 0
0,1 0,3 0,2 0,3
0,0125 0 0,2 0,3
\(m_{Fe}=0,2\cdot56=11,2g\)

\(n_{H_2}= \dfrac{8,96}{22,4} = 0,4(mol)\\ 2Al + 6HCl \to 2AlCl_3 + 3H_2\\ Fe + 2HCl \to FeCl_2 + H_2\\ m_{tăng} = m_{kim\ loại} - m_{H_2} = 11 - 0,4.2 = 10,2(gam)\)
PTHH: 2Al+6HCl→2AlCl3+3H2↑2Al+6HCl→2AlCl3+3H2↑
Fe+2HCl→FeCl2+H2↑Fe+2HCl→FeCl2+H2↑
Ta có: mH2=8,9622,4⋅2=0,8(g)<mhh=11(g)mH2=8,9622,4⋅2=0,8(g)<mhh=11(g)
⇒⇒ Sau p/ứ dd tăng 11−0,8=10,2(g)
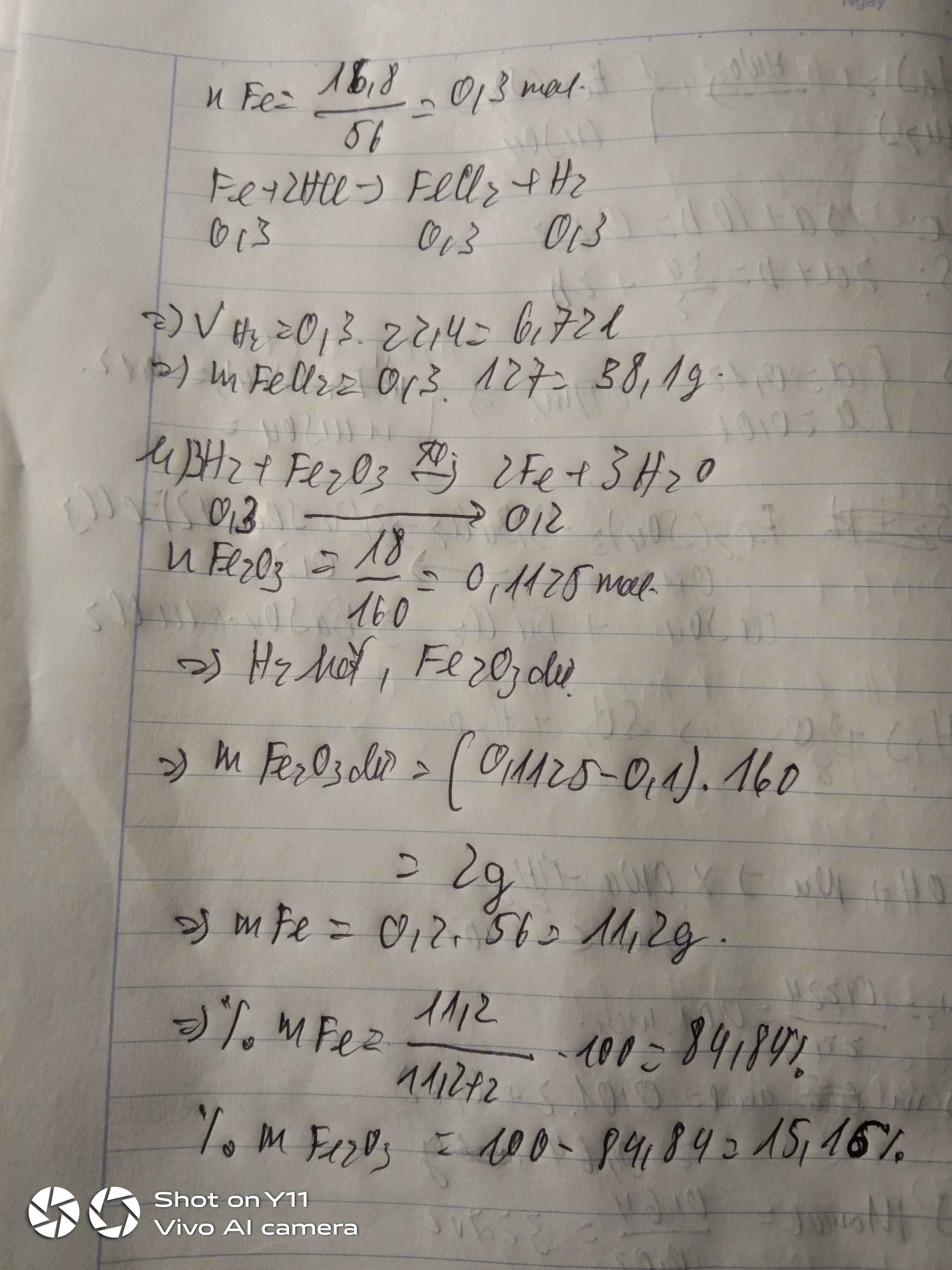
\(n_{Al}=\dfrac{5.4}{27}=0.2\left(mol\right)\)
\(2Al+6HCl\rightarrow2AlCl_3+3H_2\)
\(0.2........0.6.........0.2.........0.3\)
\(V_{dd_{HCl}}=\dfrac{0.6}{2}=0.3\left(l\right)\)
\(m_{AlCl_3}=0.2\cdot133.5=26.7\left(g\right)\)
\(V_{H_2}=0.3\cdot22.4=6.72\left(l\right)\)
\(n_{Fe_2O_3}=\dfrac{32}{160}=0.2\left(mol\right)\)
\(Fe_2O_3+3H_2\underrightarrow{^{t^0}}2Fe+3H_2O\)
\(1..............3\)
\(0.2............0.3\)
\(LTL:\dfrac{0.2}{1}>\dfrac{0.3}{3}\Rightarrow Fedư\)
\(m_{Cr}=m_{Fe_2O_3\left(dư\right)}+m_{Fe}=\left(0.2-0.1\right)\cdot160+0.2\cdot56=27.2\left(g\right)\)
a) 2Al + 6HCl $\to$ 2AlCl3 + 3H2
b)
n Al = 5,4/27 = 0,2(mol)
Theo PTHH : n HCl = 3n Al = 0,6(mol)
=> V = 0,6/2 = 0,3(lít)
n AlCl3 = n Al = 0,2(mol)
=> m = 0,2.133,5 = 26,7(gam)
c) n H2 = 1/2 n HCl = 0,3(mol)
n Fe2O3 = 32/160 = 0,2(mol)
$Fe_2O_3 + 3H_2 \xrightarrow{t^o} 2Fe + 3H_2O$
Ta thấy : n Fe2O3 /1 = 0,2 > n H2 /3 = 0,1 => Fe2O3 dư
Theo PTHH : n H2O = n H2 = 0,3(mol)
Bảo toàn khối lượng :
m Fe2O3 + m H2 = m chất rắn + m H2O
=> m chất rắn = 32 + 0,3.2 - 0,3.18 = 27,2 gam