Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(n_{HCl}=0,2.2=0,4\left(mol\right)\\ a.Zn+2HCl\rightarrow ZnCl_2+H_2\\ b.0,2........0,4.......0,2.......0,2\left(mol\right)\\ m=m_{Zn}=0,2.65=13\left(g\right)\\ c.m_{ZnCl_2}=136.0,2=27,2\left(g\right)\\ d.V_{H_2\left(đktc\right)}=0,2.22,4=4,48\left(l\right)\)

a,\(n_{Zn}=\dfrac{6,5}{65}=0,1\left(mol\right)\)
PTHH: Zn + 2HCl ---> ZnCl2 + H2
0,1--------------->0,1------>0,1
b, => \(\left\{{}\begin{matrix}C_{M\left(ZnCl_2\right)}=\dfrac{0,1}{\dfrac{6}{1000}}=\dfrac{50}{3}M\\V_{H_2}=0,1.22,4=2,24\left(l\right)\end{matrix}\right.\)
c, \(n_{O_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
PTHH: 2H2 + O2 --to--> 2H2O
LTL: \(\dfrac{0,1}{2}< 0,1\)=> O2 dư
Theo pt: \(n_{O_2}=\dfrac{1}{2}n_{H_2}=\dfrac{1}{2}.0,1=0,05\left(mol\right)\)
\(\Rightarrow\left\{{}\begin{matrix}m_{O_2\left(dư\right)}=\left(0,1-0,05\right).32=1,6\left(g\right)\\V_{O_2\left(dư\right)}=\left(0,1-0,05\right).22,4=1,12\left(l\right)\end{matrix}\right.\)

nZn= 13/65=0,2(mol)
a) PTHH: Zn + 2 HCl -> ZnCl2 + H2
b) nH2=nZnCl2=nZn=0,2(mol)
=>V(H2,đktc)=0,2 x 22,4= 4,48(l)
c) khối lượng muối sau phản ứng chứ nhỉ?
mZnCl2=136.0,2=27,2(g)

\(n_{Zn}=\dfrac{6,5}{65}=0,1\left(mol\right)\)
\(n_{CuO}=\dfrac{20}{80}=0,25\left(mol\right)\)
PTHH: Zn + 2HCl ---> ZnCl2 + H2
0,1---->0,1----------------->0,1
=> \(\left\{{}\begin{matrix}V_{H_2}=0,1.22,4=2,24\left(l\right)\\C_{M\left(HCl\right)}=\dfrac{0,2}{0,2}=1M\end{matrix}\right.\)
PTHH: CuO + H2 --to--> Cu + H2O
LTL: 0,25 > 0,1 => CuO dư
Theo pthh: nCu = nH2 = 0,1 (mol)
=> mCu = 0,1.64 = 6,4 (g)
\(n_{Zn}=\dfrac{6,5}{65}=0,1\left(mol\right)\\
pthh:Zn+2HCl\rightarrow ZnCl_2+H_2\)
0,1 0,2 0,2
\(V_{H_2}=0,2.22,4=4,48l\\
C_M=\dfrac{0,2}{0,2}=1M\\
n_{CuO}=\dfrac{20}{80}=0,25\left(G\right)\\
pthh:CuO+H_2\underrightarrow{t^o}Cu+H_2O\\
LTL:0,25>0,1\)
=>CuO dư
\(n_{Cu}=n_{H_2}=0,1\left(mol\right)\\
m_{Cu}=0,1.64=6,4g\)

a) Lập công thức hóa học của muối kẽm clorua: Z n C l 2
b) Khối lượng muối Z n C l 2 = 6,5 + 7,3 – 0,2 = 13,6 (gam)

\(a,n_{Zn}=\dfrac{1,3}{65}=0,02\left(mol\right)\)
PTHH: Zn + H2SO4 ---> ZnSO4 + H2
0,02--->0,02--------->0,02----->0,02
b, mZnSO4 = 0,02.161 = 3,22 (g)
c, VH2 = 0,02.22,4 = 0,448 (l)
d, \(m_{ddH_2SO_4}=\dfrac{0,02.98}{10\%}=19,6\left(g\right)\)
e, mdd = 19,6 + 1,3 - 0,02.2 = 20,86 (g)
=> \(C\%_{ZnSO_4}=\dfrac{0,02.161}{20,86}.100\%=15,44\%\)

a, \(n_{Zn}=\dfrac{13}{65}=0,2\left(mol\right)\)
PT: \(Zn+2HCl\rightarrow ZnCl_2+H_2\)
Theo PT: \(n_{H_2}=n_{Zn}=0,2\left(mol\right)\Rightarrow V_{H_2}=0,2.22,4=4,48\left(l\right)\)
b, \(n_{HCl}=2n_{Zn}=0,4\left(mol\right)\Rightarrow m_{HCl}=0,4.36,5=14,6\left(g\right)\)
c, \(n_{Fe_2O_3}=\dfrac{16}{160}=0,1\left(mol\right)\)
PT: \(Fe_2O_3+3H_2\underrightarrow{t^o}2Fe+3H_2O\)
Xét tỉ lệ: \(\dfrac{0,1}{1}>\dfrac{0,2}{3}\), ta được Fe2O3 dư.
Theo PT: \(n_{Fe}=\dfrac{2}{3}n_{H_2}=\dfrac{2}{15}\left(mol\right)\Rightarrow m_{Fe}=\dfrac{2}{15}.56=\dfrac{112}{15}\left(g\right)\)

a. Zn + 2HCl → ZnCl2 + H2
b. nZn = n\(_{ZnCl_2}\) =\(\dfrac{13}{65}=0,2\left(mol\right)\) => m\(_{ZnCl_2}\)= 0,2.136 = 27,2(g)
c. n\(_{H_2}\)= nZn = 0,2 (mol) => V\(_{H_2}\)=0,2.22,4 = 4,48 (lít)

a)
\(Zn + 2HCl \to ZnCl_2 + H_2\)
b),c)
Theo PTHH :
\(n_{ZnCl_2} = n_{H_2} = n_{Zn} = \dfrac{13}{65} = 0,2(mol)\)
Vậy :
\(m_{ZnCl_2} = 0,2.136 = 27,2(gam)\\ V_{H_2} =0,2.22,4 = 4,48(lít)\)
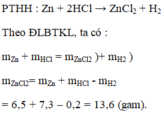
\(PTHH:Zn+2HCl->ZnCl_2+H_2\)
0,05--->0,1----->0,05----->0,05
\(n_{Zn}=\dfrac{m}{M}=\dfrac{3,25}{65}=0,05\left(mol\right)\)
\(m_{ZnCl_2}=n\cdot M=0,05\cdot\left(65+35,5\cdot2\right)=6,8\left(g\right)\)
\(V_{H_2\left(dktc\right)}=n\cdot22,4=0,05\cdot22,4=1,12\left(l\right)\)
mình k hiểu lắm phần
0,05--->0,1----->0,05----->0,05
bạn gt được không ạ