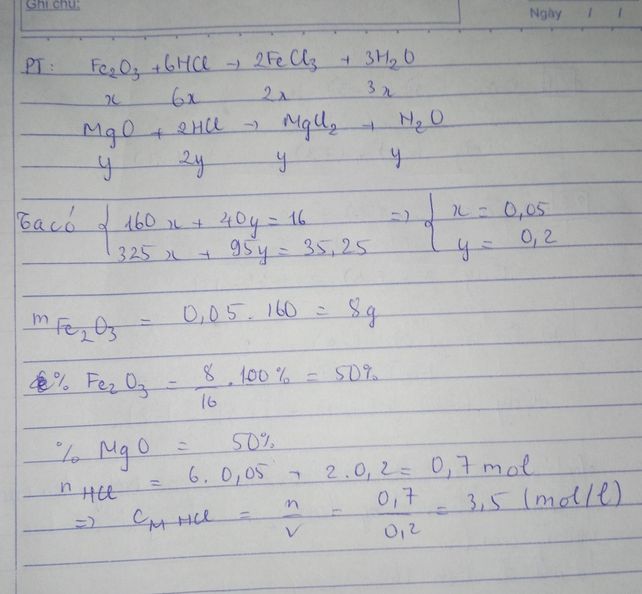Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

dạ em cảm ơn anh/thầy nhưng mà cái tổng HCl ra m bấm máy sai rồi ạ vs cảm ơn anh/thầy giúp em giải bài nha

Gọi số mol Zn và Fe là x và y.
PTHH:
Zn + 2HCl => ZnCl2 + H2
x 2x x x
Fe + 2HCl => FeCl2 + H2
y 2y y y
Khối lượng hỗn hợp ban đầu là 17.7 g => 65x + 56y = 17.7 (1)
Số mol khí hidro là: 6.72 : 22,4 = 0.3 mol suy ra x + y = 0.3 (2)
giải hệ (1) và (2) ta được: x = 0.1 và y = 0.2 (mol)
Suy ra % khối lượng Zn trong hỗn hợp ban đầu là: %mZn = \(\dfrac{65.01}{65.0,1+56.0,2}\)= 36.7%
% khối lượng Fe trong hỗn hợp ban đầu là: 100% - 36.7% = 63.3%

Zn +2 HCl ---> ZnCl2 + H2
0,1-----0,2----------0,1-------------0,1 mol
ZnO + 2HCl ---> ZnCl2 + H2O
0,2------0,4-------0,2--------0,2
n H2=\(\dfrac{2,24}{22,4}=0,1mol\)
=>m Zn=0,1.65=6,5g
=>m HCl(1)=0,2.36,5=7,3g
=>m HCl(2)=14,6g -> nHCl=0,4 mol
=>%m Zn=\(\dfrac{6,5}{6,5+14,4}.100=31,1\%\)
=>%m ZnO=68,9%
b)
->m HCl=0,6.36,5=21,9g
->m ZnCl2=0,3.136=40,8g

\(n_{H_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\\ pthh:Mg+2HCl\rightarrow MgCl_2+H_2\)
0,2 0,2
\(MgO+2HCl\rightarrow MgCl_2+H_2O\)
\(m_{Mg}=0,2.24=4,8g\\ m_{MgO}=18,4-4,8=13,6g\)

Gọi số mol Na, Zn là a, b
=> 23a + 65b = 14,3
\(n_{H_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
- Nếu Zn tan hết
PTHH: 2Na + 2H2O --> 2NaOH + H2
______a-------------------->a---->0,5a
2NaOH + Zn --> Na2ZnO2 + H2
__2b<----b-------------------->b
=> \(\left\{{}\begin{matrix}2b\le a\\0,5a+b=14,3\end{matrix}\right.\) => Loại
=> Zn không tan hết => NaOH hết
PTHH: 2Na + 2H2O --> 2NaOH + H2
______a------------------->a---->0,5a
2NaOH + Zn --> Na2ZnO2 + H2
_a--------------------------->0,5a
=> 0,5a + 0,5a = 0,1
=> a = 0,1
=> mNa = 0,1.23 = 2,3 (g)
=> mZn = 14,3 - 2,3 = 12(g)

a) Gọi n Zn = a(mol) ; n ZnO = b(mol)
=> 65a + 81b = 14,6(1)
$Zn + 2HCl \to ZnCl_2 + H_2$
$ZnO + 2HCl \to ZnCl_2 + H_2O$
n ZnCl2 = a + b = 27,2/136 = 0,2(2)
Từ (1)(2) suy ra : a = b = 0,1
%m Zn = 0,1.65/14,6 .100% = 44,52%
%m ZnO = 100% -44,52% = 55,45%
b)
n HCl = 2n Zn + 2n ZnO = 0,4(mol)
m dd HCl = 0,4.36,5/7,3% = 200(gam)

Ở phần b, nếu trong hỗn hợp đầu thì phải là % khối lượng mỗi oxit chứ nhỉ? Và ở phần c phải là 1,1 g/ml chứ không phải g/mol bạn nhé!


Bạn tham khảo link nhé!
một hỗn hợp gồm Fe2O3 và MgO nặng 16g được hòa tan hết trong udng dịch axit HCL sau đó đem cô cạn dung dịch thu được 35,25g muối khan a) viết các PTHH b) tính thành phần % khối lượng mỗi oxit trong hỗn hợp ban đầu >< giúp với ạ - Hoc24