Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Bài 1:
A + Cl2 → ACl2 (1)
Fe + ACl2 → FeCl2 + A (2)
x x x (mol)
gọi số mol của Fe phản ứng với một số mol của ACl2 là x
khối lương thanh sắt sau phản ứng là:11,2 - 56x + xMA = 12
=> x =
Ta có:
= 0,25.0,4 = 0,1 (mol)
=> MA = 64 g/mol; Vậy kim loại A là Cu
= nCu =
= 0,2 (mol) =>
= 0,5M
bài 2:
(C17H35COO)3C3H5 + 3NaOH -> 3 C17H35COONa + C3H5(OH)3
890 kg 918 kg
x kg 720 kg
=> x = 698,04 kg.

a) Đặt \(\hept{\begin{cases}n_{Al}=x\left(mol\right)\\n_{Cu}=y\left(mol\right)\end{cases}}\)
PTHH : \(2Al+3H_2SO_4-->Al_2\left(SO_4\right)_3+3H_2\) (1)
\(Al+6HNO_3-->Al\left(NO_3\right)_3+3NO_2+3H_2O\) (2)
\(Cu+4HNO_3-->Cu\left(NO_3\right)_2+2NO_2+2H_2O\) (3)
Theo pthh (1) : \(n_{Al}=\frac{2}{3}n_{H_2}=0,2\left(mol\right)\) => \(x=0,2\left(mol\right)\)
Theo ptr (2); (3) : \(n_{NO_2}=3n_{Al}+2n_{Cu}\)
=> \(0,8=0,2\cdot3+2\cdot n_{Cu}\)
=> \(n_{Cu}=0,1\left(mol\right)\)
=> \(a=0,2\cdot27+0,1\cdot64=11,8\left(g\right)\)
b) PTHH : \(NH_3+HNO_3-->NH_4NO_3\) (4)
\(3NH_3+3H_2O+Al\left(NO_3\right)_3-->Al\left(OH\right)_3\downarrow+3NH_4NO_3\) (5)
\(2NH_3+2H_2O+Cu\left(NO_3\right)_2-->Cu\left(OH\right)_2\downarrow+2NH_4NO_3\) (6)
BT Al : \(n_{Al\left(OH\right)_3}=n_{Al}=0,2\left(mol\right)\)
BT Cu : \(n_{Cu\left(OH\right)_2}=n_{Cu}=0,1\left(mol\right)\)
=> \(m\downarrow=m_{Al\left(OH\right)_3}+m_{Cu\left(OH\right)_2}=25,4\left(g\right)\)
c) Gọi tên KL là X .
PTHH : \(2Al\left(NO_3\right)_3-t^o->Al_2O_3+6NO_2+\frac{3}{2}O_2\) (7)
\(Cu\left(NO_3\right)_2-t^o->CuO+2NO_2+\frac{1}{2}O_2\) (8)
\(4NO_2+O_2+2H_2O-->4HNO_3\) (9)
\(3X+4nHNO_3-->3X\left(NO_3\right)_n+nNO+2nH_2O\) (10)
viết ptr rồi, nhưng mik có thắc mắc là cho khí B hấp thụ vô nước => tính đc số mol của hno3, rồi áp vô X là ra, nhưng đề lại cho số mol NO =((( hoặc có thể dùng số mol NO để tính nhưng như thế có hơi thừa ko ? tính ra theo 2 cách thì cx ra 2 kq khác nhau ? ai githich giùm mik, hay mik tính sai hoặc phân tích đề sai nhỉ ?? :D

Bạn bấn vào đây, có người hỏi bài này rồi nhá Câu hỏi của Mạc Nhược Ca - Hóa học lớp 12 | Học trực tuyến

Đáp án B
Cho 5,52 gam Mg, Al tác dụng với 0,54 mol NaHSO4 và 0,08 mol HNO3 thu được dung dịch X chỉ chứa muối trng hòa và hỗn hợp Y gồm 3 khí không màu
Ta có: M Y ¯ = 15 , 75
do vậy Y có H2, N2 và N2O
Cho NaOH dư vào X thu được kết tủa là Mg(OH)2
![]()
Do dung dịch X chứa chứa muối trung hòa nên H+ hết, mặt khác do sinh ra khí H2 nên NO3- hết.
Dung dịch X sẽ chứa Mg2+ 0,14 mol, Al3+ 0,08 mol, NH4+, Na+ 0,54 mol và SO42-0,54 mol.
Bảo toàn điện tích: ![]()
Bảo toàn N:
![]()
Gọi số mol N2, N2O và H2 lần lượt là a, b,c => a + b = 0,03
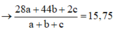
Bảo toàn e: 10a + 8b + 2c + 0,02.8 = 0,14.x + 0,08.3
Giải hệ: a=0,01; b=0,02; c=0,05
→ % H 2 = 7,94%
 với các chất sau:
với các chất sau:
Chọn đáp án B
gt ⇒ Z gồm N2O, N2, H2 ⇒ Y không chứa NO3–; khí có PTK lớn nhất trong Z là N2O.
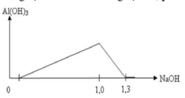
Từ 1 mol NaOH đến 1,3 mol NaOH thì kết tủa từ cực đại đến tan hết do xảy ra phản ứng:
Al(OH)3 + NaOH → NaAlO2 + 2H2O ⇒ nAl3+ = nAl(OH)3 = 1,3 - 1 = 0,3 mol.
Đặt nNaHSO4 = x ⇒ nNa+/Y = nSO42– = x. Khi kết tủa đạt cực đại thì chỉ thu được Na2SO4.
⇒ nNa2SO4 = x ⇒ ∑nNa+ = 2x ⇒ nNa+/Y = 2x - 1 = x ⇒ x = 1.
Đặt nNH4+ = y; nH+ = z. Bảo toàn điện tích: 0,3 × 3 + 1 + y + z = 1 × 2
mmuối = 127,88(g) = 0,3 × 27 + 1 × 23 + 18y + z + 1 × 96
Giải hệ có: y = 0,04 mol; z = 0,06 mol. Bảo toàn khối lượng:
mH2O = 10,92 + 1 × 120 + 0,09 × 63 - 127,88 - 0,08 × 20 = 7,11g ⇒ nH2O = 0,395 mol.
Bảo toàn nguyên tố Hidro: nH2 = (1 + 0,09 - 0,04 × 4 - 0,06 - 0,395 × 2)/2 = 0,04 mol.
Đặt nN2O = a; nN2 = b ⇒ nZ = a + b + 0,04 = 0,08; mZ = 44a + 28b + 0,04 × 2 = 0,08 × 20
Giải hệ có: a = 0,025 mol; b = 0,015 mol ⇒ %mN2O = 0,025 × 44 ÷ 1,6 × 100% = 68,75%.