Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Oxi tác dụng với canxi:\(2Ca+O_2\underrightarrow{t^0}2CaO\)
Oxi tác dụng với nhôm:\(2Al+3O_2\underrightarrow{t^o}Al_2O_3\)
Oxi tác dụng với kẽm:\(2Zn+O_2\underrightarrow{t^o}2ZnO\)
Oxi tác dụng với đồng:\(2Cu+O_2\underrightarrow{t^o}2CuO\)
Oxi tác dụng với cacbon:\(C+O_2\underrightarrow{t^o}CO_2\)
Oxi tác dụng với lưu huỳnh:\(S+O_2\underrightarrow{t^o}SO_2\)
Oxi tác dụng với photpho:\(4P+5O_2\underrightarrow{t^o}2P_2O_5\)

\(2Ca+O_2\underrightarrow{t^o}2CaO\)
\(2Cu+O_2\underrightarrow{t^o}2CuO\)
\(2Al+3O_2\underrightarrow{t^o}Al_2O_3\)
\(2Zn+O_2\underrightarrow{t^o}2ZnO\)
\(C+O_2\underrightarrow{t^o}CO_2\)
\(S+O_2\underrightarrow{t^o}SO_2\)
\(4P+5O_2\underrightarrow{t^o}2P_2O_5\)
Oxi tác dụng với canxi:2Ca+O2t0→2CaO2Ca+O2t0→2CaO
Oxi tác dụng với nhôm:2Al+3O2to→Al2O32Al+3O2to→Al2O3
Oxi tác dụng với kẽm:2Zn+O2to→2ZnO2Zn+O2to→2ZnO
Oxi tác dụng với đồng:2Cu+O2to→2CuO2Cu+O2to→2CuO
Oxi tác dụng với cacbon:C+O2to→CO2C+O2to→CO2
Oxi tác dụng với lưu huỳnh:S+O2to→SO2S+O2to→SO2
Oxi tác dụng với photpho:4P+5O2to→2P2O5

1) 2Ca + O2 -to-➢ 2CaO
2) 4Al + 3O2 -to-➢ 2Al2O3
3) 2Zn + O2 -to-➢ 2ZnO
4) 2Cu + O2 -to-➢ 2CuO
5) C + O2 -to-➢ CO2
6) S + O2 -to-➢ SO2
7) 4P + 5O2 -to-➢ 2P2O5

$S + O_2 \xrightarrow{t^o} SO_2$
$3Fe + 2O_2 \xrightarrow{t^o} Fe_3O_4$
$C + O_2 \xrightarrow{t^o} CO_2$
$4P + 5O_2 \xrightarrow{t^o} 2P_2O_5$
$4Al + 3O_2 \xrightarrow{t^o} 2Al_2O_3$
$2Zn + O_2 \xrightarrow{t^o} 2ZnO$
$4K + O_2 \xrightarrow{t^o} 2K_2O$
$CH_4 + 2O_2 \xrightarrow{t^o} CO_2 + 2H_2O$
$C_2H_6O + 3O_2 \xrightarrow{t^o} 2CO_2 + 3H_2O$

\(c,2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\\ Fe+H_2SO_4\rightarrow FeSO_4+H_2\\ Mg+H_2SO_4\rightarrow MgSO_4+H_2\\ Cu+H_2SO_4\rightarrow CuSO_4+H_2\\ Zn+H_2SO_4\rightarrow ZnSO_4+H_2\\ 2Ag+H_2SO_4\rightarrow Ag_2SO_4+H_2\)
\(a,O_2+4K\underrightarrow{t^o}2K_2O\\ 2Mg+O_2\underrightarrow{t^o}2MgO\\ C+O_2\underrightarrow{t^o}CO_2\\ 2C+O_2\underrightarrow{t^o}2CO\\ 4P+5O_2\underrightarrow{t^o}2P_2O_5\\ 4P+3O_2\underrightarrow{t^o}2P_2O_3\\ 2Cu+O_2\underrightarrow{t^o}2CuO\\ 4Cu+O_2\underrightarrow{t^o}2Cu_2O\\ 4Ag+O_2\underrightarrow{t^o}2Ag_2O\)
\(b,Al_2O_3+3H_2\underrightarrow{t^o}2Al+3H_2O\\ FeO+H_2\underrightarrow{t^o}Fe+H_2O\\ CaO+H_2\underrightarrow{t^o}Ca+H_2O\\ BaO+H_2\underrightarrow{t^o}Ba+H_2O\\ Ag_2O+H_2\underrightarrow{t^o}2Ag+H_2O\\ P_2O_5+5H_2\underrightarrow{t^o}2P+5H_2O\)

Các oxit tác dụng với nước: N a 2 O , P 2 O 5 , C O 2 , S O 3
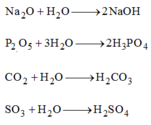
- Các oxit không hòa tan trong nước: CuO, MgO, A l 2 O 3 .

1.
Cách 2 và 3 vì cách 2 là tăng diện tích tiếp xúc,cách 3 là tăng oxi để sự cháy diễn ra mãnh liệt hơn.
2.
2Ca + O2 \(\rightarrow\)2CaO
4Al + 3O2\(\underrightarrow{t^o}\)2Al2O3
2Zn + O2\(\underrightarrow{t^o}\)2ZnO
2Cu + O2\(\underrightarrow{t^o}\)2CuO
C + O2\(\underrightarrow{t^o}\)CO2
S + O2\(\underrightarrow{t^o}\)SO2
4P + 5O2\(\underrightarrow{t^o}\)2P2O5
2Ca + O2 --to-> 2CaO;
2Al + 3 O2 ---to--> Al2O3;
2Zn + O2 ---to-> 2ZnO;
2Cu + O2 --to-> 2CuO;
C + O2 --to--> CO2;
S + O2 ---to-> SO2;
4P + 5O2 --to-> 2P2O5.
Các pư với oxi đều có nhiệt độ hết nha pn.
Bạn ơi câu Oxi tác dụng với Al bạn cân bằng phương trình sai rồi, phải là: 4Al +3O2----> 2Al2O3