Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a) 2HCl+Fe--->FeCl2+H2, 2HCl+Zn--->ZnCl2+H2, 6HCl+2Al--->2AlCl3+3H2
b) HCl+NaOH---->NaCl+H2O, 2HCl+CuO--->CuCl2+H2O, HCl+AgNO3--->AgCl+HNO3
chúc bạn học giỏi nhé.

a)
a)
Những ví dụ phương trình phản ứng hóa học của axit clohiđric là phản ứng oxi hóa – khử:
+ Với vai trò là chất khử:
\(K_2Cr_2O_7+14HCl\rightarrow2KCl+2CrCl_3+3Cl_2+7H_2O\)
+ Với vai trò chất oxi hóa:
\(Fe+HCl\rightarrow FeCl_2+H_2\)
b) Axit clohidric tham gia phản ứng không oxi hóa - khử
\(CaCO_3+2HCl\rightarrow CaCl_2+CO2\uparrow+H_2O\)
a)-Chất khử:
\(K_2Cr_2O_7+14HCL\rightarrow2KCL+2CrCl_3+3Cl_2+7H_2O\)
\(PbO_2+4HCL\rightarrow PbCl_2+Cl_2=2H_2O\)
-Oxy hóa:
\(Fe+2HCL\rightarrow FeCl_2+H_2\)

Những ví dụ phương trình phản ứng hóa học của axit clohidric là không phải là phản ứng oxi hóa – khử:
CaCO3 + 2HCl → CaCl2 + CO2 + H2O.
CuO + 2HCl → CuCl2 + H2O.

a) Dung dịch axit sunfuric loãng có những tính chất chung của axit, đó là:
- Đổi màu quỳ tím thành đỏ.
- Tác dụng với kim loại giải phóng hiđro.
Fe + H2SO4 → FeSO4 + H2
- Tác dụng với oxit bazơ và bazơ
Ba(OH)2 + H2SO4 → BaSO4 + 2H2O
- Tính chất với nhiều chất muối
BaCl2 + H2SO4 → BaSO4 +2HCl
b) Tính chất hóa học đặc trưng của axit sunfuric đặc là tính oxi hóa mạnh và tính háo nước.
- Tính chất oxi hóa mạnh
2H2SO4 + Cu → CuSO4 + SO2 + 2H2O
2H2SO4 + S → 3SO2 + 2H2O
2H2SO4 + 2KBr → Br2 + SO2 + 2H2O + K2SO4
- Tính háo nước và tính chất oxi hóa
Axit sunfuric đặc háp thụ mạnh nước. Axit sunfuric đặc chiếm các nguyên tử H và O là những nguyên tố thành phần của các hợp chất gluxit giải phóng cacbon và nước.
C12H22O11 → 12C + 11H2O.
Da thịt tiếp xúc với H2SO4 đặc sẽ bị bỏng rất nặng, vì vậy khi sử dụng axit sunfuric phải hết sức thận trọng
a) Dung dịch axit sunfuric loãng có những tính chất chung của axit, đó là:
- Đổi màu quỳ tím thành đỏ.
- Tác dụng với kim loại giải phóng hiđro.
Fe + H2SO4 \(\rightarrow\) FeSO4 + H2
- Tác dụng với oxit bazơ và bazơ
Ba(OH)2 + H2SO4 \(\rightarrow\) BaSO4 + 2H2O
- Tính chất với nhiều chất muối
BaCl2 + H2SO4 \(\rightarrow\) BaSO4 +2HCl
b) Tính chất hóa học đặc trưng của axit sunfuric đặc là tính oxi hóa mạnh và tính háo nước.
- Tính chất oxi hóa mạnh
2H2SO4 + Cu \(\rightarrow\) CuSO4 + SO2 + 2H2O
2H2SO4 + S \(\rightarrow\) 3SO2 + 2H2O
2H2SO4 + 2KBr \(\rightarrow\) Br2 + SO2 + 2H2O + K2SO4
- Tính háo nước và tính chất oxi hóa
Axit sunfuric đặc háp thụ mạnh nước. Axit sunfuric đặc chiếm các nguyên tử H và O là những nguyên tố thành phần của các hợp chất gluxit giải phóng cacbon và nước.
C12H22O11 \(\rightarrow\) 12C + 11H2O.
Da thịt tiếp xúc với H2SO4 đặc sẽ bị bỏng rất nặng, vì vậy khi sử dụng axit sunfuric phải hết sức thận trọng.

a) Oxi và ozon đều có tính oxi hóa.
(1) Tác dụng với kim loại, oxi tác dụng với hầu hết các kim loại trừ Pt, Au, Ag... còn ozon tác dụng với hầu hết các kim loại trừ Au và Pt.
3Fe + 2O2 tocao→→tocao Fe3O4
2Ag + O3 -> Ag2O + O2
(2) Tác dụng với phi kim.
4P + 5O2 -> 2P2O5
2C + 2O3 -> 2CO2 + O2
(3) Tác dụng với nhiều hợp chất vô cơ, hữu cơ :
C2H5OH + 3O2 -> 2CO2 + 3H2O
2H2S + 3O2 -> 2SO2 + 2H2O
b) Ozon có tính oxi hóa mạnh hơn oxi.
- Oxi không tác dụng được với Ag, nhưng Ozon tác dụng được :
2Ag + O3 -> Ag2O + O2
O2 không oxi hóa được I- nhưng O3 oxi hóa được thành I2 :
2KI + O3 + H2O -> I2 + 2KOH + O2
-So với phân tử O2, phân tử O3 kém bền , dễ bị phân hủy .
O3 -> O2 + O ; 2O -> O2
Oxi dạng nguyên tử hoạt động mạnh hơn oxi dạng phân tử nên ozon hoạt động mạnh hơn oxi.
a) Oxi và ozon đều có tính oxi hóa.
(1) Tác dụng với kim loại, oxi tác dụng với hầu hết các kim loại trừ Pt, Au, Ag... còn ozon tác dụng với hầu hết các kim loại trừ Au và Pt.
3Fe + 2O2 tocao→→tocao Fe3O4
2Ag + O3 -> Ag2O + O2
(2) Tác dụng với phi kim.
4P + 5O2 -> 2P2O5
2C + 2O3 -> 2CO2 + O2
(3) Tác dụng với nhiều hợp chất vô cơ, hữu cơ :
C2H5OH + 3O2 -> 2CO2 + 3H2O
2H2S + 3O2 -> 2SO2 + 2H2O
b) Ozon có tính oxi hóa mạnh hơn oxi.
- Oxi không tác dụng được với Ag, nhưng Ozon tác dụng được :
2Ag + O3 -> Ag2O + O2
O2 không oxi hóa được I- nhưng O3 oxi hóa được thành I2 :
2KI + O3 + H2O -> I2 + 2KOH + O2
-So với phân tử O2, phân tử O3 kém bền , dễ bị phân hủy .
O3 -> O2 + O ; 2O -> O2
Oxi dạng nguyên tử hoạt động mạnh hơn oxi dạng phân tử nên ozon hoạt động mạnh hơn oxi.

Những ví dụ phương trình phản ứng hóa học của axit clohidric là phản ứng oxi hóa – khử:
Với vai trò là chất khử:
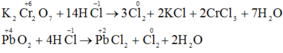
Với vai trò là chất oxi hóa :
Mg + 2HCl → MgCl2 + H2

Những cặp chất xảy ra phản ứng oxi hoá - khử :
(1)
(2) MnO2 + 4HCl > MnCl2 + Cl2 + 2H2O
b) Trong phản ứng (1) :
- Nguyên tử hiđro nhường electron là chất khử, sự nhường electron của H2 được gọi là sự oxi hoá nguyên tử hiđro.
- Ion đồng nhận electron, là chất oxi hoá. Sự nhận electron của ion đồng được gọi là sự khử ion đồng.
Trong phản ứng (2) :
- Ion Clo nhường electron là chất khử. Sự nhường electron của Cl được gọi là sự oxi hoá ion clo.
- Ion Mn nhận electron là chất oxi hoá. Sự nhận electron của ion Mn được gọi là sự khử ion Mn.

a) S + O2 → SO2 (Dựa vào tính khử của S)
SO2 + 2H2S → 2S + 2H2O (Dựa vào tính oxi hóa của SO2)
b) Tính khử của SO2
SO2 do nhà máy thải vào khí quyển. Nhờ xúc tác là oxit kim loại có trong khói bụi của nhà máy, nó bị O2 của không khí oxi hóa thành SO3
2SO2 + O2 → 2SO3
SO3 tác dụng với nước mưa thành mưa axit tạo ra H2SO4. Tính axit của H2SO4 đã phá hủy những công trình được xây bằng đá, thép.

a) Khí H2S và axit sunfuric đặc tham gia các phản ứng oxi hóa – khử thì khí H2S chỉ thể hiện tính khử còn H2SO4 chỉ thể hiện thính oxi hóa. Vì trong H2S số oxi hóa của (S-2) chỉ có thể tăng, trong H2SO4 số oxi hóa (S+6) chỉ có thể giảm.
b) Phương trình phản ứng hóa học:
2H2S + O2 -> 2H2O + 2S.
2 H2SO4 + Cu -> CuSO4 + SO2 + 2H2O
2 H2SO4 + KBr -> Br2 + SO2 + 2H2O + K2SO4
Những phương trình phản ứng hóa học chứng minh:
a) Axit clohiđric tham gia phản ứng oxi hóa – khử với vai trò là chất khử:
b) Axit clohiđric tham gia phản ứng không oxi hóa – khử:
CaCO3 + 2HCl \(\rightarrow\) CaCl2 + CO2 + H2O.
CuO + 2HCl \(\rightarrow\) CuCl2 + H2O.