Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

1/ Gọi x, y lần lượt là số mol của Na2CO3 và KHCO3.
Khi cho từ từ HCl vào dung dịch A thì các phản ứng xảy ra lần lượt là :
CO3^2- + H^+ => HCO3-
x ---------> x ----------> x
HCO3^- + H+ => H2O + CO2.
0,045 <--- 0,045 <-------- 0,045
.........HCO3^- + OH- => CO3^2- + H2O.
x+y - 0,045 -------------> x+y-0,045.
Giải hệ: x+y-0,045 = 29,55/197; n HCl = x+ 0,045 = 0,15.
=> x = 0,105 ; y = 0,09.
2/ Nồng độ của HCO3- , CO3^2- lần lượt là 0,225 M; 0,2625 M.
3/ Cho từ từ dung dịch A vào bình đựng 100 ml dung dịch HCl 1,5 M => Các phản ứng xảy ra đồng thời:
CO3^2- + 2 H^+ => H2O + CO2.
HCO3- + H+ => H2O + CO2.
Do tỉ lệ trong hỗn hợp : n CO3^2-/ n HCO3- = 7/6 => 7x*2+6x = 0,15 => x=0,0075.
=> V = 2,184 lít.

Câu 1 :
\(Mg+2HCl\rightarrow MgCl_2+H_2\)
x______2x______x________x__(mol)
\(Al+2HCl\rightarrow AlCl_3+\frac{3}{2}H_2\)
y_____2y______y______3/2y__(mol)
\(n_{khí}=\frac{11,2}{22,4}=0,5\left(mol\right)\)
\(\left\{{}\begin{matrix}24x+27y=10,2\\x+\frac{3}{2}y=0,5\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}x=0,2\\y=0,2\end{matrix}\right.\)
\(\%m_{Mg}=\frac{10,2-\left(24.0,2\right)}{0,2}.100\%=52,94\%\)
\(\%m_{Al}=100\%-52,94\%=47,06\%\)
\(m_{muoi}=95.0,2+133,5.0,2=28,6\left(g\right)\)
\(V_{HCl}=1,6\left(l\right)\)
Dùng 7,5% \(\Rightarrow V=1,6-1,6.7,5\%=1,48\left(l\right)\)
Câu 2:
\(FeCl_2+2AgNO_3\rightarrow Fe\left(NO_3\right)_2+2AgCl\)
\(n_{FeCl2}=0,2.1=0,2\left(mol\right)\)
\(\Rightarrow n_{AgCl}=2n_{FeCl2}=2.0,2=0,4\left(mol\right)\)
\(m_{AgCl}=0,4.143,5=57,4\left(g\right)\)
\(n_{Fe\left(NO3\right)2}=n_{FeCl2}=0,2\left(mol\right)\)
V dd sau phản ứng= VFeCl2 + VAgNO3 = 0,2+0,3= 0,5 (l)
\(\Rightarrow CM_{FeCl2}=\frac{0,2}{0,5}=0,4M\)

1.
a)
- Cho quỳ tím vào các dung dịch
Quỳ tím chuyển thành màu đỏ : HCl , HNO3 (nhóm 1 )
Quỳ tím chuyển thành màu xanh : KOH , Ba(OH)2 ( nhóm 2 )
Quỳ tím không xảy ra hiện tượng : NaCl và NaNO3 (nhóm 3 )
*Cho AgNO3 vào ( nhóm 1 ) ta được :
Kết tủa trắng : HCl
\(AgNO3+HCl\rightarrow AgCl\downarrow+HNO3\)
Không xảy ra hiện tượng : HNO3
*Cho AgNO3 vào (nhóm 3) ta được :
Kết tủa trắng : NaCl
\(NaCl+AgNO_3\rightarrow NaNO_3+AgCl\downarrow\)
Không xảy ra hiện tượng :NaNO3
*Cho H2SO4 vào ( nhóm 2) ta được :
Kết tủa trắng : Ba(OH)2
\(Ba\left(OH\right)_2+H_2SO_4\rightarrow BaSO_4\downarrow+2H_2O\)
Không xảy ra hiện tượng : KOH
b)
- Cho quỳ tím vào các dung dịch
Quỳ tím chuyển thành màu đỏ : HCl , H2SO4 (nhóm 1)
Quỳ tìm chuyển thành màu xanh : NaOH
Không xảy ra hiện tượng :NaCl , NaBr ; NaI (nhóm 2)
*Cho AgNO3 vào (nhóm 1) ta được
Kết tủa trắng HCl
\(AgNO_3+HCl\rightarrow AgCl\downarrow+HNO_3\)
Không xảy ra hiện tượng H2SO4
Cho AgNO3 vào (nhóm 3) ta được
Kết tủa trắng là : NaCl
\(NaCl+AgNO_3\rightarrow AgCl\downarrow+NaNO_3\)
Chuyển thành màu vàng nhạt là :NaBr
\(AgNO3+NaBr\rightarrow AgBr\downarrow+NaNO_3\)
Chuyển thành màu vàng : NaI
\(AgNO_3+NaI\rightarrow AgI\downarrow+NaNO_3\)
2.
Cho hỗn hợp X vào HCl chỉ có Fe phản ứng:
\(Fe+2HCl\rightarrow FeCl_2+H_2\)
Ta có: \(n_{H2}=\frac{0,448}{22,4}=0,02\left(mol\right)=n_{Fe}\)
Cho X tác dụng với Cl2
\(2Fe+3Cl_2\rightarrow2FeCl_3\)
\(Cu+Cl_2\rightarrow CuCl_2\)
\(\rightarrow n_{FeCl3}=n_{Fe}=0,02\left(mol\right)\)
\(\rightarrow m_{FeCl3}=0,02.\left(56+35,5.3\right)=3,25\left(g\right)\)
\(m_{CuCl2}=7,3-3,25=4,05\left(g\right)\)
\(\rightarrow n_{CuCl2}=\frac{4,05}{64+35,5.2}=0,03\left(mol\right)=n_{Cu}\)
\(\rightarrow m=m_{Fe}+m_{Cu}=0,02.56+0,03.64=3,04\left(g\right)\)
3.
Gọi số mol Al là x; Fe là y
\(\rightarrow27x+56y=8,3\left(g\right)\)
\(Al+3HCl\rightarrow AlCl_3+\frac{3}{2}H_2\)
\(Fe+2HCl\rightarrow FeCl_2+H_2\)
\(\rightarrow n_{H2}=1,5n_{Al}+n_{Fe}=1,5x+y=\frac{5,6}{22,4}=0,25\left(mol\right)\)
Giải được \(x=y=0,1\)
\(\rightarrow m_{Al}=0,1.27=2,7\left(g\right)\)
\(\rightarrow\%m_{Al}=\frac{2,7}{8,3}=32,5\%\rightarrow\%m_{Fe}=100\%-32,5\%=67,5\%\)
Ta có muôí gồm AlCl3 và FeCl2
\(\rightarrow m_{muoi}=0,1.\left(27+35,5.3\right)+0,1.\left(56+35,5.2\right)=20,05\left(g\right)\)
b) Ta có: nHCl phản ứng=2nH2=0,5 mol
\(n_{HCl_{tham.gia}}=0,5.120\%=0,6\left(mol\right)\)
\(\rightarrow V_{HCl}=\frac{0,6}{1}=0,6\left(l\right)\)

Gọi số mol của NO2 và NO là a và b
Ta có hệ phương trình :
\(\left\{{}\begin{matrix}a+b=\frac{1,12}{22,4}\\\frac{46a+30b}{a+b}=16,75.2\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}a=0,01\\b=0,04\end{matrix}\right.\)
\(n_{HNO3}=n_{HNO3_{tao.muoi}}+n_{N\left(pu.khử\right)}=2n_{NO2}+4n_{NO}\)
\(=0,18\left(mol\right)\)
\(\Rightarrow CM_{HNO3}=0,65M\)
\(m_{muoi}=m_{pu}+m_{NO3}=\left(6,25-2,516\right)+\left(0,01.1+0,04.3\right).62\)
\(=11,794\left(g\right)\)

nhh khí = 2,464 / 22,4 = 0,11 mol; nPbS = 23,9 /239 = 0,1 mol.
a) Phương trình hóa học của phản ứng:
Fe + 2HCl → FeCl2 + H2
FeS + 2HCl → FeCl2 + H2S
H2S + Pb(NO3)2 → PbS + 2HNO3
nH2S = nPbS = 0,1 mol.
Gọi nFe = x; nFeS = y.
b) Hỗn hợp khí thu được là H2 và H2S
Theo phương trình phản ứng hóa học trên ta có:
Ta có x + y = 0,11.
Có nFeS = nH2S = 0,1.
x = 0,01 mol
VH2 = 0,01 x 22,4 = 0,224l.
VH2S = 0,1 x 22,4 = 2,24l.
c) mFe = 56 × 0,01 = 0,56g; mFeS = 0,1 × 88 = 8,8g.
nhh khí = 2,464 / 22,4 = 0,11 mol; nPbS = 23,9 /239 = 0,1 mol.
a) Phương trình hóa học của phản ứng:
Fe + 2HCl \(\rightarrow\) FeCl2 + H2
FeS + 2HCl \(\rightarrow\) FeCl2 + H2S
H2S + Pb(NO3)2 \(\rightarrow\) PbS + 2HNO3
nH2S = nPbS = 0,1 mol.
Gọi nFe = x; nFeS = y.
b) Hỗn hợp khí thu được là H2 và H2S
Theo phương trình phản ứng hóa học trên ta có:
Ta có x + y = 0,11.
Có nFeS = nH2S = 0,1.
x = 0,01 mol
VH2 = 0,01 x 22,4 = 0,224l.
VH2S = 0,1 x 22,4 = 2,24l.
c) mFe = 56 × 0,01 = 0,56g; mFeS = 0,1 × 88 = 8,8g.
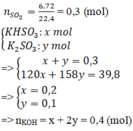

Đáp án C.
nSO2 = 0,3 mol
Gọi số mol KHSO3: x mol; K2SO3:y mol
x+y = 0,3 (1)
120x +158y = 39,8 (2)
=> x=0,2; y=0,1
=> nKOH = x + 2y = 0,4 (mol) (bảo toàn K)