
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


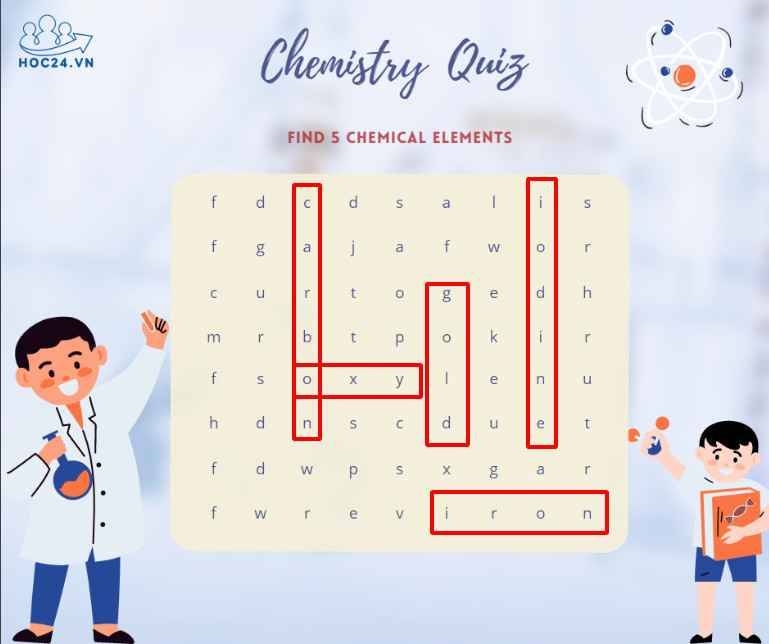
*cái oxy em k chắc á cô:<< em tìm được mấy nguyên tố này th ạ:<.

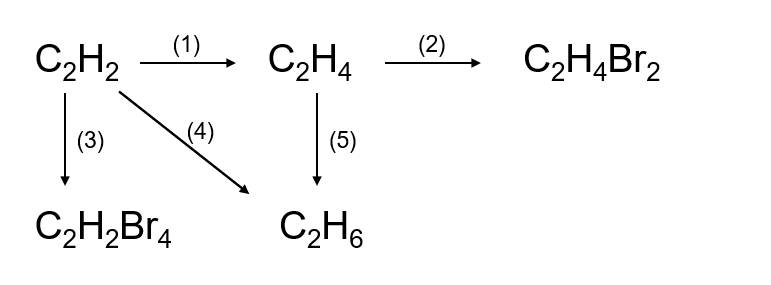
(1) \(2CH_4\xrightarrow[lln]{1500^oC}C_2H_2+3H_2\)
(2) \(C_2H_2+H_2\underrightarrow{t^o,Pd}C_2H_4\)
(3) \(C_2H_4+Br_2\rightarrow C_2H_4Br_2\)
(4) \(CH_4+Cl_2\underrightarrow{as}CH_3Cl+HCl\)
(5) \(C_2H_2+2Br_2\rightarrow C_2H_2Br_4\)
(6) \(C_2H_2+2H_2\underrightarrow{t^o,Ni}C_2H_6\)
(7) \(C_2H_4+H_2\underrightarrow{t^o,Ni}C_2H_6\)
(1) 2��4→���1500���2�2+3�22CH41500oCllnC2H2+3H2
(2) �2�2+�2��,��→�2�4C2H2+H2to,PdC2H4
(3) �2�4+��2→�2�4��2C2H4+Br2→C2H4Br2
(4) ��4+��2��→��3��+���CH

Câu 3:
N2+O2\(\overset{t^0}{\rightarrow}\)2NO
4NO+3O2+2H2O\(\rightarrow\)4HNO3
NO3- : làm tăng lượng phân đạm cho cây!

A là CuSO4
PTHH : CuSO4 + 2NaOH → Na2SO4 + Cu(OH)2↓
Cu(OH)2 ---to→ CuO + H2O
H2 + CuO ---to→ Cu + H2O
Cu +2 H2SO4 ---to→ CuSO4 + SO2 + 2H2O

ta co
M=5.4 , O2=32 va M2O=10,2
==>5,4+32=2M+16
giai ra M=10,7~11
ma 11 la Na
cau tra loi minh chua chac dung nhe
\(4M+nO_2\rightarrow2M_2O_n\)
\(m_{oxit}=m_O+m_M\Rightarrow m_O=m_{oxit}-m_M=10,2-5.4=4,8\)
\(n_O=\frac{4,8}{16}=0,3\Rightarrow n_{O_2}=0,15\)
\(\Rightarrow n_M=\frac{4}{n}.0,15\Rightarrow M_M=\frac{5,4}{\frac{4}{n}.0,15}=9n\)
lập bảng ta được n=3 thi M=27 nên M là nhôm


1. nna2o=\(\frac{15,5}{23.2+16}\)= 0,25( mol)
PTHH: Na2O + H2O \(\rightarrow\) 2NaOH
0,25(mol) 0,25( mol) 0,5(mol)
Dung dịch A là NaOH.
CM của dd NaOh=\(\frac{n}{V}\)=\(\frac{0,5}{0,5}\)=1 (M)
2. PTHH: 2NaOH + H2SO4 \(\rightarrow\) Na2SO4 + 2H2O
0,5(mol) 0,25(mol) 0,25(mol)
Khối lượng của H2SO4 là:
mH2SO4= n. M=0,25. 98=24,5(g)
Khối lượng dung dịch H2SO4 là
mdd H2SO4 = \(\frac{100.m_{H2SO\text{4}}}{C\%}\)=\(\frac{100.24,5}{20}\)=122.5 (g)
Thể tích dd H2SO4=\(\frac{m}{D}\)=\(\frac{122,5}{1,14}\)=107,45(ml)=0,107(l)
3. Nồng độ mol dung dịch sau phản ứng là
CM Na2SO4= \(\frac{n}{V}\)= \(\frac{0,25}{0,5}\)=0,5 M



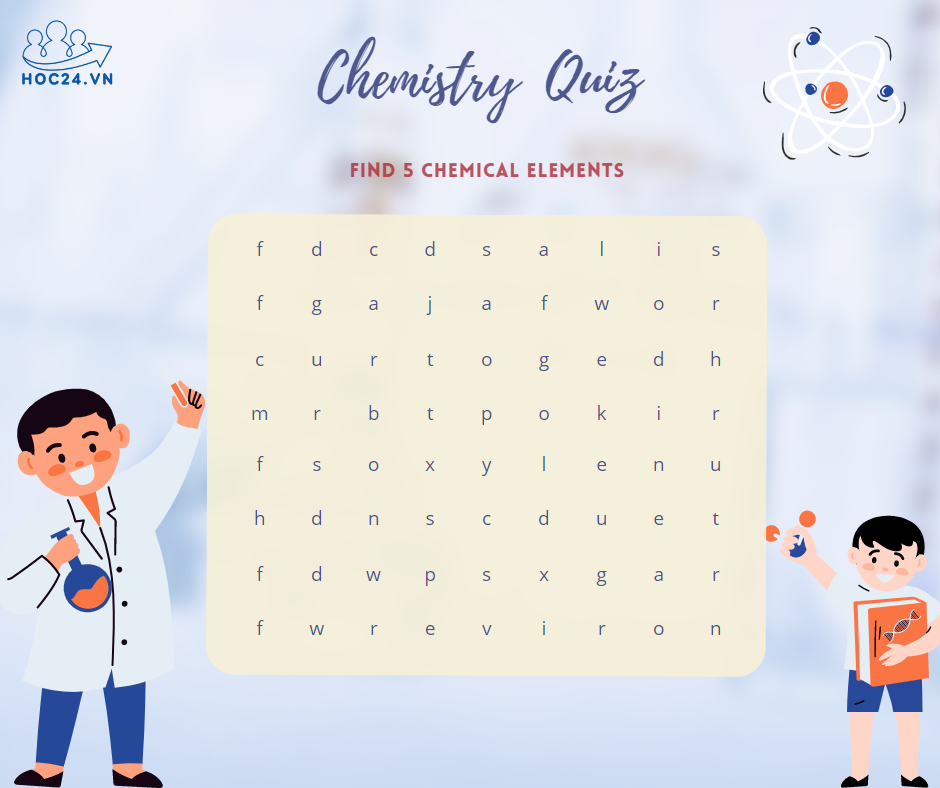
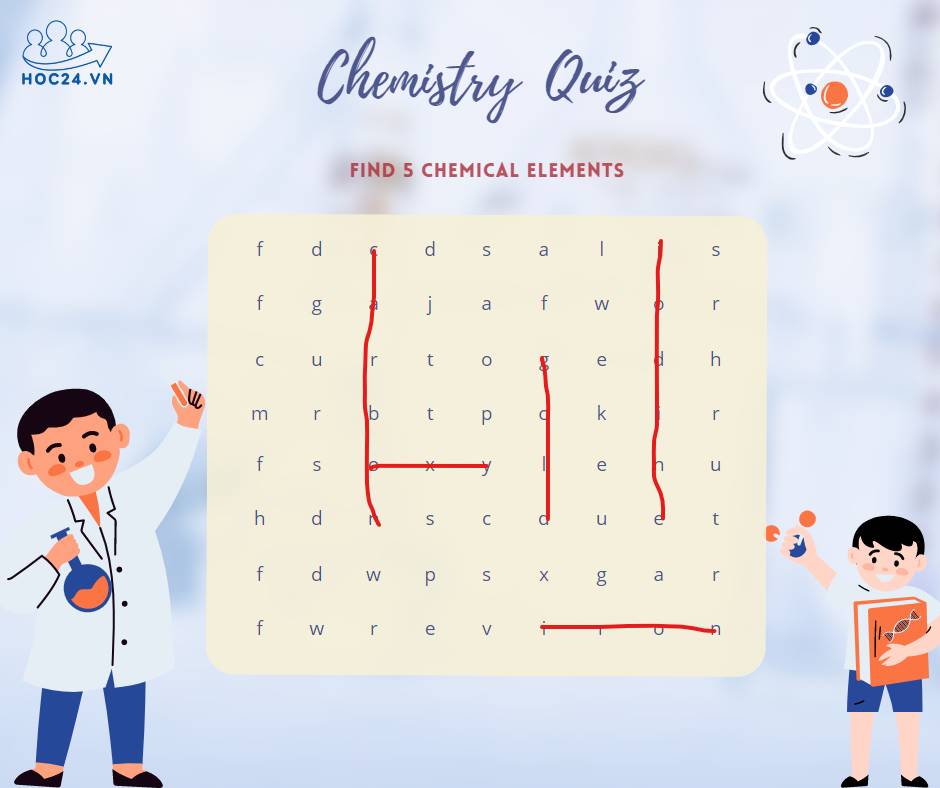

















 Giúp mình giải vài câu thực tế Hoá nha..
Giúp mình giải vài câu thực tế Hoá nha..
 Câu cuối cùng nha ae
Câu cuối cùng nha ae giúp em giải câu đó với
giúp em giải câu đó với





 chọn đáp án ạ
chọn đáp án ạ
Bài 7:
a, Ta có: \(n_{H_2O}=\dfrac{1,26}{18}=0,07\left(mol\right)\Rightarrow n_H=0,07.2=0,14\left(mol\right)\)
\(n_{CO_2}=\dfrac{3,08}{44}=0,07\left(mol\right)=n_C\)
\(n_{O_2}=\dfrac{1,568}{22,4}=0,07\left(mol\right)\)
Theo ĐLBT KL, có: mA + mO2 = mCO2 + mH2O
⇒ m = mA = 3,08 + 1,26 - 0,07.32 = 2,1 (g)
b, Ta có: mC + mH = 0,07.12 + 0,14.1 = 0,98 (g) < mA
→ A gồm C, H và O.
⇒ mO = 2,1 - 0,98 = 1,12 (g) \(\Rightarrow n_O=\dfrac{1,12}{16}=0,07\left(mol\right)\)
Gọi CTPT của A là CxHyOz.
⇒ x:y:z = 0,07: 0,14:0,07 = 1:2:1
→ A có CTPT dạng (CH2O)n.
Mà: \(M_A=\dfrac{12}{\dfrac{4,48}{22,4}}=60\left(g/mol\right)\)
\(\Rightarrow n=\dfrac{60}{12+1.2+16}=2\)
Vậy: CTPT của A là C2H4O2.