Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

2Fe + 3Cl2 → 2FeCl3
0,06 → 0,06 (mol)
=> mFeCl3 = 0,06. 162,5 = 9,75 (g)
Đáp án C

nHCl=2.0,1=0,2mol
PTHH: Fe+2HCl=>FeCl2+H2
0,1<-0,2--->0,1---->0,1
mFe phản ứng=0,1.56=5,6g
VH2 thu đc=0,1.22,4=2,24 lít

2.
nAl = 0,2 mol
2Al + 6HCl \(\rightarrow\) 2AlCl3 + 3H2
0,2......................0,2.......0,3
\(\Rightarrow\) VH2 = 0,3.22,4 = 6,72 (l)
\(\Rightarrow\) mAlCl3 = 0,2.133,5 = 26,7 (g)
nFe = 0,1 mol
Fe + 2HCl \(\rightarrow\) FeCl2 + H2
Đặt tỉ lệ ta có
0,1 < \(\dfrac{0,4}{2}\)
\(\Rightarrow\) HCl dư
\(\Rightarrow\) VH2 = 0,1.22,4 = 2,24 (l)
\(\Rightarrow\) nFeCl2 = 0,1 ( mol )

Số mol H2 là 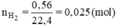
Fe + H2SO4 → FeSO4 + H2
Theo pt nFe = nH2 = 0,025(mol)
→ Khối lượng sắt dùng ở trường hợp 1 là: mFe = 0,025 x 56 = 1,4(g)
TH2: Lượng Fe gấp đôi khi đó số mol Fe là: 0,025. 2 = 0,05 (mol)
Fe + CuSO4 → FeSO4 + Cu
nFe = 0,05 mol.
Khối lượng Fe đã dùng ở trường hợp 2 là: mFe = 0,05 x 56 = 2,8 (g)
Khối lượng chất rắn m = mCu = 0,05 x 64 = 3,2(g)

\(TH1.Fe+H_2SO_4\rightarrow FeSO_4+H_2\\ n_{Fe}=n_{H_2}=\dfrac{0,56}{22,4}=0,025\left(mol\right)\\ \Rightarrow m_{Fe}=0,025.56=1,4\left(g\right)\\ TH2.Fe+CuSO_4\rightarrow FeSO_4+Cu\\ Lượnggấpđôi:n_{Fe}=0,025.2=0,05\left(mol\right)\\ \Rightarrow m_{Fe}=0,05.56=2,8\left(g\right)\\ n_{Cu}=n_{Fe}=0,05\left(mol\right)\\ \Rightarrow m_{Cu}=0,05.64=3,2\left(g\right)\)
