
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


a)
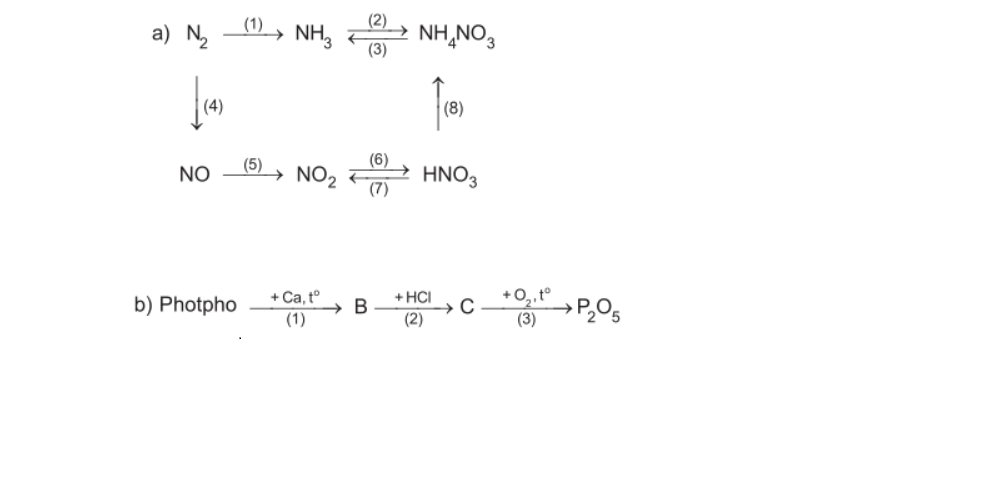
\(\left(1\right)N_2+3H_2⇌\left(xt,t^o,P\right)2NH_3\\ \left(2\right)NH_3+HNO_3\rightarrow NH_4NO_3\\ \left(3\right)NH_4NO_3+KOH\rightarrow KNO_3+NH_3+H_2O\\ \left(4\right)N_2+O_2⇌\left(3000^oC\right)2NO\\ \left(5\right)2NO+O_2\rightarrow2NO_2\\ \left(6\right)4NO_2+O_2+2H_2O\rightarrow4HNO_3\\ \left(7\right)Cu+4HNO_{3\left(đ\right)}\underrightarrow{t^o}Cu\left(NO_3\right)_2+2NO_2+2H_2O\\ \left(8\right)NH_3+HNO_3\rightarrow NH_4NO_3\)
b)
\(\left(1\right)2P+3Ca\underrightarrow{to}Ca_3P_2\\ \left(2\right)Ca_3P_2+6HCl\rightarrow3CaCl_2+2PH_3\\ \left(3\right)2PH_3+4O_2\underrightarrow{to}P_2O_5+3H_2O\)
Lưu ý đối với các phản ứng 2 chiều, mình không có thêm được điều kiện trên mũi tên phản ứng (do đặc thù của latex hoc24.vn) vì thế mình có mở ngoặc sau, bạn nào sau này thấy thì trong ngoặc là đk phản ứng nhé!



Câu 67:
Đổi 5,1 tấn = 5100 kg
Ta có: \(n_{NH_3}=\dfrac{5100}{17}=300\left(kmol\right)\)
Bảo toàn Nitơ: \(n_{NH_3}=n_{HNO_3\left(lý.thuyết\right)}=300\left(kmol\right)\)
\(\Rightarrow m_{ddHNO_3\left(thực\right)}=\dfrac{300\cdot40\%\cdot63}{63\%}=12000\left(kg\right)=12\left(tấn\right)\)
Câu 68:
Ta có: \(n_{HNO_3\left(thực\right)}=\dfrac{400\cdot12,6\%}{63}=0,8\left(mol\right)\) \(\Rightarrow n_{HNO_3\left(lý.thuyết\right)}=\dfrac{0,8}{40\%}=2\left(mol\right)\)
Bảo toàn Nitơ: \(n_{NH_3}=n_{HNO_3\left(lý.thuyết\right)}=2\left(mol\right)\) \(\Rightarrow V_{NH_3}=2\cdot22,4=44,8\left(l\right)\)







 giup mk vs
giup mk vs