Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án A
Ta có:
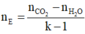
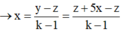
![]()
Trong E có 6 liên kết π (3 liên kết π của gốc R và 3 liên kết π của 3 nhóm COO)
![]()
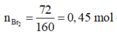
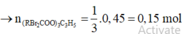
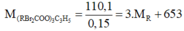
![]()
![]()
![]()
![]()

Đáp án A.
Đặt công thức của este E là (RCOO)3C3H5
Ta có y = z + 5x → y –z = 5x
→E có 6 liên kết pi (3 pi trong gốc COO, 3 pi trong gốc hiđrocacbon)
![]()
![]()
![]()
![]()

Từ b-d = 5a → A có 6 liên kết π
⟶ Gốc có 3 liên kết π ⟶A + 3Br2 = 110,1 g
⟶mA =110,1 -72 .
Dùng bảo toàn với KOH tính được x = 49,5
Đáp án B

N+5 +1e =>N+4
0,02 mol<=0,02 mol
2N+5 +2.4e =>2N+1
0,04 mol<=0,01 mol
ne nhận=ne nhường=0,06 mol
nNO3- tạo muối=ne nhận=0,06 mol
=>mNO3-=0,06.62=3,72g
mKL=5,04g=>m muối=m gốc KL+mNO3-=3,72+5,04=8,76g
nHNO3 =0,06+0,02+0,005.2=0,09 mol
=>CM dd HNO3=0,09/0,1=0,9M
Phương trình nhận electron:
N+5 + 8e → N2O
N+5 +1e→NO2
nNO tạo muối = nNO + 8nN2O = 0,02 + 8.0,005 = 0.02 + 0,04 = 0,06 mol
mNO tạo muối =0,06.62 = 3,72g
m =mKL+ mNO tạo muối = 5,04 + 3,72 = 8,76g
nHNO3 tham gia phản ứng = 2nNO + 10nN2O = 2.0,02 + 10.0,005= 0,09 mol
x =0.09:0,1=0,9M ==>> Đáp án thứ nhất




Chọn đáp án D
Vì nCO2 – nH2O = 5nEste ⇒ ∑ liên kết π trong este = 5+1 = 6.
⇒ Số liên kết π/C=C = 6 – 3 = 3 ⇒ Este + Br2 tối đa theo tỷ lệ 1:3
Mà nBr2 = 72 160 = 0,45 ⇒ nEste = 0 . 45 3 = 0,15 mol
Bảo toàn khối lượng ta có mEste = 110,1 – 72 = 38,1 gam.
⇒ Tăng giảm khối lượng ta có mMuối = mEste + mK – mC3H5
mMuối = 38,1 + 0,45×39 – 0,15×41 = 49,5 gam ⇒ Chọn D