Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đặt CT oxit kim loại là \(R_2O_n\)
\(R_2O_n+nCO\rightarrow\left(t^o\right)2R+nCO_2\) (1)
\(\overline{M_X}=19.2=38\) \((g/mol)\)
\(\Leftrightarrow\dfrac{28n_{CO\left(dư\right)}+44n_{CO_2}}{n_{CO\left(dư\right)}+n_{CO_2}}=38\)
\(\Leftrightarrow10n_{CO\left(dư\right)}-6n_{CO_2}=0\) (1)
\(n_{Ca\left(OH\right)_2}=2,5.0,025=0,0625\left(mol\right)\)
\(n_{CaCO_3}=\dfrac{5}{100}=0,05\left(mol\right)\)
`@` TH1: chỉ tạo ra kết tủa
\(Ca\left(OH\right)_2+CO_2\rightarrow CaCO_3\downarrow+H_2O\)
0,05 0,05 0,05 ( mol )
\(n_{CO_2}=0,05\) theo ptr (1)\(\Rightarrow n_{R_2O_n}=\dfrac{0,05}{n}\left(mol\right)\)
\(M_{R_2O_n}=\dfrac{4}{\dfrac{0,05}{n}}=80n\) \((g/mol)\)
\(\Leftrightarrow2R+16n=80n\)
\(\Leftrightarrow R=32n\)
`n=2->R` là Cu `->` CT oxit: \(CuO\)
`@`TH2: Ca(OH)2 hết
\(Ca\left(OH\right)_2+CO_2\rightarrow CaCO_3\downarrow+H_2O\)
0,0625 ( mol )
0,05 0,05 0,05 ( mol )
\(Ca\left(OH\right)_2+2CO_2\rightarrow Ca\left(HCO_3\right)_2\)
0,0125 0,025 ( mol )
\(n_{CO_2}=0,05+0,025=0,075\left(mol\right)\)
Theo ptr (1) \(n_{R_2O_n}=\dfrac{0,075}{n}\left(mol\right)\)
\(M_{R_2O_n}=\dfrac{4}{\dfrac{0,075}{n}}=\dfrac{160}{3}n\)
\(\Leftrightarrow2R+16n=\dfrac{160}{3}n\)
\(\Leftrightarrow R=\dfrac{56}{3}n\)
`n=3->R` Fe `->` CT oxit: \(Fe_2O_3\)

a) Công thức oxit là CuO
b) V CO banđầu= 1,792 (l)
Giải thích các bước giải:
Gọi công thức của oxit kim loại A là A2On
nCO+A2Onto→nCO2+2AnCO+A2On→tonCO2+2A
Ta có: nCa(OH)2=0,0625 (mol); nCaCO3=0,05 (mol)nCa(OH)2=0,0625 (mol); nCaCO3=0,05 (mol)
-) Xét TH Ca(OH)2 dư:
Chỉ tạo một muối CaCO3 ⇒ Số mol CO2 tính theo số mol CaCO3
PTHH: CO2+Ca(OH)2→CaCO3+H2OCO2+Ca(OH)2→CaCO3+H2O
Theo PTHH: nCO2=nCaCO3=0,05 molnCO2=nCaCO3=0,05 mol
Ta có: mCO2=2,2 (g); mCO=1,4 (g)mCO2=2,2 (g); mCO=1,4 (g)
BTKL: ⇒mA=4+1,4−2,2=3,2 (g)⇒mA=4+1,4−2,2=3,2 (g)
⇒MA=mn=3,20,1n=32n⇒MA=mn=3,20,1n=32n
Vì A là kim loại nên sẽ có hóa trị nằm từ 1 đến 3
Chỉ có cặp nghiệm duy nhất thỏa mãn: {n=2M=64{n=2M=64
Vậy A là Cu ⇒ Công thức oxit là CuO
Hỗn hợp khí X sau phản ứng gồm CO2 và CO dư
MX=19.2=38 (g/mol)MX=19.2=38 (g/mol)
Gọi a là số mol của CO dư
Ta có: MX=mn=mCO dư+mCO2nCO dư+nCO2MX=mn=mCO dư+mCO2nCO dư+nCO2
MX=a.28+0,05.44a+0,05=38MX=a.28+0,05.44a+0,05=38
⇒a=0,03 (mol)⇒a=0,03 (mol)
⇒nCO ban đầu=nCO pư+nCO dư=0,05+0,03=0,08 (mol)⇒nCO ban đầu=nCO pư+nCO dư=0,05+0,03=0,08 (mol)
VCO ban đầu=0,08.22,4=1,792 (l)VCO ban đầu=0,08.22,4=1,792 (l)
-) Xét TH Ca(OH)2 đủ: Tương tự với TH trên

Dung dịch Ca(OH)2 không hấp thụ khí CO nên 6,72 lít khí thoát ra chính là khí CO dư.


\(n_{Ca\left(OH\right)_2}=0,2.2,5=0,5\left(mol\right)\)
\(CuO+CO\underrightarrow{t^o}Cu+CO_2\uparrow\)
\(Fe_2O_3+CO\underrightarrow{t^o}2FeO+CO_2\uparrow\)
\(CO+PbO\underrightarrow{t^o}CO_2\uparrow+Pb\)
\(FeO+CO\underrightarrow{t^o}Fe+CO_2\uparrow\)
--> Hh kim loại Y là Cu , Pb , FeO , Fe
hh khí Z sau p/u là CO2
\(CO_2+Ca\left(OH\right)_2\rightarrow CaCO_3\downarrow+H_2O\)
trc p/u : 0,5 0,3
p/u : 0,3 0,3 0,3 0,3
sau : 0,3 0,2 0 0,3
\(n_{CaCO_3}=\dfrac{30}{100}=0,3\left(mol\right)\)
\(m_{CO_2}=0,3.44=13,2\left(g\right)\)
Áp dụng định luật bảo toàn khổi lượng :
\(m_Y=53,5-13,2=40,3\left(g\right)\)

Gọi oxit kim loại là M2Oy
Khí X gồm CO2 và CO
\(n_{Ca\left(OH\right)_2}=0,025\cdot2,5=0,0625\left(mol\right)\)
kết tủa là CaCO3 => \(n_{CaCO_3}=\dfrac{5}{100}=0,05\left(mol\right)\)
Ta xét 2 TH:
TH1 : chỉ tạo 1 muối trung hòa ( bazo dư )
PTHH : Ca(OH)2 + CO2 ----> CaCO3 + H2O
..............0,05...........0,05............0,05.......0,05(mol)
PTHH : M2Oy + yCO ----> 2M + yCO2
............0,05/y......0,05........0,1/y.....0,05...(mol)
=> ta có PT : \(\dfrac{4}{2M+16y}=\dfrac{0,05}{y}\)
y = 2 => M =64(Cu) ... ( Bạn tự lập bảng nha )
=> CT oxit : CuO
TH2 : tạo 2 muối ( CO2 dư, kết tủa tan 1 phần )
PTHH : Ca(OH)2 + CO2 ----> CaCO3 + H2O
.............0,0625........0,0625.......0,0625.....0,0625..(mol)
CaCO3 + CO2 + H2O ----> Ca(HCO3)2
0,0625-0,05.....................................(mol)
=> nCO2 = 0,0625 + 0,0625 -0,05 = 0,075 (mol)
PTHH : M2Oy + yCO ----> 2M + yCO2
..........0,075/y.....0,075.......0,15/y....0,075...(mol)
=> ta có PT : \(\dfrac{4}{2M+16y}=\dfrac{0,075}{y}\)
y = 3 => M = 56(Fe) -( Tự lập bảng nha )
=> CT oxit : Fe2O3
Xong câu a , câu b đợi
*Tỉnh V
Ta có sơ đồ dường chéo
=> \(\dfrac{n_{CO2}}{n_{CO}}=\dfrac{44-38}{38-28}=\dfrac{5}{3}\)
TH1 : theo PT khử : nCO phản ứng = nCO2
=> nCO = \(0,05+\left(0,05\cdot\dfrac{3}{5}\right)=0,08\left(mol\right)\)
=> \(V=0,08\cdot22,4=1,792\left(l\right)\)
TH2 : Tương tự TH1
=>\(n_{CO}=0,075+\left(0,075\cdot\dfrac{3}{5}\right)=0,12\left(mol\right)\)
\(\Rightarrow V=0,12\cdot22,4=2,688\left(l\right)\)
*Tỉnh V SO2
TH1 :
CuO + CO ----> Cu + CO2
.0,05....0,05........0,05....0,05..(mol)
Cu + 2H2SO4 ( đ,n ) ----> CuSO4 + 2H2O + SO2
.0,05...0,1.........................0,05........0,1........0,05...(mol)
\(\Rightarrow V_{SO_2}=0,05\cdot22,4=1,12\left(l\right)\)
TH2 :
Fe2O3 + 3CO ----> 2Fe + 3CO2
..0025....0,075.........0,05.....0,075..(mol)
2Fe + 6H2SO4 (đ,n) ----> Fe2(SO4)3 + 6H2O + 3SO2
0,05.....0,15......................0,025.........0,15........0,075..(mol)
\(\Rightarrow V_{SO_2}=0,075\cdot22,4=1,68\left(l\right)\)
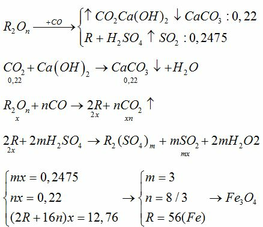
Sau phản ứng thu được hh khí => hh khí chứa CO, CO2 => RxOy bị khử hoàn toàn
PTHH:
\(R_xO_y+yCO\xrightarrow[]{t^o}xR+yCO_2\) (1)
\(Ca\left(OH\right)_2+CO_2\rightarrow CaCO_3\downarrow+H_2O\) (2)
\(Ca\left(OH\right)_2+2CO_2\rightarrow Ca\left(HCO_3\right)_2\) (3)
Ta có: \(\left\{{}\begin{matrix}M_X=19.2=38\left(g/mol\right)\\n_{Ca\left(OH\right)_2}=2,5.0,025=0,0625\left(mol\right)\\n_{CaCO_3}=\dfrac{5}{100}=0,05\left(mol\right)\end{matrix}\right.\)
Áp dụng sơ đồ đường chéo, ta có:
\(\dfrac{n_{CO}}{n_{CO_2}}=\dfrac{44-38}{38-28}=\dfrac{3}{5}\)
`-` TH1: Ca(OH)2 dư
Theo PT (2): \(n_{CO_2}=n_{CaCO_3}=0,05\left(mol\right)\)
Theo PT (1): \(n_{O\left(oxit\right)}=n_{CO_2}=0,05\left(mol\right)\)
`=>` \(\left\{{}\begin{matrix}m_R=4-0,05.16=3,2\left(g\right)\\n_R=\dfrac{x}{y}n_O=\dfrac{0,05x}{y}\left(mol\right)\end{matrix}\right.\)
`=>` \(M_R=\dfrac{3,2}{\dfrac{0,05x}{y}}=\dfrac{64y}{x}=32.\dfrac{2y}{x}\left(g/mol\right)\)
Với \(\dfrac{2y}{x}=2\Rightarrow M_R=32.2=64\left(g/mol\right)\)
`=> R` là `Cu`
`=>` \(n_{Cu}=0,05\left(mol\right)\)
PTHH: \(Cu+2H_2SO_{4\left(đ\right)}\xrightarrow[]{t^o}CuSO_4+SO_2+2H_2O\)
0,05--------------------------------->0,05
`=> V_{SO_2} = 0,05.22,4 = 1,12 (l)`
`-` TH2: CO2 dư
BTNT Ca: \(n_{Ca\left(HCO_3\right)_2}=n_{Ca\left(OH\right)_2}-n_{CaCO_3}=0,0125\left(mol\right)\)
BTNT C: \(n_{CO_2}=n_{CaCO_3}+2n_{Ca\left(HCO_3\right)_2}=0,075\left(mol\right)\)
`=>` \(\left\{{}\begin{matrix}m_R=4-0,075.16=2,8\left(g\right)\\n_R=\dfrac{0,075x}{y}\left(mol\right)\end{matrix}\right.\)
`=>` \(M_R=\dfrac{2,8}{\dfrac{0,075x}{y}}=\dfrac{112y}{3x}=\dfrac{56}{3}.\dfrac{2y}{x}\left(g/mol\right)\)
Với \(\dfrac{2y}{x}=3\Rightarrow M_R=56\left(g/mol\right)\)
`=> R` là `Fe`
`=>` \(n_{Fe}=\dfrac{0,075.2}{3}=0,05\left(mol\right)\)
PTHH: \(2Fe+6H_2SO_{4\left(đ\right)}\xrightarrow[]{t^o}Fe_2\left(SO_4\right)_3+3SO_2\uparrow+6H_2O\)
0,05------------------------------------->0,075
`=> V_{SO_2} = 0,075.22,4 = 1,68(l)`