Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

TN1. nKOH = 0,22 mol
2KOH + ZnSO4 → Zn(OH)2 + K2SO4 (1)
2KOH + Zn(OH)2 → K2ZnO2 + 2H2O (2)
Gọi x là số mol của Zn(OH)2 phản ứng ở pt (2)
ð Số mol của Zn(OH)2 tạo ra ở pt (1) là \(x+\frac{3a}{99}\); nKOH = 2x + \(2\left(x+\frac{3a}{99}\right)\)= 0,22 mol (1')
TN2. nKOH = 0,28 ; Lượng KOH ở thí nghiệm 2 lớn hơn TN1 là 0,28 – 0,22 = 0,06 mol.
Tương tự như trên ta có: nKOH = (2x + 0,06) + \(2\left(x+0,03+\frac{2a}{99}\right)\)= 0,28 mol (2')
Từ (1') và (2') => x = 0,01 ; a = 2,97 ==> nZnSO4 = = 0,1 mol => mZnSO4 = 161.0,1 = 16,1g

Goi nAl2O3=x mol ,nH2=0,6mol
2Al + 6HCl →2AlCl3 + 3H2
0,4mol<--- 0,4 <--- 0,6mol
Al2O3 + 6HCl → 2AlCl3 + 3H2O
0,1mol --->0,2
Ta co: 0,4.27 + x.102 = 21 ==> x=0,1 mol
ΣnAlCl3= 0,4 + 0,2 = 0,6 mol ---> nAl3+=0,6 mol
n↓=0,4 mol
pt ion rut gon giau NaOH tac dung voi dd A
Al3+ +3OH- → Al(OH)3↓
0,12<----- 0,4
==> VNaOH= 0,12:0,5 = 2,4lit==> A
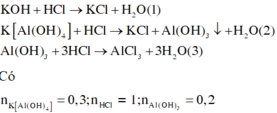



Nhận thấy nkết tủa = 0,2 mol < nK[Al(OH)4] =0,3 mol → Xảy ra 2 trường hợp
- TH1: không xảy ra sư hòa tan kết tủa :
KOH+ HCl → KCl + H2O
x----> x
K[Al(OH)4] + HCl → Al(OH)3 + KCl + H2O
0,3---------> 0,2---------> 0,2
Ta có x+ 0,2 = 1 → x= 0,8 mol → m= 44,8 gam
- TH2: xảy ra sự hòa tan kết tủa
KOH+ HCl → KCl + H2O
x----> x
K[Al(OH)4] + HCl → Al(OH)3 + KCl + H2O
0,2---------> 0,2---------> 0,2
K[Al(OH)4] + 4HCl → AlCl3+ KCl + H2O
0,1---------->0,4
Ta có x+ 0,2 + 0,4 = 1 → x= 0,4 → m = 22,4 gam.
Đáp án A