Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a, phương trình hóa học
3Fe2O3 + CO \(\rightarrow\) 2Fe3O4 + CO2 (1)
3mol..........1mol....2mol....... 1mol
Fe3O4 + CO \(\rightarrow\) 3FeO + CO2 (2)
1mol.........1mol......3mol ......1mol
FeO + CO \(\rightarrow\) Fe + CO2 (3)
1mol ......1mol ....... 1mol....1mol
Sè mol sắt thu được nFe = 0,3mol
Theo (1), (2) và (3) ta có số mol Fe2O3 là = nFe2O3 = 0,15mol
=> mFe2O3 = 0,15.160 = 24g

ta có nCO2=\(\frac{13.44}{22.4}\)=0,6 mol
bt1) Fe2O3+ CO\(\rightarrow\) CO2+Fe
ta có nFe= 0,6 mol
vậy mFe=0,6.56=33,6

PTHH: \(Fe_2O_3+3H_2\underrightarrow{t^o}2Fe+3H_2O\)
a+b) \(n_{Fe}=\dfrac{22,4}{56}=0,4\left(mol\right)\)
\(\Rightarrow\left\{{}\begin{matrix}n_{Fe_2O_3}=0,2\left(mol\right)\\n_{H_2}=0,6\left(mol\right)\end{matrix}\right.\) \(\Rightarrow\left\{{}\begin{matrix}m_{Fe_2O_3}=0,2\cdot160=32\left(g\right)\\V_{H_2}=0,6\cdot22,4=13,44\left(l\right)\end{matrix}\right.\)
c) PTHH: \(Zn+H_2SO_4\rightarrow ZnSO_4+H_2\uparrow\)
Theo PTHH: \(n_{Zn}=n_{H_2}=0,6\left(mol\right)\)
\(\Rightarrow m_{Zn}=0,6\cdot65=39\left(g\right)\)
a,
nFe = 22,4/56 = 0,4 (mol)
PTHH
Fe2O3 + 3H2 ---to----) 2Fe + 3H2O (1)
theo phương trình (1) ,ta có:
nFe2O3 = 0,4 x 2 / 1 = 0,8 (mol)
mFe2O3 = 160 x 0,8 = 128 (g)
b,
theo pt (1)
nH2 = (0,4 x 3)/2 = 0,6 (mol)
=) VH2 = 0,6 x 22,4 = 13,44 (L)
c,
PTHH
Zn + H2SO4 -------------) ZnSO4 + H2 (2)
Số mol H2 cần dùng là 0,6 (mol)
Theo PT (2) :
nZn = nH2 ==) nZn = 0,6 x 65 = 39 (g)

PTHH: \(Fe_2O_3+3CO\underrightarrow{t^o}2Fe+3CO_2\uparrow\)
Ta có: \(n_{Fe}=\dfrac{5,6}{56}=0,1\left(mol\right)\)
\(\Rightarrow\left\{{}\begin{matrix}n_{Fe_2O_3}=0,05\left(mol\right)\\n_{CO_2}=0,15\left(mol\right)\end{matrix}\right.\) \(\Rightarrow\left\{{}\begin{matrix}m_{Fe_2O_3}=0,05\cdot160=8\left(g\right)\\V_{CO_2}=0,15\cdot22,4=3,36\left(l\right)\end{matrix}\right.\)

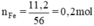
Phương trình hóa học của phản ứng:
Fe2O3 + 3H2 → 2Fe + 3H2O.
Khử 1 mol Fe2O3 cho 2 mol Fe.
x mol Fe2O3 → 0,2 mol.
x = 0,2 : 2 =0,1 mol.
m = 0,1 .160 =16g.
Khử 1 mol Fe2O3 cần 3 mol H2.
Vậy khử 0,1 mol Fe2O3 cần 0,3 mol H2.
V= 0,3 .22.4 = 6,72l.

\(n_{Fe}=\dfrac{8,4}{56}=0,15\left(mol\right)\\ pthh:3Fe+2O_2\underrightarrow{t^o}Fe_3O_{\text{4}}\)
0,15 0,1 0,05
\(m_{Fe_2O_4}=0,05.232=11,6\left(g\right)\\
V_{O_2}=0,1.11,4=2,24\left(l\right)\\
pthh:2KMnO_4\underrightarrow{t^o}K_2MnO_4+MnO_2+O_2\uparrow\)
0,2 0,1
\(m_{KMnO_4}=0,2.158=31,6\left(g\right)\)
\(n_{Fe}=\dfrac{8,4}{56}=0,15\left(mol\right)\\ pthh:3Fe+2O_2\underrightarrow{t^o}Fe_3O_4\)
0,15 0,1 0,05
\(m_{Fe_3O_{\text{ 4}}}=0,05.232=11,6\left(g\right)\\ V_{O_2}=0,1.22,4=2,24\left(l\right)\\ pthh:2KMnO_4\underrightarrow{t^o}K_2MnO_4+MnO_2+O_2\)
0,1 0,05
\(m_{KMnO_4}=0,1.158=15,8\left(g\right)\)

a, \(Fe_2O_3+3H_2\underrightarrow{t^o}2Fe+3H_2O\)
b, \(n_{Fe}=\dfrac{11,2}{56}=0,2\left(mol\right)\)
Theo PT: \(n_{Fe_2O_3}=\dfrac{1}{2}n_{Fe}=0,1\left(mol\right)\Rightarrow m_{Fe_2O_3}=0,1.160=16\left(g\right)\)
c, Theo PT: \(n_{H_2}=\dfrac{3}{2}n_{Fe}=0,3\left(mol\right)\)
\(\Rightarrow V_{H_2}=0,3.22,4=6,72\left(l\right)\)

\(3Fe_2O_3+CO-to>2Fe_3O_4+CO_2\left(1\right)\)
\(Fe_3O_4+CO-to>3FeO+CO_2\left(2\right)\)
\(FeO+CO-to>Fe+CO_2\left(3\right)\)
\(^nFe=\frac{16,8}{56}=0,3\left(mol\right)\)
theo pt (3) ta có \(^nFe=^nFeO=>^nFeO=0,3\left(mol\right)\)
theo pt (2) ta có \(3.^nFe_3O_4=^nFeO=>^nFe_3O_4=0,1\left(mol\right)\)
theo pt (1) ta có \(2.^nFe_2O_3=3.^nFe_3O_4=>^nFe_2O_3=0,15\left(mol\right)=>^mFe_2O_3=24\left(g\right)\)
\(CO_2+C< -to>2CO\)
\(=>^nCO_2\left(1\right)=0,05\left(mol\right)\)
\(=>^nCO_2\left(2\right)=0,1\left(mol\right)\)
\(=>^nCO_2\left(3\right)=0,3\left(mol\right)\)
\(=>^nCO_2\left(1,2,3\right)=0,45\left(mol\right)=>^VCO_2=10,08\left(l\right)\)
Fe2O3 + 3CO\(\rightarrow\)2Fe + 3CO2
Ta có: nFe=\(\frac{16,8}{56}\)=0,3 mol
Theo ptpu: nFe2O3=\(\frac{1}{2}\)nFe=0,15 mol
\(\rightarrow\) mFe2O3=0,15.160=24 gam
Ta có: nCO=nCO2=3nFe2O3=0,15.3=0,45 mol
CO2 + C \(\rightarrow\) 2CO
\(\rightarrow\)nCO2 cần=\(\frac{1}{2}\)nCO=0,225 mol \(\rightarrow\) nCO2 dư=0,45-0,225=0,225 mol
\(\rightarrow\)V CO2 dư=0,225.22,4=5,04 lít