Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Pt:
Fe3O4 + 4H2SO4 → FeSO4 + Fe2(SO4)3 + 4H2O
0,1 → 0,4 0,1 0,1
Cu + Fe2(SO4)3 → CuSO4 + 2FeSO4
0,1 ←0,1 → 0,1 0,2
Rắn B là 0,1 mol Cu → x = 6,4 (g)
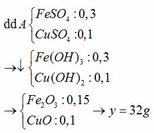

Tính toán theo PTHH :
Mg + CuSO4 → Cu + MgSO4
Mg + FeSO4 → Fe + MgSO4
Ba(OH)2 + MgSO4 → BaSO4 + Mg(OH)2
Ba(OH)2 + FeSO4 → BaSO4 + Fe(OH)2
Mg(OH)2 → MgO + H2O
2 Fe(OH)2 + ½ O2 → Fe2O3 + 2 H2O
Giả sư dung dịch muối phản ứng hết
=> n Fe = n FeSO4 = 0,2 . 1= 0,2 mol => m Fe = 0,2 . 56 = 11,2 g
=> n Cu =n CuSO4 = 0,2 . 0,5 = 0,1 mol => m Cu = 0,1 . 64 = 6,4 g
=> m chất rắn = 11,2 + 6,4 = 17,6 g > 12 g > 6,4
=> kim loại Fe dư sau phản ứng Vì CuSO4 phản ứng trước sau đó mới đến FeSO4 phản ứng
CuSO4 đã hết và phản ứng với 1 phần FeSO4
12 g = m Cu + m Fe phản ứng = 6,4 g + m Fe phản ứng
=> m Fe = 5,6 g => n Fe = 0,1 mol => n FeSO4 dư = 0,2 – 0,1 = 0,1 mol
Theo PTHH : n Mg = 0,1 + 0,1 = 0,2 mol ( bắng số mol CuSO4 và FeSO4 phản ứng )
Theo PTHH : n Mg = n MgSO4 = n Mg(OH)2 = n MgO = 0,2 mol
n FeSO4 dư = n Fe(OH)2 = n Fe2O3 . 2 = 0,1 mol
=> n Fe2O3 = 0,1 mol
=> m chất rắn = m Fe2O3 + m MgO = 0,1 . 160 + 0,2 . 40 = 24 g

\(n_{BaCO_3\left(5\right)}=\dfrac{19,7}{197}=0,1\left(mol\right)\)
\(n_{BaCO_3\left(7\right)}=\dfrac{14,775}{197}=0,075\left(mol\right)\)
\(C+\dfrac{1}{2}O_2\underrightarrow{t^o}CO\uparrow\) (1)
\(C+O_2\underrightarrow{t^o}CO_2\uparrow\) (2)
0,25 <------- 0,25
\(CO+Fe_3O_4\underrightarrow{t^o}3FeO+CO_2\uparrow\) (3)
\(FeO+CO\underrightarrow{t^o}Fe+CO_2\uparrow\) (4)
\(CO_2+Ba\left(OH\right)_2\underrightarrow{t^o}BaCO_3\downarrow+H_2O\) (5)
0,1 <------------------- 0,1
\(2CO_2+Ba\left(OH\right)_2\underrightarrow{t^o}Ba\left(HCO_3\right)_2\) (6)
0,15 <-------------------- 0,075
\(Ba\left(HCO_3\right)_2\underrightarrow{t^o}BaCO_3\downarrow+CO_2\uparrow+H_2O\) (7)
0,075 <--------- 0,075
\(Fe+CuSO_4\rightarrow FeSO_4+Cu\) (8)
0,03<-- 0,03
E: Cu, FeO, Fe3O4
(5)(6) \(\Rightarrow\Sigma_{n_{CO_2}}=0,1+0,15=0,25\left(mol\right)\)
\(m_C=0,25.12=3\left(g\right)\)
ý sau tự xử nha ![]() gọi ẩn, lắp hệ vào
gọi ẩn, lắp hệ vào ![]()

CO2 + Ca(OH)2 → CaCO3↓ + H2O
0,34 ←0,34
CO + O(Oxit) → CO2
Nhận thấy:
nO = nCO2
mX = mO (oxit) + mY
=> mY = 37,68 – 16 . 0,34 = 32,24g

Phương trình:
Fe3O4 + 4H2SO4 → FeSO4 + Fe2(SO4)3 + 4H2O
FeSO4 + 2NaOH → Na2SO4 + Fe(OH)2↓
Fe2(SO4)3 + 6NaOH → 3Na2SO4 + 2Fe(OH)3↓
2Fe(OH)2 + ½ O2 → Fe2O3 + 2H2O
2Fe(OH)3 → Fe2O3 + 3H2O
Fe2O3 + 3CO → 2Fe + 3CO2↑
CO2 + Ca(OH)2 → CaCO3↓ + H2O
3CO2 + Ca(OH)2 → Ca(HCO3)2
Ca(HCO3)2 → CaCO3 + CO2↑ + H2O





a)
\(C+O_2\xrightarrow[]{t^o}CO_2\) (1)
\(2C+O_2\xrightarrow[]{t^o}2CO\) (2)
\(Fe_3O_4+CO\xrightarrow[]{t^o}3FeO+CO_2\) (3)
\(Fe_3O_4+4CO\xrightarrow[]{t^o}3Fe+4CO_2\) (4)
\(Ba\left(OH\right)_2+CO_2\rightarrow BaCO_3\downarrow+H_2O\) (5)
\(Ba\left(OH\right)_2+2CO_2\rightarrow Ba\left(HCO_3\right)_2\) (6)
\(Ba\left(HCO_3\right)_2\xrightarrow[]{t^o}BaCO_3\downarrow+CO_2\uparrow+H_2O\) (7)
\(Fe+CuSO_4\rightarrow FeSO_4+Cu\) (8)
b)
Ta có: \(\left\{{}\begin{matrix}n_{BaCO_3\left(5\right)}=\dfrac{19,7}{197}=0,1\left(mol\right)\\n_{BaCO_3\left(7\right)}=\dfrac{14,775}{197}=0,075\left(mol\right)\end{matrix}\right.\)
Theo (5): \(n_{Ba\left(HCO_3\right)_2}=n_{BaCO_3\left(7\right)}=0,075\left(mol\right)\)
Theo (3), (4): \(n_{CO_2}=2n_{Ba\left(HCO_3\right)_2}+n_{BaCO_3\left(5\right)}=0,3\left(mol\right)\)
BTNT C: \(n_C=n_{CO_2}=0,3\left(mol\right)\)
=> m = 0,3.12 = 3,6 (g)
\(n_{Fe_3O_4}=\dfrac{23,2}{232}=0,1\left(mol\right)\)
Theo (8): \(n_{Fe}=n_{Cu}=n_{CuSO_4\left(pư\right)}=0,03\left(mol\right)\)
Gọi \(\left\{{}\begin{matrix}n_{FeO}=x\left(mol\right)\\n_{Fe_3O_4}=y\left(mol\right)\end{matrix}\right.\)
=> 72x + 232y = 21,84 - 0,03.64 = 19,92 (*)
BTNT Fe: \(3n_{Fe_3O_4\left(bđ\right)}=3n_{Fe_3O_4\left(dư\right)}+n_{FeO}+n_{Fe}\)
=> x + 3y = 3.0,1 - 0,03 = 0,27 (**)
Từ (*), (**) => \(\left\{{}\begin{matrix}x=0,18\\y=0,03\end{matrix}\right.\)
=> mB = 0,18.72 + 0,03.232 + 56.0,03 = 21,6 (g)
Theo BTNT: \(m_{O\left(pư\right)}=m_{giảm}=23,2-21,6=1,6\left(g\right)\)
=> \(n_{O\left(pư\right)}=\dfrac{1,6}{16}=0,1\left(mol\right)\)
Theo (3), (4): \(n_{CO_2\left(sinh.ra\right)}=n_{CO}=n_{O\left(oxit\right)}=0,1\left(mol\right)\)
=> \(n_{CO_2\left(1\right)}=0,3-0,1=0,2\left(mol\right)\)
=> \(\overline{M}_A=\dfrac{0,2.44+0,1.28}{0,2+0,1}=\dfrac{116}{3}\left(g/mol\right)\)
=> \(d_{A/H_2}=\dfrac{\dfrac{116}{3}}{2}=\dfrac{58}{3}\)
hóa học 9 có vẻ khó nhỉ mik trả hiểu j nên ko trả lời đc sorry