Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Chọn đáp án D
Quy đổi T về C (x mol), H (y mol), O (z mol). Bảo toàn C, H ta có sơ đồ phản ứng cháy sau:
T (C, H, O) + O2 → CO2 (x mol) + H2O (0,5y mol).
0,5y = 1,04 ⇒ y = 2,08.
Bảo toàn O ta có z + 1,6.2 = 2x + 0,5y ⇔ 2x – z = 2,16 (1).
Chất béo no có công thức chung là CnH2n–4O6.
ncbéo no = 1 6 nO = 1 6 z.
Nhận thấy: nC – 1 2 nH = 2ncbéo no ⇔ nH = 2x – 2 z 3 .
mcbéo no = 12x + 2x – 2 z 3 + 16z = 17,8 (2).
Từ (1) và (2) suy ra x = 1,14; z = 0,12.
Vậy x : y : z = 1,14 : 2,08 : 0,12 = 57 : 104 : 6 → T là C57H104O6.
MT = 884.

Chọn đáp án A
đốt a mol X + O2 → b mol CO2 + c mol H2O.
Tương quan: nCO2 – nH2O = 4nX (b – c = 4a theo giả thiết).
mà nCO2 – nH2O = (∑πtrong X – 1)nX ||→ ∑πtrong X = 4 + 1 = 5.
► chú ý πC=O trong X = 3 → πC=C = ∑π – πC=O = 5 – 3 = 2.
||→ Phản ứng: 1X + 2H2 → 25,02 gam chất béo no. có nH2 = 0,06 mol → nX = 0,03 mol
và mX = 25,02 – 0,06 × 2 = 24,9 gam → MX = Ans ÷ 0,03 = 830

Chọn đáp án D
a gam E + 0,06 mol H2 → chất béo no T.
⇒ quy đổi đốt T cần thêm 0,03 mol O2 và sinh thêm 0,06 mol H2O so với đốt E.
||⇒ đốt T dạng CnH2n – 4O6 + 1,57 mol O2 → t o 2x mol CO2 + 1,06 mol H2O.
Tương quan đốt T có: ∑nCO2 – ∑nH2O = 2nT ⇒ nT = x – 0,53 mol.
♦ bảo toàn nguyên tố O có: 6 × (x – 0,53) + 1,57 × 2 = 4x + 1,06 ⇒ x = 0,55 mol.
Biết x ⇒ giải ra các thông số về T: mT = 17,24 gam và nT = 0,02 mol.
♦ thủy phân: 0,02 mol T cần 0,06 mol NaOH → muối + 0,02 mol glixerol.
⇒ BTKL có mmuối = 17,24 + 0,06 × 40 – 0,02 × 92 = 17,80 gam.

Chọn đáp án D
Gọi nT = x mol và triglixerit T có a liên kết π (gồm 3πC=O và (a – 3)πC=C).
♦ tương quan đốt: ∑nCO2 – ∑nH2O = (∑π – 1)nT ⇒ (a – 1)x = 0,12 mol.
♦ phản ứng với H2: 1πC=C + 1H2 ⇒ (a – 3)x = nH2 = 0,06 mol.
||⇒ giải x = 0,03 mol và a = 5 ||⇒ Mchất béo no = 25,86 ÷ 0,03 = 862.
890 là phân tử khối của tristearat ⇒ 862 gồm 1 gốc panmitat và 2 gốc stearat.
Vậy, chất béo không no T gồm 1 gốc panmitat và 2 gốc oleat.

Chọn đáp án B
đốt a gam E + 3,08 mol O2 → t o 2,2 mol CO2 + 2,0 mol H2O.
• BTKL có a = mCO2 + mH2O – mO2 = 34,24 gam.
• bảo toàn nguyên tố có nO trong E = 2nCO2 + nH2O – 2nO2 = 0,24 mol ⇒ nE = 0,04 mol.
• tương quan đốt có (∑π – 1)nE = ∑nCO2 – ∑nH2O = 0,2 mol.
⇒ ∑πtrong E = 6 = 3πC=O + 3πC=C ||⇒ E + 3H2 → m gam chất béo no
⇒ m = mE + mH2 = 34,24 + 0,04 × 3 × 2 = 34,48 gam.

Chọn đáp án A
đốt m gam E + a mol O2 → 1,1 mol CO2 + 1,02 mol H2O.
Tương quan: nCO2 – nH2O = (∑πtrong E – 1) × nE = 1,1 – 1,02 = 0,08 mol (1).
vì E là trglixerit nên sẵn có 3πC=O rồi nên πC=C trong E = ∑πtrong E – 3.
||→ phản ứng hiđro hóa E + H2 thực chất là 1πC=C + 1H2
||→ nπC=C trong E = nH2 = 0,04 mol → (∑πtrong E – 3) × nE = 0,04 mol (2).
Từ (1) và (2) → có ∑πtrong E – 1 = 2 × (∑πtrong E – 3) → ∑πtrong E = 5.
Thay lại (1) hoặc (2) tính ra nE = 0,02 mol; E có 6O → nO trong E = 0,02 × 6 = 0,12 mol.
► ở phản ứng đốt, bảo toàn O có nO2 cần = (2nCO2 + nH2O – nO trong E) ÷ 2
Thay số vào có ngay a = nO2 cần = 1,55 mol

Chọn đáp án B
a mol T + 4a mol H2 → Ni , t o chất béo no (phản ứng vừa đủ).
||→ trong T có chứa 4 nối đôi C=C hay πC=C trong T = 4; lại thêm πC=O trong T = 3
||→ ∑πtrong T = 7. Đốt cháy 0,02 mol T + O2 → t o CO2 + 1,02 mol H2O.
||→ tương quan: nCO2 – nH2O = (∑πtrong T – 1).nT. Thay số có nCO2 = 1,14 mol.
T có 6O nên bảo toàn O có nO2 cần đốt = 1,14 + 1,02 ÷ 2 – 0,02 × 3 = 1,59 mol.
||→ V = VO2 cần đốt = Ans × 22,4 = 35,616 lít
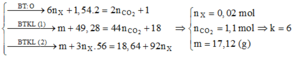
Chọn đáp án C
đốt x mol triglixerit T + 1,5 mol O2 → t 0 CO2 + 1,0 mol H2O.
Bảo toàn nguyên tố O có nCO2 = 3x + 1 mol.
Tương quan: nCO2 – nH2O = 3x = 3nT → ∑πtrong T = 3 + 1 = 4.
Mà sẵn trong T có 3πC=O → πC=C = 1 → 1T + 1H2 → 16,68 gam chất béo no.
||→ mT = 16,68 – 2x = 18 + 44 × (3x + 1) – 1,5 × 32 ||→ x = 0,02 mol.
Thay x ngược lại có mT = 16,64 gam → MT = Ans ÷ 0,02 = 832