Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Chọn B.
Ta có:
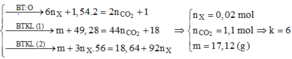
(có 3π gốc H.C)
Khi cho X tác dụng với H2 thì a = 0,02 mol

Chọn đáp án B
► Đặt nX = x ⇒ Bảo toàn nguyên tố Oxi: nCO2 = (3x + 1,04) mol.
⇒ mX = mC + mH + mO = 12.(3x + 1,04) + 1 × 2 + 16.6x = (132x + 14,48) (g).
Bảo toàn khối lượng: (132x + 14,48) + 56 × 3x = 18,64 + 92x ||⇒ x = 0,02 mol.
● Tìm được: nCO2 = 1,1 mol || Lại có: đối với HCHC chứa C, H và có thể có O thì
nCO2 – nH2O = (k – 1).nHCHC (k: độ bất bão hòa của HCHC)
||⇒ áp dụng: 1,1 – 1 = (k – 1).0,02 ⇒ k = 6 = 3πC=C + 3πC=O.
⇒ X tác dụng với Br2 theo tỉ lệ 1 : 3 ⇒ a = 0,06 ÷ 3 = 0,02 mol

N+5 +1e =>N+4
0,02 mol<=0,02 mol
2N+5 +2.4e =>2N+1
0,04 mol<=0,01 mol
ne nhận=ne nhường=0,06 mol
nNO3- tạo muối=ne nhận=0,06 mol
=>mNO3-=0,06.62=3,72g
mKL=5,04g=>m muối=m gốc KL+mNO3-=3,72+5,04=8,76g
nHNO3 =0,06+0,02+0,005.2=0,09 mol
=>CM dd HNO3=0,09/0,1=0,9M
Phương trình nhận electron:
N+5 + 8e → N2O
N+5 +1e→NO2
nNO tạo muối = nNO + 8nN2O = 0,02 + 8.0,005 = 0.02 + 0,04 = 0,06 mol
mNO tạo muối =0,06.62 = 3,72g
m =mKL+ mNO tạo muối = 5,04 + 3,72 = 8,76g
nHNO3 tham gia phản ứng = 2nNO + 10nN2O = 2.0,02 + 10.0,005= 0,09 mol
x =0.09:0,1=0,9M ==>> Đáp án thứ nhất

Chọn đáp án C
X C 3 H 5 O O C R 3 + O 2 → t 0 C O 2 + H 2 O
![]()
C 3 H 5 O O C R 3 + 3 K O H → t 0 3 R C O O K + C 3 H 5 O H 3
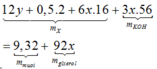
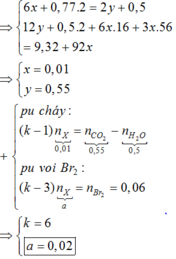
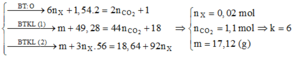


- Công thức của X có dạng: (RCOO)3C3H5
- Gọi số mol X trong m gam là x => nO(X) = 6x mol
- Phản ứng cháy:
BTNT "O": nO(X) + 2nO2 = 2nCO2 + nH2O => nCO2 = ½ (6x + 2.1,54 – 1) = 3x + 1,04
=> mX = mC + mH + mO = 12(3x + 1,04) + 1.2 + 16.6x = 132x + 14,48
- Thủy phân X với NaOH:
(RCOO)3C3H5 + 3KOH → 3RCOOK + C3H5(OH)3
Mol x → 3x → 3x → x
Bảo toàn khối lượng: mX + mNaOH = mmuối + mancol
=> (132x + 14,48) + 3x.56 = 18,64 + 92x
=> x = 0,02 mol => nCO2 (cháy) = 3x + 1,04 = 1,1 mol
Số nguyên tử C = nC : nX = nCO2 : nX = 1,1 : 0,02 = 55
Số nguyên tử H = nH : nX = 2nH2O : nX = 2 : 0,02 = 100
Vậy CTPT của X là C55H100O6 => Độ bất bão hòa: k = (2C + 2 - H)/2 = (2.55 + 2 - 100)/2 = 6
Vì X có sẵn 3 liên kết π trong 3 nhóm COO => 3 liên kết π còn lại nằm trong gốc hidrocacbon
=> Khi X + H2 dư thì: nH2 = 3nX => a = nX = 0,06 : 3 = 0,02 mol
Đáp án cần chọn là: B