Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án C
Đốt cháy hết hỗn hợp H thu được 0,83 mol CO2 và 0,815 mol H2O.
Tổng số nguyên tử O trong ba peptit là 12 do vậy tổng số gốc aa trong 3 peptit là 9 vậy Z là 5-peptit
Quy đổi H vè C2H3ON a mol, CH2 b mol và H2O c mol
=> 2a+b= 0,83=> 1,5a+b+c= 0,815
Muối khan T gồm C2H4O2NNa a mol và CH2 b mol
Đốt T sẽ thu được 1,5a+b mol CO2 và 2a +b mol H2O
=> 44(1,5a+b)+18(2a+b)= 44,2
Giải được: a=0,33; b=0,17; c=0,15
Gọi số mol của X, Y lần lượt là m, số mol của Z là n
=> m+n= 0,15=> 2m+5n=0,33
Giải được: m=0,14; n=0,01
Do X, Y là dipeptit cùng số nguyên tử C nên X, Y gồm hai aa thay đổi vị trí của nhau.
Do vậy số mol của hai amino axit đều từ 0,14 trở lên
Vậy một amino axit là Gly 0,16 mol và 0,17 mol Ala (từ 0,17 mol CH2)
Do vậy X và Y đều có dạng GlyAla và Z là Ala3Gly2
Vậy tổng số nguyên tử của 3peptit là 87

Chọn đáp án A.
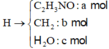
→ + O 2 , t o C O 2 : 0 , 83 m o l H 2 O : 0 , 815 m o l
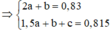 (1)
(1)
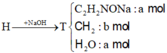
→ + O 2 , t o N a 2 C O 3 : 0 , 5 a m o l C O 2 : 1 , 5 a + b m o l H 2 O : a + b + a m o l
![]() (2)
(2)
Từ (1) và (2) suy ra:
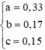
Tổng số nguyên tử O trong 3 peptit là 12, X và Y là đipeptit
=> Z là pentapeptit.
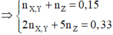
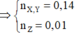
X và Y là đipeptit, có cùng số nguyên tử C
=> X và Y là đồng phân của nhau.
Có m T = 79 a + 14 b + 18 a = 34 , 39 g
![]()
⇒ Có 1 aminoaxit là Gly
Có n A ≥ 0 , 14 m o l mà giá trị 0 , 17 n A phải là một số nguyên
⇒ n A = 0 , 17 và A là Ala
=> n G l y = 0 , 33 - 0 , 17 = 0 , 16
=> Z có cấu tạo là Gly2Ala3 (CTPT: C13H23N5O6) X và Y có cấu tạo AlaGly (CTPT: C5H10N2O3)
=> Tổng số nguyên tử tỏng 3 phân tử = 87

MgCO3 + 2HCl → MgCl2 + CO2 + H2O (1)
BaCO3 + 2HCl → BaCl2 + CO2 + H2O (2)
CO2 + Ca(OH)2 → CaCO3↓ + H2O. (3)
Theo (1), (2) và (3), để lượng kết tủa B thu được là lớn nhất thì:
nCO2 = nMgCO3 + nBaCO3 = 0,2 mol
Ta có:  = 0,2
= 0,2
=> a = 29,89.

Bài giải:
- Vì =
=>
=
, suy ra polime đó là polietilen (-CH2 – CH2 - )n.
- Không thể là tinh bột (-C6H10O5-)n, vì có tỉ lệ =
, cũng không thể là PVC vì chất này khi cháy phải có sinh ra hợp chất chứa clo.

VO2(pư)=1/5Vkk=8.4(l).theo bài ra ta có nCO2+N2=44.8/22.4=2(1)lại có dB/H2=15=>nCO2/nN2=1/7(2).từ (1)và(2)=>nCO2=0.25(mol)và nN2=1.75(mol).
áp dụng ĐLBTKL ta có m=mCO2+mH2O+mN2-mO2(pư)=57(gam).ta lại có mC+mH+mN=nCO2.12+2.nH2O+28.nN2=53(gam) <57(gam)=>trong A có nguyên tố oxi mO=57-53=4(gam).gọi CTĐGN của A là CxHyOzNt ta có:x:y:z:t=nCO2:2nH2O:nO:2nN2=1:4:1:14=>CTĐGN của A:CH4ON14.lại có 12n+4n+16n+196n=600(tớ nghĩ phải là 600 chứ A chứa nhiều nguyên tố lắm)=>n=3=>CTHH của A:C3H12O3N42.

TH1: Cả 2 muối \(NaX\) và \(NaY\) đều pứ vs \(\text{AgNO3}\)
\(NaZ\) + \(AgNO_3\) \(\rightarrow\) \(NaNO_3\) + \(AgZ\)
TH2: 2 muối của X và Y lần lượt là \(NaF\) và \(NaCl\)
Mol \(AgCl\) =8,61/143,5 = 0,06mol
0,06<= 0,06
m\(NaCl\) = 0,06.58,5=3,51g
%m\(NaF\) = 2,52/6,03 .100% = 41,79%
Do AgF tan, khác các muối còn lại nên chia thành 2 trường hợp:
TH1: Hai muối ban đầu là NaF và NaCl —> nNaCl = nAgCl = 0,06 —> %NaF = 41,79%
TH2: Cả 2 muối đều tạo kết tủa:
m tăng = n muối (108 – 23) = 8,61 – 6,03 —> n muối = 0,03 —> M = 198,6 —> Halogen = M – 23 = 175,6: Vô nghiệm


