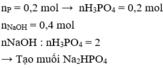Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Theo pt: nNa2HPO4 = 2.nP2O5 = 0,1. 2 = 0,2 mol
Theo định luật bảo toàn khối lượng:
Khối lượng dung dịch sau phản ứng = khối lượng các chất tham gia phản ứng = mNaOH + mP2O5 = 50 + 0,1.142 = 64,2
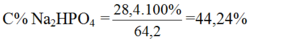

Đáp án C
4P + 5O2 → 2P2O5
P2O5 + 6NaOH dư → 2Na3PO4 + 3H2O
=> nNa3PO4 = 82/164 = 0,5 (mol)
BTNT P => nP = nNa3PO4 = 0,5 (mol) => mP = 0,5.31 = 15,5 (gam)

Đáp án: A.
Hướng dẫn:
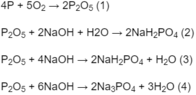
Số mol photpho: 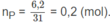
Số mol NaOH: ![]()
Sản phẩm tạo thành khi đốt photpho là P 2 O 5 .
Theo (1), số mol P 2 O 5 :
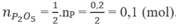
Ti lệ số mol NaOH và P 2 O 5 :
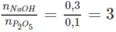
Tỉ lệ số mol nằm trong khoảng 2 và 4, do đó theo các phản ứng (2) và (3) trong dung dịch thu được có hai muối được tạo thành là N a H 2 P O 4 và N a 2 H P O 4 .

a, \(n_P=\dfrac{7,75}{31}=0,25\left(mol\right)\)
PTHH: 4P + 5O2 ---to→ 2P2O5
Mol: 0,25 0,125
PTHH: P2O5 + 3H2O → 2H3PO4
Mol: 0,125 0,25
\(C\%_{ddH_3PO_4}=\dfrac{0,25.98.100\%}{280}=8,75\%\)
b, \(n_{NaOH}=0,3.2=0,6\left(mol\right)\)
Ta có: \(T=\dfrac{0,6}{0,25}=2,4\) ⇒ tạo ra 2 muối Na2HPO4, Na3PO4
PTHH: 2NaOH + H3PO4 → Na2HPO4 + 2H2O
Mol: 2x x x
PTHH: 3NaOH + H3PO4 → Na3PO4 + 3H2O
Mol: 3y y y
Ta có: \(\left\{{}\begin{matrix}x+y=0,25\\2x+3y=0,6\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}x=0,15\\y=0,1\end{matrix}\right.\)
\(m_{muối}=0,15.141+0,1.164=37,55\left(g\right)\)

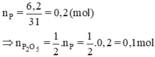
Theo pt: nNaOH = 4. nP2O5 = 4. 0,1 = 0,4 mol
Khối lượng NaOH = 0,4. 40 = 16 g
Khối lượng dung dịch NaOH = 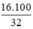 = 50,0 g
= 50,0 g

Phương trình phản ứng:
4P + 5O2 → 2P2O5 (1)
P2O5 + 4NaOH → 2Na2HPO4 + H2O (2)