Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a)
\(FeSO_4 + 2NaOH \to Fe(OH)_2 + Na_2SO_4\)
b)
\(n_{FeSO_4} = 0,4.0,5 = 0,2(mol) ; n_{NaOH} = 0,5.0,5 = 0,25(mol)\)
Ta thấy : \(2n_{FeSO_4} = 0,4 > n_{NaOH} = 0,25\) nên FeSO4 dư.
Theo PTHH :
\(n_{Fe(OH)_2} = 0,5n_{NaOH} = 0,125(mol)\\ \Rightarrow m_{Fe(OH)_2} = 0,125.90 = 11,25(gam)\)
c)
\(4Fe(OH)_2 + O_2 \xrightarrow{t^o} 2Fe_2O_3 + 4H_2O\)
Theo PTHH :
\(n_{Fe_2O_3} = 0,5n_{Fe(OH)_2} = 0,0625(mol)\\ \Rightarrow m_{Fe_2O_3} = 0,0625.160 = 10(gam)\)

Bài 1
nBaCl2= 200 *2.6%= 5.2 (g) ; nBaCl2= 5.2/208=0.025(mol)
nH2SO4=49*10%=4.9(g) ; nH2SO4=4.9/98=0.05(mol)
PTHH
..........................H2SO4 + BaCl2 ➞ 2HCl + BaSO4
Trước phản ứng:0.05 : 0.025...................................(mol)
Trong phản ứng:0.025 : 0.025......... : 0.025 : 0.05(mol)
Sau phản ứng : 0.025 : 0 ......... : 0.025 : 0.05 (mol)
a) mBaSO4=0.025*233=5.825(g)
b) mdd sau phản ứng = 49+200-5.825=243.175(g)
C% (H2SO4) = (0.025* 98)/243.175*100%=1.007%
C% (HCl) = (0.05*36.5)/243.175*100%=0.007%
Bài 2:
nHCl= 73 *25%= 18.25 (g) ; nHCl= 18.25/36.5=0.5(mol)
nAgNO3=34*5%=1.7(g) ; nAgNO3=1.7/170=0.01(mol)
PTHH
..........................HCl + AgNO3 ➞ AgCl + 2HNO3
Trước phản ứng:0.5 : 0.01......................................(mol)
Trong phản ứng:0.01 : 0.01.............. : 0.01 : 0.01(mol)
Sau phản ứng : 0.49: 0 ............... : 0.01 : 0.01(mol)
a) mAgCl=0.01*143.5=1.435(g)
b) mdd sau phản ứng = 73+34-1.435=105.565(g)
C% (HNO3) = (0.01* 63)/105.565*100%=0.0059%
C% (HCl) = (0.49*36.5)/105.565*100%=16.94%

\(MgCO_3+2HCl\rightarrow MgCl_2+H_2O+CO_2\)
\(CO_2+Na\left(OH\right)_2\rightarrow CaCO_3+H_2O\)
b. \(n_{MgCO_3}=\dfrac{21}{84}=0,25mol\) \(\Rightarrow n_{HCl}=2.0,25=0,5mol\)
\(V_{ddHCl}=\dfrac{0,5}{2}=0,25l\)
c. \(n_{CO_2}=n_{MgCO_3}=0,25mol\)
\(n_{CaCO_3}=n_{CO_2}=0,25mol\)
\(\Rightarrow m_{CaCO_3}=0,25.100=25g\)

a) PTHH: \(FeCl_3+3NaOH\rightarrow3NaCl+Fe\left(OH\right)_3\downarrow\)
\(2Fe\left(OH\right)_3+3H_2SO_4\rightarrow Fe_2\left(SO_4\right)_3+6H_2O\)
b) Ta có: \(n_{FeCl_3}=0,3\cdot0,5=0,15\left(mol\right)\)
\(\Rightarrow n_{NaOH}=0,45mol\) \(\Rightarrow V_{ddNaOH}=\dfrac{0,45}{0,25}=1,8\left(l\right)\)
c) Theo PTHH: \(n_{NaCl}=n_{NaOH}=0,45mol\)
\(\Rightarrow C_{M_{NaCl}}=\dfrac{0,45}{2,1}\approx0,21\left(M\right)\)
(Coi như thể tích dd thay đổi không đáng kể)
d) Theo PTHH: \(n_{H_2SO_4}=\dfrac{3}{2}n_{Fe\left(OH\right)_3}=\dfrac{3}{2}n_{FeCl_3}=0,225mol\)
\(\Rightarrow m_{ddH_2SO_4}=\dfrac{0,225\cdot98}{20\%}=110,25\left(g\right)\)
\(\Rightarrow V_{ddH_2SO_4}=\dfrac{110,25}{1,14}\approx96,71\left(ml\right)\)

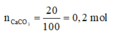
C O 2 + C a C O 3 + H 2 O → C a H C O 3 2
x……….x………..x
Theo PTHH ta có:
n C O 2 l t = x = n C a C O 3 =0,2mol
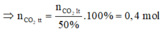
⇒ V C O 2 t t = 0,4.22,4 = 8,96 lit
Ta lại có:
C a O H 2 + C a H C O 3 2 → 2 C a C O 3 + 2 H 2 O
x………..x………2x
Vậy tối thiểu cần là x = 0,2 mol ⇒
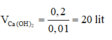
n C a C O 3 = 2x = 0,4 mol
⇒ m↓ = 0,4.100 = 40g
⇒ Chọn C.

\(\text{nAlCl3=0,125}\)
a. AlCl3+3NaOH\(\rightarrow\)Al(OH)3+3NaCl
Al(OH)3+NaOH\(\rightarrow\)NaAlO2+2H2O
Để kết tủa tối đa thì Al(OH)3 không bị hòa tan, hay phản ứng 2 không xảy ra
\(\rightarrow\)\(\text{nAl(OH)3=nAlCl3=0,125}\)
\(\rightarrow\)mAl(OH)3=9,75g
b. Thể tích NaOH 0.25M tối thiểu
-Không có kết tủa khi thể tích=0
-Kết tủa bằng nựa lượng tối đa: nAl(OH)3=\(\frac{0,125}{2}=\frac{1}{16}\)
AlCl3+3NaOH\(\rightarrow\)Al(OH)3+3NaCl
nNaOH=3nAlCl3=\(\frac{3}{16}\)
\(\rightarrow\)V=0,75l