Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án A.
Tại catot: Cu2+: a mol; Na+: b mol;
Cu2+ + 2e → Cu
a ⟶ 2a
Hết Cu2+: 2H2O+2e→2OH−+H2
Tại anot: Cl−: b mol; SO2−4: a mol; H2O
2Cl−→Cl2+2e
b ⟶ b
Hết Cl−: 2H2O − 4e→4H++O2
Vì dung dịch sau điện phân làm phenolphtalein chuyển sang màu hồng chứng tỏ ở catot Cu2+ hết trước Cl− ở anot, còn ở anot Cl− vẫn điện phân ⟹ 2a < b

|
Catôt (-): Cu2+, Na+, H2O |
Anôt (+): SO42-, Cl-, H2O |
|
Cu2+ + 2e = Cu 2H2O + 2e = H2 + 2OH- |
2Cl- - 2e = Cl2 H2O -2e = ½.O2 + 2H+ |
Dung dịch sau đ/p có mt bazơ: OH- được tạo ra sau khi đ/p.
® Khi Cu2+ đ/p thì Cl- đ/p, như vậy để OH- được sinh ra thì: ne(nhận) = 2a < ne(cho) = b.

|
Catôt (-): Cu2+, Na+, H2O |
Anôt (+): SO42-, Cl-, H2O |
|
Cu2+ + 2e = Cu 2H2O + 2e = H2 + 2OH- |
2Cl- - 2e = Cl2 H2O -2e = ½.O2 + 2H+ |
Dung dịch sau đ/p có mt bazơ: OH- được tạo ra sau khi đ/p.
® Khi Cu2+ đ/p thì Cl- đ/p, như vậy để OH- được sinh ra thì: ne(nhận) = 2a < ne(cho) = b.

Bài 1:
A + Cl2 → ACl2 (1)
Fe + ACl2 → FeCl2 + A (2)
x x x (mol)
gọi số mol của Fe phản ứng với một số mol của ACl2 là x
khối lương thanh sắt sau phản ứng là:11,2 - 56x + xMA = 12
=> x =
Ta có:
= 0,25.0,4 = 0,1 (mol)
=> MA = 64 g/mol; Vậy kim loại A là Cu
= nCu =
= 0,2 (mol) =>
= 0,5M
bài 2:
(C17H35COO)3C3H5 + 3NaOH -> 3 C17H35COONa + C3H5(OH)3
890 kg 918 kg
x kg 720 kg
=> x = 698,04 kg.

Đáp án C
Điện phân trong 3378 giây tương đương với số e trao đổi là 0,07 mol
Do trao đổi 0,07 mol e chỉ thu được thêm 0,025 mol Cu, chứng tỏ Cu hết
Lúc này ở catot thu thêm 0,025 mol Cu và 0,01 mol H2
Vậy lúc này ở anot thu được thêm 0,025 mol khí
Do số mol khí trao đổi 0,07 nên chứng tỏ đã có tạo ra O2.
Vậy ở anot thu được Cl2 và O2 với số mol lần lượt là 0,015 và 0,01 mol.
Mặt khác do lúc t giây chỉ thu được Cu ở catot và Cl2 ở anot nên a=b.
Vậy t giây thì n e = 2 a nên 2t giây thì n e = 4 a
Lúc 2t giây ở anot thu được a+0,025 mol Cu và a-0,025 mol H2.
Ở catot thu được a+0,015 mol Cl2 và O2 0,5a-0,0075 mol
Tổng số mol khí thu được là:
a - 0,025 +a + 0,015 + 0,5a - 0,0075 = 2,0625a
Giải được a= 0,04
Vậy số mol CuSO4 là 0,065 mol và KCl là 0,11 mol
=> m = 18,595 gam

 với các chất sau:
với các chất sau:





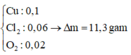
Phản ứng điện phân xảy ra ở các điện cực như sau:
Catot(-): Cu2+ + 2e → Cu; Anot(+): 2Cl- - 2e → Cl2.
Để dung dịch sau điện phân làm dung dịch phenolphtalein chuyển sang màu hồng thì môi trường của dd phải là môi trường bazơ, tức là H2O đã bị điện phân ở Catot và chưa bị điện phân ở Anot. 2H2O + 2e → H2 + 2OH- . Mà số mol e ở Catot = số mol e ở Anot → 2a + nH2O = b → b > 2a.