Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Phương trình điện phân: 4AgNO3 + 2H2O → 4Ag + O2 + 4HNO3 (1)
Dung dịch Y gồm: AgNO3, HNO3. Cho Fe + dd Y sau phản ứng thu được 14,5g hỗn hợp kim loại nên Fe dư có các phản ứng:
3Fe + 8HNO3 → 3Fe(NO3)3 + 2NO + 4H2O (2)
Fe + 2AgNO3 → Fe(NO3)2 + 2Ag (3)
Gọi x là số mol AgNO3 bị điện phân® nHNO3 = x, dung dịch Y: HNO3: x mol; AgNO3 dư: 0,15 –x mol.
Theo (2,3) nFe phản ứng = 3x/8 + (0,15-x)/2 = 0,075 –x/8 mol
nAg = 0,15 – x mol
Vậy mhỗn hợp kim loại = mFedư + mAg =12,6 –(0,075-x/8).56 +(0,15-x).108 =14,5
Suy ra: x= 0,1 mol. Ta có mAg = 0,1.108 ® t = 1,0 h

Đáp án C
Điện phân trong 3378 giây tương đương với số e trao đổi là 0,07 mol
Do trao đổi 0,07 mol e chỉ thu được thêm 0,025 mol Cu, chứng tỏ Cu hết
Lúc này ở catot thu thêm 0,025 mol Cu và 0,01 mol H2
Vậy lúc này ở anot thu được thêm 0,025 mol khí
Do số mol khí trao đổi 0,07 nên chứng tỏ đã có tạo ra O2.
Vậy ở anot thu được Cl2 và O2 với số mol lần lượt là 0,015 và 0,01 mol.
Mặt khác do lúc t giây chỉ thu được Cu ở catot và Cl2 ở anot nên a=b.
Vậy t giây thì n e = 2 a nên 2t giây thì n e = 4 a
Lúc 2t giây ở anot thu được a+0,025 mol Cu và a-0,025 mol H2.
Ở catot thu được a+0,015 mol Cl2 và O2 0,5a-0,0075 mol
Tổng số mol khí thu được là:
a - 0,025 +a + 0,015 + 0,5a - 0,0075 = 2,0625a
Giải được a= 0,04
Vậy số mol CuSO4 là 0,065 mol và KCl là 0,11 mol
=> m = 18,595 gam

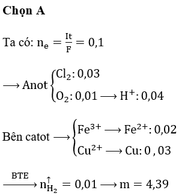
∑ne trao đổi = 0,3 mol < 2nCu2+.
⇒ Cu chưa bị điện phân hết và khí thoát ra là Cl2 và có thể có cả O2.
Nếu chỉ có khí Cl2
⇒ Quy đổi mDung dịch giảm = mCuCl2 = 0,15×135 = 20,25 ≠ 14,75 ⇒ Loại.
+ Vậy có cả O2 thoát ra
⇒ mDung dịch giảm = mCuCl2 + mCuO.
+ Đặt số mol 2 chất lần lượt là a và b ta có:
a + b = 0,15 mol (PT bảo toàn Cu).
135a + 80b = 14,75 (PT theo m dung dịch giảm).
+ Giải hệ ⇒ a = nCuCl2 = 0,05 mol
⇒ nNaCl = 0,05×2 = 0,1 mol.
⇒ CM NaCl = 0 , 1 0 , 2 = 0,5M
Đáp án D
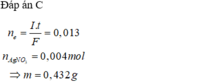
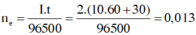
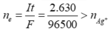





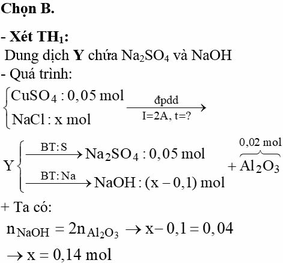
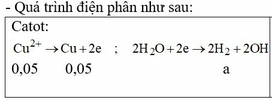

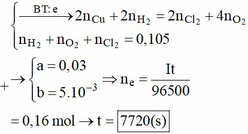

Đáp án C