Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

- Thí nghiệm 1: Gọi hóa trị của X là n
CÓ n H2 = 0,06 ( mol ) => n HCL = 0,12 ( mol )
PTHH: 2X +2n HCL ===> 2XCLn + nH2
theo pthh: n X = 0,12/n ( mol )
=> X = 32,5n
Xét: n = 2 => X = 65 ( Zn )
- Thí nghiệm 2
Gọi CT của oxit : YaOb
PTHH
\(YaOb+2bHCL\rightarrow aYCl_{\dfrac{2b}{a}}+bH2O\)
theo pthh: n YaOb = 0,06/b ( mol )
=> aY + 16b = 160/3 . b
=> Y = 56 . 2b/a
Xét: 2b/a = 3 => Y = 56 ( Fe )

Thể tích dung dịch HCl dùng cho cả 2 phản ứng bằng nhau, nên có cùng số mol. Kí hiệu X, Y là khối lượng mol nguyên tử của 2 kim loại.
Phương trình hoá học của phản ứng :
2X + 2nHCl → 2X Cl n + n H 2 ↑
n H 2 = 0,672 /22,4 = 0,03 mol
Theo đề bài: 0,06/n x X = 1,95 → X = 32,5n
Kẻ bảng
| n | 1 | 2 | 3 |
| X | 32,5 | 65 | 97,5 |
Vậy X là Zn
Y 2 O m + mHCl → Y Cl m + m H 2 O
Theo đề bài, ta có:
(2Y + 16m) = 1,6 → Y = 56/3.m
Kẻ bảng
| m | 1 | 2 | 3 |
| Y | 56,3 | 112/3 | 56 |
Vậy Y là Fe.

Ta có: \(n_{HCl}=0,12.2=0,24\left(mol\right)\)
Gọi CTHH của oxit kim loại là A2On.
PT: \(A_2O_n+2nHCl\rightarrow2ACl_n+nH_2O\)
Theo PT: \(n_{A_2O_n}=\dfrac{1}{2n}n_{HCl}=\dfrac{0,24}{2n}=\dfrac{0,12}{n}\left(mol\right)\)
\(\Rightarrow M_{A_2O_n}=\dfrac{4,8}{\dfrac{0,12}{n}}=40n=2M_A+16n\Rightarrow M_A=12n\)
Với n = 2 thì MA = 24 (g/mol)
Vậy: A là Mg.

Nếu đã khử hoàn toàn thì chất rắn sau pư là Cu và Fe.
Chỉ có Fe tác dụng với HCl tạo ra H2.
nH2=0.448/22.4=0.02 mol
PTHH: Fe + 2HCl ---> FeCl2 +H2(1)
0.02 0.02
mFe=0.02*56=1.12g
=>mCu=1.76-1.12=0.64g
=> nCu=0.64/64=0.01 mol
PTHH: CuO + H2 -----> Cu + H2O(2)
0.01 0.01
mCuO= 0.01*80=0.8 g
=>mFexOy=2.4-0.8=1.6g
PTHH: FexOy + CO ---> xFe + yCO2 (3)
0.02/x 0.02
Giả sử nFexOy = nCuO=0.01 mol
Theo (3), ta có: 0.02/x=0.01 => x=2(*)
Theo đề, ta có; mFexOy= (56x+16y)*0.01=1.6
<=> 0.56x+0.16y=1.6 (**)
Thay(*) vào (**) , giải ra y=3
Vậy CTHH của oxit sắt cần tìm là Fe2O3.
\(n_{H_2}=0,06\left(mol\right)\)
Gọi CTC cuả oxit KL Y là \(Y_mO_n\)
\(2X+2aHCl-->2XCl_a+aH_2\)
0,12/a.....0,12.................................0,06
\(Y_mO_n+2nHCl-->mYCl_{\dfrac{2n}{m}}+nH_2O\)
0,06/n........0,12
Ta có
\(\dfrac{0,12}{a}.X=3,2\Rightarrow3X=80a\)
| a | 1 | 2 | 3 |
| X | 80/3 | 160/3 | 80 |
=> X: Br
Ta có
\(\dfrac{0,06}{n}.\left(mY+16n\right)=3,2\)
\(\Rightarrow\dfrac{0,06Ym}{n}=2,24\)
| m | 1 | 2 | 3 |
| n |
1 |
3 | 4 |
| Y | 112/3 | 56 |
448/9 |
=> Y: Fe

\(CT:A_2O_n\)
\(\%A=\dfrac{2A}{2A+16n}\cdot100\%=70\%\)
\(\Leftrightarrow2A+16n=\dfrac{20}{7}A\)
\(\Leftrightarrow16n=\dfrac{6}{7}A\)
\(\Leftrightarrow A=\dfrac{56}{3}n\)
\(BL:n=3\Rightarrow A=56\)
\(CT:Fe_2O_3\)
\(n_{Fe_2O_3}=\dfrac{40}{160}=0.25\left(mol\right)\)
\(Fe_2O_3+3H_2SO_4\rightarrow Fe_2\left(SO_4\right)_3+3H_2O\)
\(0.25...........0.75\)
\(m_{dd_{H_2SO_4}}=\dfrac{0.75\cdot98}{24.5\%}=300\left(g\right)\)
\(V_{dd_{H_2SO_4}}=\dfrac{300}{1.2}=250\left(ml\right)\)
Nhận thấy rằng oxit không phải trường hợp đặc biệt $Fe_3O_4$
Nên gọi CTTQ của oxit là $R_2O_x$
Ta có: \(\dfrac{2.R.100\%}{2R+16.x}=70\%\Rightarrow0,6R=11,2x\Rightarrow R=\dfrac{56}{3}x\)
Vậy oxit là $Fe_2O_3$
$Fe_2O_3+3H_2SO_4\rightarrow Fe_2(SO_4)_3+3H_2O$
Ta có: $n_{Fe_2O_3}=0,25(mol)\Rightarrow n_{H_2SO_4}=0,75(mol)\Rightarrow V=250(ml)$

=>AO+2HCL->ACL2+H2O(1)
=>HCL+NaOH->NaCL+H2O(2)
(2)=>\(nHCL=nNaOH=\dfrac{100}{1000}.0,1=0,01mol\)
\(\)\(=>nHCL\left(1\right)=\dfrac{500}{1000}.0,1-0,01=0,04mol\)
\(=>nAO=\dfrac{1}{2}nHCL=>=\dfrac{0,8}{A+16}=0,02=>A=24g/mol\)
=>A là Mg =>ct oxit : MgO
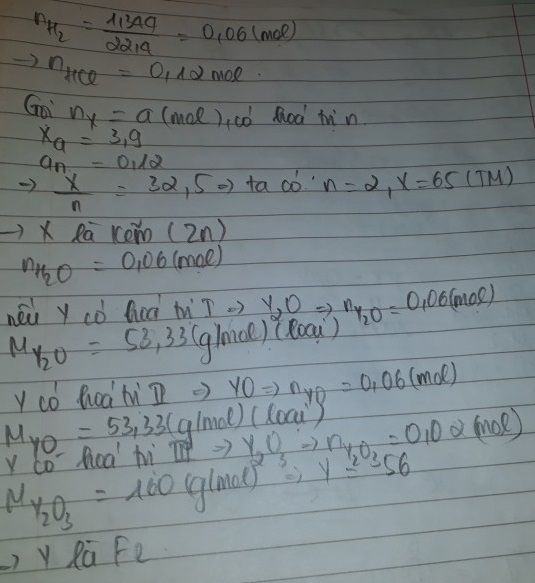
mik sửa lại đề : Để hòa tan 3,9g kim loại X cần dùng thể tích(ml) dd HCl và có 1,344 l H2 bay ra (đktc) . mặt khác để hòa tan 3,2g oxit kim loại Y cần dùng thể tích dd HCl ở trên . hỏi X,Y là kim loại gì ?
2X +2nHCl --> 2XCln +nH2 (1)
YxOy + 2yHCl --> xYCl2y/x + yH2 (2)
nX=3,9/MX (MOL)
nH2=0,06(mol)
theo (1): nX=2/n .nH2=0,12/n(mol)
=> 3,9/MX=0,12/n => MX=32,5n(g/mol)
Xét => X :Zn
nZn=0,06(mol)
nYxOy=3,2/xMY+16y(mol)
theo (2) : nYxOy=1/2y.nHCl=0,06/y(mol)
=> \(\dfrac{3,2}{xMY+16y}=\dfrac{0,06}{y}\)=> MY=\(\dfrac{56}{3}.\dfrac{2y}{x}\) (g/mol)
Xét => Y :Fe