Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Câu 1:
Ta có:
\(m_{NaOH}=80.25\%=20\left(g\right)\)
\(\Rightarrow n_{NaOH}=\frac{20}{23+17}=0,5\left(mol\right)\)
Phản ứng xảy ra:
\(2NaOH+CO_2\rightarrow Na_2CO_3+H_2O\)
\(NaOH+CO_2\rightarrow NaHCO_3\)
Giả sử số mol NaHCO3 là x thì Na2CO3 là 1,5x
\(n_{NaOH}=n_{NaHCO3}+2n_{Na2CO3}=x+1,5x.2=4x\)
\(\Rightarrow x=0,125\left(mol\right)\)
\(\Rightarrow n_{CO2}=n_{NaHCO3}+n_{Na2CO3}=x+1,5x=2,5x=0,3125\left(mol\right)\)
\(\Rightarrow V_{CO2}=0,3125.22,4=7\left(l\right)\)
Câu 2:
\(m_{muoi}=m_{Cl}+m_{SO4}+m_{Na}+m_{Ca}=0,4.35,5+0,2.96+0,5.23+0,15.40\)
\(=50,9\left(g\right)\)
Câu 3:
Muối CuCO3
\(CuSO_4+Na_2CO_3\rightarrow CuCO_3+Na_2SO_4\)
Câu 4
\(n_{CO2}=\frac{0,896}{22,4}=0,04\left(mol\right)\)
Gọi a là mol CaCO3; b là mol BaCO3
\(\Rightarrow100a+197b=4,67\left(1\right)\)
\(CaCO_3+2HCl\rightarrow CaCl_2+CO_2+H_2O\)
\(BaCO_3+2HCl\rightarrow BaCl_2+CO_2+H_2O\)
\(\Rightarrow a+b=0,04\left(2\right)\)
\(\left(1\right)+\left(2\right)\Rightarrow\left\{{}\begin{matrix}a=0,03\\b=0,01\end{matrix}\right.\)
\(\%_{CaCO3}=\frac{0,03.100.100}{4,67}=64,24\%\)
\(\%_{BaCO3}=100\%-64,24\%=35,76\%\)
Câu 5:
\(CaCO_3\underrightarrow{^{to}}CaO+CO_2\)
\(MgCO_3\underrightarrow{^{to}}MgO+CO_2\)
Theo ĐLBTKL, ta có:
mhh = moxit + mCO2
\(\Rightarrow m_{CO2}=m_{hh}-m_{oxit}=26,8-13,6=13,2\left(g\right)\)
\(\Rightarrow n_{CO2}=\frac{13,2}{44}=0,3\left(mol\right)\)
\(\Rightarrow V_{CO2}=0,3.22,4=6,72\left(l\right)\)

\(n_{CaCO3}=\dfrac{2}{100}=0,02\left(mol\right)\)
Bảo toàn nguyên tố C: \(n_{CO}=n_{CaCO_3}=0,02\left(mol\right)\)
\(n_{Cu}=\dfrac{1,92}{64}=0,03\left(mol\right)\)
CuO + CO -------> Cu + CO2
0,02-------->0,02-->0,02
CuO + H2 -------> Cu + H2O
0,01<--------0,03-0,02=0,01
Phần trăm về thể tích cũng là phần trăm về số mol
=>\(\%V_{H_2}=\dfrac{0,01}{0,01+0,02}.100=33,33\%\)
=> %VCO=100- 33,33=66,67%
\(\%m_{H_2}=\dfrac{2.0,01}{2.0,01+44.0,02}.100=2,22\%\)
%mCO= 100-2,22=97,78%
b) \(V_{CO_2}=0,02.22,4=0,448\left(l\right)\)

Bài 1 :
Đặt :
nCuO = x mol
nZnO = y mol
<=> 80x + 81y = 12.1 (1)
nHCl = 0.3 mol
CuO + 2HCl --> CuCl2 + H2O
x______2x
ZnO + 2HCl --> ZnCl2 + H2O
y_______2y
<=> x + y = 0.15 (2)
(1) , (2) :
x = 0.05
y = 0.1
mCuO = 4 g
mZnO = 8.1 g
%CuO = 33.05%
%ZnO = 66.95%
ZnO + H2SO4 --> ZnSO4 + H2O
0.1_____0.1
CuO + H2SO4 --> CuSO4 + H2O
0.05____0.05
mH2SO4 = 14.7 g
nCuCl2 : nZnCl2 = 0.05 : 0.1 = 1 : 2
Bài 2 :
Đặt :
nH2 = 0.2 mol
nAl = x mol
nFe = y mol
mAl + mFe = 7 - 1.5 = 5.5 g
<=> 27x + 56y = 5.5 (1)
2Al + 3H2SO4 --> Al2(SO4)3 + 3H2
x__________________________1.5x
Fe + H2SO4 --> FeSO4 + H2
y_____________________y
<=> 1.5x + y = 0.2 (2)
(1) , (2) :
x = 0.1
y = 0.05
mAl = 2.7 g
mFe = 2.8 g
mCu = 1.5 g
%Al = 38.57%
%Fe = 40%
%Cu = 21.43%
\(n_{CuO}=x;n_{ZnO}=y\)
\(PTHH:CuO+2HCl\rightarrow CuCl_2+H_2O\\ PTHH:ZnO+2HCl\rightarrow ZnCl_2+H_2O\)
\(\Rightarrow hpt:\left\{{}\begin{matrix}80x+81y=12,1\\2\left(x+y\right)=0,3\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}x=0,05\\y=0,1\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}\%m_{CuO}=\frac{0,05.80}{12,1}.100\%=33,1\left(\%\right)\\\%m_{ZnO}=100-33,1=66,9\left(\%\right)\end{matrix}\right.\)
\(PTHH:CuO+H_2SO_4\rightarrow CuSO_4+H_2O\\ PTHH:ZnO+H_2SO_4\rightarrow ZnSO_4+H_2O\)
\(m_{H_2SO_4}=98.\left(0,05+0,1\right)=14,7\left(g\right)\)
\(\frac{n_{CuCl_2}}{n_{ZnCl_2}}=\frac{0,05}{0,1}=\frac{1}{2}\)

PTHH: K2CO3 + 2 HCl ->2 KCl + H2O + CO2
x___________2x______2x____________x(mol)
KHCO3 + HCl -> KCl + H2O + CO2
y____y__________y_______y(mol)
mHCl= 27,375.0,2= 5,475
Ta có hpt:
\(\left\{{}\begin{matrix}2.36,5x+36,5y=5,475\\22,4x+22,4y=2,24\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}x=0,05\left(mol\right)\\x=0,05\left(mol\right)\end{matrix}\right.\)
mK2CO3= 0,05.138= 6,9(g)
mKHCO3= 0,05.100=5(g)
=> %mK2CO3= (6,9/11,9).100=57,893%
=> %mKHCO3= 100%- 57,893%= 42,107%
c) mKCl= 0,15. 74,5=11,175(g)
mddKCl= mhh+ mddHCl - mCO2= 11,9+27,375- 0,1.44=34,875(g)
=> C%ddKCl = (11,175/34,875).100=32,043%

3. CuO +H2SO4 -->CuSO4 +H2O
nCuO=64/80=0,8(mol)
theo PTHH :nCuO =nH2SO4=nCuSO4=0,8(mol)
=>mddH2SO4 20%=0,8.98.100/20=392(g)
mCuSO4=0,8.160=128(g)
mdd sau phản ứng =64 +392=456(g)
mH2O=456 -128=328(g)
giả sử có a g CuSO4.5H2O tách ra
trong 250g CuSO4 tách ra có 160g CuSO4 và 90g H2O tách ra
=> trong a g CuSO4.5H2O tách ra có : 160a/250 g CuSO4 và 90a/250 g H2O tách ra
=>mCuSO4(còn lại)=128 -160a/250 (g)
mH2O (còn lại)=328 -90a/250 (g)
=>\(\dfrac{128-\dfrac{160a}{250}}{328-\dfrac{90a}{250}}.100=25\)
=>a=83,63(g)

m rắn giảm = mO (oxit) => nO (oxit) = (1,6 – 1,408) : 16 = 0,012mol
Dễ thấy n = nO (oxit) = 0,012mol
=> nH2 ban đầu = 0,012 : 80% = 0,015
=> nFe = nH2= 0,015 → x = 0,015
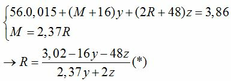
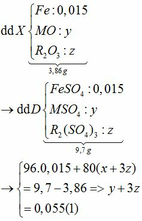
Ta có: CO + O(Oxit) → CO2
Vì: m(Rắn giảm) = mO(Oxit) → nO(Oxit) = (3,86 – 3,46) : 16 = 0,025
TH1: cả 2 oxit đều bị khử bởi CO
→ nO(Oxit) = y + 3z = 0,025 kết hợp với (1) loại
TH2: chỉ có MO bị khử bởi CO
→ nO(Oxit) = nMO = 0,025 → y = 0,025 kết hợp với (1) => z = 0,01
Kết hợp với (*) => M = 64 (Cu)
TH3: chỉ có R2O3 bị khử bởi CO
→ nO(Oxit) = 3.nR2O3 → z = 0,025/3 kết hợp với (1) => y = 0,03
Kết hợp với (*) y => M lẻ => loại
Vậy %m các chất trong X là: 21,76%; 51,81%; 26,43%

nH2 = \(\dfrac{1,792}{22,4}\) = 0,08 mol
KL không phản ứng là Cu
2Al + 6HCl -> 2AlCl3 + 3H2 \(\uparrow\)
x--------------------------->1,5x
Fe + 2HCl -> FeCl2 + H2 \(\uparrow\)
y------------------------>y
-ta có \(\left\{{}\begin{matrix}27x+56y=3,34\\1,5x+y=0,08\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}x=0,02mol\\y=0,05mol\end{matrix}\right.\)
=> %Al = \(\dfrac{0,02.27}{4,54}.100\%\approx11,9\%\)
=>%Cu = \(\dfrac{1,2}{4,54}.100\%\approx26,4\%\)
=>%Fe = 100% - 11,9% - 26,4% = 61,7%
Gọi a,b là số mol của ZnO và Fe2O3
PT: CO + ZnO→ Zn+ CO2
a--------------a
3CO + Fe2O3➞ 2Fe+ 3CO2
b-----------------3b
CO2 + Ca(OH)2➝ CaCO3 + H2O biết m caco3 = 35g⇒ n caco3 =35/100 = 0,35 mol n co2 = 0,35 mol
Ta có : 81a + 160b = 20,05 g
a +3b = 0,35 mol
gải pt được : a = 0,05 mol ; b= 0,1 mol
⇒m zno= 0,05*81 = 4,05g
⇒mfe2o3 = 20,05- 4,05 = 16 g
%ZnO =4,05/20,05* 100% =20%
%Fe2O3 = 80%