Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án C
(2) , ( 5) , ( 7)
Điều kiện xảy ra ăn mòn điện hóa học: đồng thời cả 3 điều kiện sau
- Các điện cực phải khác nhau về bản chất. Có thể là cặp hai kim loại khác nhau, kim loại – phi kim hay kim loại – hợp chất. Kim loại có thế điện cực chuẩn nhỏ hơn là cực âm
- Các điện cực phải tiếp xúc trực tiếp hoặc gián tiếp với nhau qua dây dẫn
- Các điện cực cùng tiếp xúc với dung dịch chất điện li
Gang, thép là hợp kim Fe – C
Không khí ẩm có chứa H2O, CO2, O2…tạo ra lớp dung dịch chất điện li phủ lên bề mặt gang, thép làm xuất hiện vô số pin điện hóa mà Fe là cực âm, C là cực dương.

Chọn đáp án C
Thí nghiệm xảy ra ăn mọn điện hóa là (2), (5) và (7) ⇒ Chọn C
______________________________
+ Loại (3) vì Cu và Ag đều không tác dụng với HCl.
+ Loại (4) vì thiếc (Sn) tráng thanh sắt (Fe)
⇒ Không có 2 kim loại nhúng trong cùng 1 dung dịch chất điện li.
+ Loại (6) vì không thỏa điều kiện nhúng trong dung dịch chất điện ly.

D
- Hòa tan các mẫu hợp kim vào H2O dư:
+ Chất rắn không tan: Mg-Al, Mg-Ag (1)
+ Chất rắn tan 1 phần, có khí thoát ra: Mg-K
\(2K+2H_2O\rightarrow2KOH+H_2\)
- Lọc lấy dd thu được sau khi hòa tan Mg-K vào nước, cho 2 hợp kim ở (1) tác dụng với dd thu được:
+ Chất rắn không tan: Mg-Ag
+ Chất rắn tan 1 phần, có khí thoát ra: Mg-Al
\(2Al+2KOH+2H_2O\rightarrow2KAlO_2+3H_2\)

Đáp án A
a. nung NH4NO3
NH4NO3 => N2O + 2H2O
b. đun nóng nacl tinh thể với dd H2SO4đặc
2NaCl +H2SO4 => Na2SO4 + 2HCl
c.sục khí Cl2 vào dd NaHCO3
Cl2 + 2NaHCO3 => 2NaCl + 2CO2 + 1/2O2 + H2O
d. sục khí co2 vào dd Ca(OH)2 dư
CO2 + Ca(OH)2 => CaCO3 + H2O
e. sục SO2 vào dd KMnO4
5 SO2 + 2 KMnO4 + 2 H2O => K2SO4 + 2 MnSO4 + 2 H2SO4
g. cho dd KHSO4 vào dd NaHCO3
KHSO4 + NaHCO3 => K2SO4 + Na2SO4 + CO2 + H2O
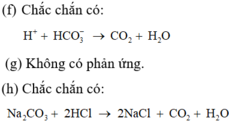
h. cho PbS vào dd HCl loãng : không phản ứng.
i. cho Na2SO3 vào dung dịch H2SO4 dư đun nóng
Na2SO3 + H2SO4 => Na2SO4 + H2O + SO2

Chọn đáp án A
Số thí nghiệm sinh ra chất khí là:
(a)(b) (g) (h) (i)

Đáp án cần chọn là: D
(a) đúng tạo AgCl
(b) sai vì A l 2 O 3 tan hết trong HCl
(c) đúng vì Cu không tác dụng với HCl nên còn nguyên sau phản ứng
(d) đúng do tạo kết tủa B a C O 3 : B a O H 2 + K H C O 3 → B a C O 3 + KOH + H 2 O
Vậy có 3 thí nghiệm thu được chất rắn sau phản ứng.

PTHH
Fe + 2HCl --->FeCl2 + H2
0.5==1======0.5====0.5
2H2 + 02 ---->2H20
0.5========0.5
nH20=0.5
nHCl=2 =>nHCl dư=1mol
PTHH:
10FeCl2 + 6KMnO4 + 24H2SO4 ----> 3K2SO4 + 5Fe2(SO4)3 + 6MnSO4 + 10Cl2 + 24H2O
0.25======0.15========================...
2KMnO4 + 16HCl --> 2MnCl2 + 5Cl2 + 2KCl + 8H2O
0.0625=====0.5===========0.15625
Cl2 + 2FeCl2 ----->2FeCl3
=====0.25======0.25
nKMn04=0.2125mol
VKMn04=0.425
mFeCl3=40.625g
Nếu sửa nồng độ HCl thành 0.65 :
nHCl dư=1.6 mol
2KMnO4 + 16HCl --> 2MnCl2 + 5Cl2 + 2KCl + 8H2O
0.1=======0.8
nKMn04=0.25 mol
=>VKMn04=0.5 (l)

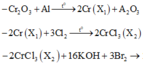
Chọn D