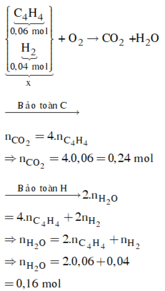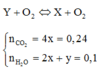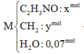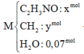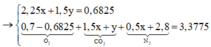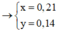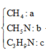Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Chọn đáp án D
Ta có mZ = 0,2 × 8,5×2 = 3,4 gam.
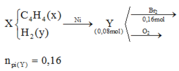
Ta có sơ đồ
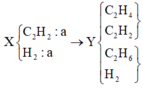
+ Theo định luật BTKL ⇒ mC2H2 + mH2 = 19 + 3,4 = 22,4 gam
⇒ nC2H2 = nH2 = 22,4 ÷ (26 + 2) = 0,8 mol
+ Vì thành phần nguyên tố C và H trong X và Y như nhau.
⇒ Đốt cháy hoàn toàn hh Y hay X thì đều cần 1 lượng oxi như nhau.
Ta có sơ đồ đốt cháy
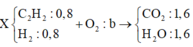
⇒nO2 = b = nCO2 + ½ nH2O = 2,4 mol ⇒ VO2 = 53,76 lít ⇒ Chọn D

Chọn D.
Giả sử có 1 mol hỗn hợp Y. Làm lạnh Y Þ H2O: 0,425 mol và Z: 0,575 mol
Dẫn Z qua dung dịch KOH dư Þ CO2: 0,5217.0,575 = 0,3 mol Þ O2 dư: 0,275 mol
Nhận thấy: n C O 2 < n H 2 O nên X là ankan với n X = n H 2 O - n C O 2 = 0 , 125 m o l ⇒ C X = 2 , 4
Vậy 2 ankan trong X là C2H6 (0,075 mol) và C3H8 (0,05 mol) ⇒ % m C 2 H 6 = 50 , 56 %